Clear Sky Science · fr
NatA participe à des complexes multifactoriels à la sortie du tunnel polypeptidique ribosomal
Comment les cellules affinent les nouvelles protéines dès leur naissance
Chaque seconde, vos cellules fabriquent des milliers de nouvelles protéines sur de petites machines appelées ribosomes. À mesure que chaque chaîne protéique émerge, elle doit être coupée, marquée et repliée correctement, sinon elle peut mal fonctionner et contribuer à la maladie. Cette étude examine l’un des systèmes de marquage clés, une modification appelée acétylation N-terminale, et montre comment un complexe enzymatique central, NatA, coopère avec plusieurs partenaires précisément à l’endroit où les nouvelles protéines sortent du ribosome. Comprendre cette chorégraphie aide à expliquer comment les cellules maintiennent le bon fonctionnement de leurs usines à protéines.
La petite étiquette chimique qui compte
La plupart des protéines commencent leur vie avec le même premier bloc de construction, l’acide aminé méthionine. Souvent, cette méthionine initiale est retirée et remplacée par une petite étiquette chimique appelée groupe acétyle. Cette étiquette, ajoutée à l’extrémité de la protéine (son N‑terminus), peut influencer la durée de vie de la protéine, sa localisation dans la cellule et son fonctionnement. Deux grands types d’enzymes se tiennent à la sortie du tunnel ribosomal pour gérer cette première transformation : les méthionine aminopeptidases (MAP), qui coupent la méthionine de départ, et les N‑terminal acetyltransferases (NAT), qui ajoutent l’étiquette acétyle. Parmi les NAT, NatA est le moteur dans les cellules humaines, modifiant potentiellement près de 40 % de toutes les protéines. Parce que de nombreuses protéines sont synthétisées simultanément, la cellule doit organiser ces enzymes pour que la coupe et le marquage se fassent rapidement et dans le bon ordre.
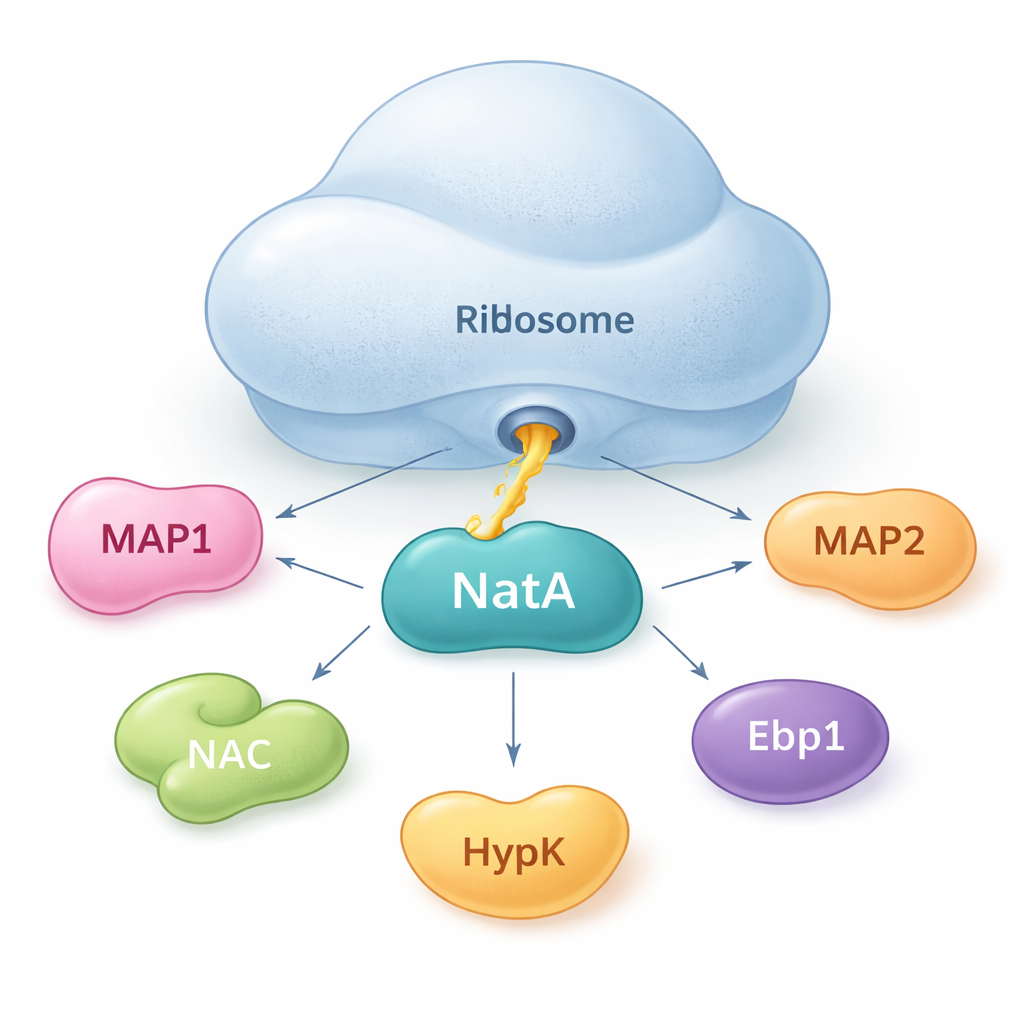
NatA comme point de rencontre pour les aides protéiques
Les auteurs montrent que NatA n’agit pas seul. Il se comporte plutôt comme un hub qui rassemble plusieurs protéines auxiliaires, à la fois sur le ribosome et en solution. Grâce à des mesures de liaison sensibles en solution, ils ont constaté que NatA peut former des complexes stables avec MAP1, le complexe d’association aux polypeptides naissants (NAC), la protéine régulatrice HypK, et une autre enzyme, Naa50, même en l’absence du ribosome. NAC peut faire le lien entre NatA et MAP1, permettant que la coupe et le marquage soient couplés au sein d’un même assemblage. Cependant, HypK, qui inhibe habituellement l’activité de NatA, peut empêcher la liaison de NAC. Cela suggère que la cellule peut basculer NatA entre un état plus actif lié à NAC et un état restreint lié à HypK, selon ses besoins.
Un second point d’ancrage juste à la sortie du tunnel
En utilisant la cryo‑microscopie électronique, une technique qui image de grandes molécules en détail quasi atomique, les chercheurs ont découvert que NatA peut se lier au ribosome en deux positions distinctes. Un site, connu auparavant, se situe un peu à l’écart de la sortie du tunnel. Le nouveau site « proximal » place le cœur catalytique de NatA très près de l’endroit où la chaîne protéique en croissance émerge, raccourcissant la distance que la chaîne doit parcourir pour être modifiée. Fait remarquable, les deux positions peuvent être occupées simultanément, ce qui signifie que deux complexes NatA peuvent siéger sur le même ribosome. La copie la plus éloignée joue le rôle d’échafaudage et d’ancrage, tandis que la copie proximale est idéalement placée pour marquer les nouvelles protéines. Les deux molécules de NatA se touchent aussi, indiquant que NatA peut coordonner ses propres duplicatas en équipes multi‑enzymatiques.
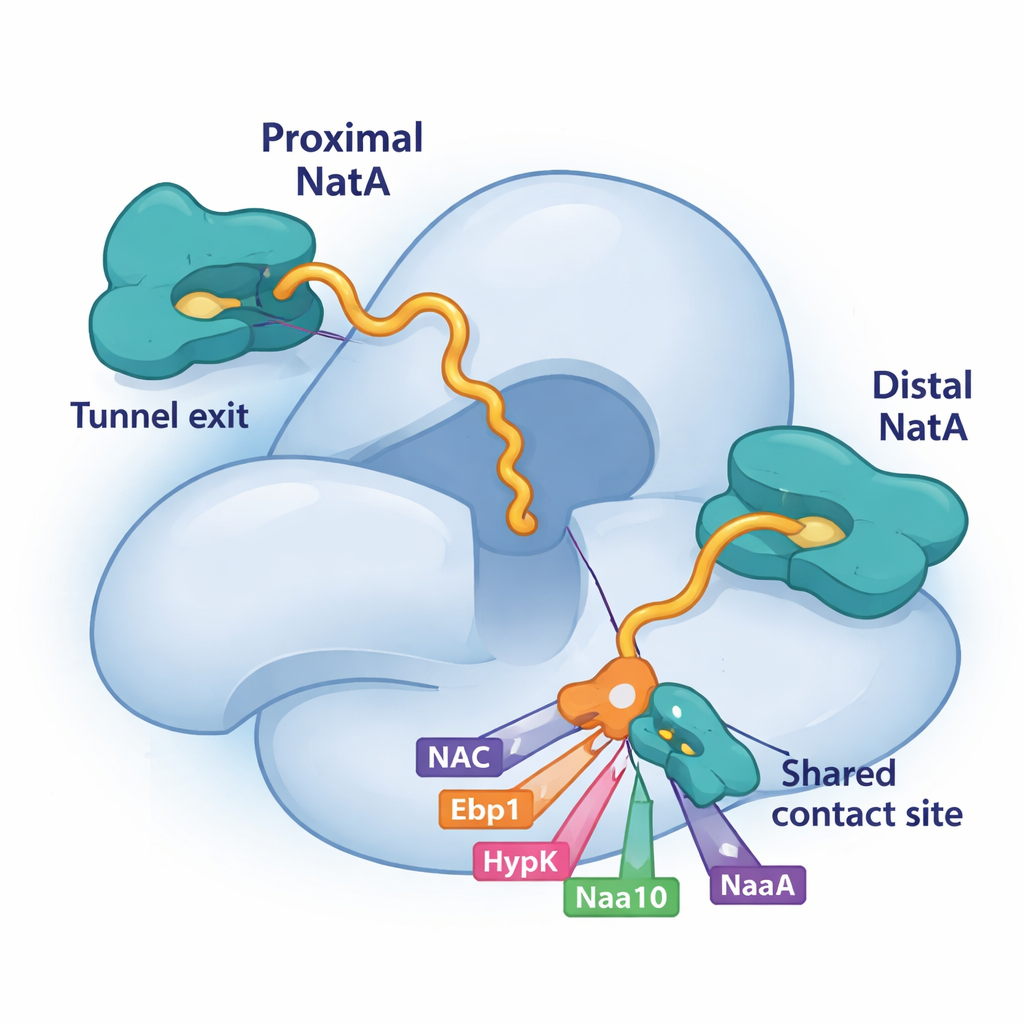
Compétition pour une même plateforme d’accueil sur NatA
Un élément clé de ce puzzle est une petite gouttière sur la grande sous‑unité de NatA, Naa15. L’étude montre que quatre facteurs associés au ribosome — NAC, HypK, Ebp1 et même un segment terminal de la propre sous‑unité catalytique de NatA, Naa10 — utilisent de courtes hélices pour se fixer exactement sur la même zone de Naa15. Parce qu’ils dépendent tous de cette plateforme partagée, ils doivent se concurrencer pour l’accès. Lorsque HypK occupe le site, il non seulement éteint l’activité de NatA, mais empêche aussi NatA de s’associer à NAC ou de former des dimères NatA–NatA. Lorsque NAC, le pseudo‑enzyme Ebp1 ou Naa10 proximal se lient à la place, ils peuvent remodeler la position de NatA ou ses connexions au ribosome. Cette liaison compétitive offre à la cellule un moyen flexible de choisir quels partenaires s’assemblent autour de NatA à un moment donné.
Un pseudo‑enzyme en régulateur de circulation
La protéine Ebp1 est particulièrement intrigante. Elle ressemble à l’une des enzymes qui retirent la méthionine mais lui manque l’activité catalytique ; c’est un « pseudo‑enzyme ». Des travaux antérieurs ont montré qu’Ebp1 peut se placer sur le ribosome près de la sortie du tunnel et serrer un long segment d’ARN. Dans cette étude, les auteurs trouvent que lorsque NatA rejoint le ribosome, Ebp1 change de position, lâche l’ARN et utilise plutôt sa propre hélice pour occuper le même site de liaison sur Naa15 que NAC et HypK. Cette réorganisation suggère qu’Ebp1 peut agir comme un remplaçant ou un organisateur : il peut façonner l’environnement local de l’ARN puis céder le contrôle aux enzymes actives comme les MAP et NatA, sans effectuer lui‑même de réaction chimique.
Pourquoi ce contrôle moléculaire de la circulation importe
Pour un non‑spécialiste, les détails des hélices et des sites de liaison peuvent sembler abstraits, mais le message est simple : les cellules exécutent un système de contrôle qualité multi‑étapes hautement chorégraphié exactement là où les protéines naissent. NatA se situe au centre de ce système, capable de recruter ou de libérer différents partenaires selon les facteurs qui remportent l’accès à une plaque d’ancrage cruciale et selon le site ribosomal occupé par NatA. Ce réseau flexible aide à garantir que la coupe et l’acétylation se déroulent avec le bon timing et dans le bon ordre pour des milliers de protéines différentes. Parce que des erreurs dans le traitement N‑terminal sont liées à des troubles du développement, à la neurodégénérescence et au cancer, cartographier la façon dont NatA et ses partenaires s’assemblent donne aux chercheurs une feuille de route plus claire sur le contrôle du traitement protéique précoce — et sur la façon de l’intervenir lorsqu’il dysfonctionne.
Citation: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Mots-clés: contrôle de la qualité des protéines, acétylation N-terminale, sortie du tunnel ribosomal, complexe NatA, modification co-traductionnelle