Clear Sky Science · fr
La fucosyltransférase végétale FUT11 déforme l’accepteur sucré pour catalyser via un intermédiaire oxocarbenioum transitoire
Comment les plantes ajustent les sucres sur leurs protéines
Les protéines de nos cellules, comme celles des plantes, sont souvent parées de chaînes complexes de sucres qui jouent un rôle de « code-barres », guidant le repliement des protéines, leur durée de vie et les partenaires qu’elles peuvent lier. Cette étude se concentre sur une enzyme végétale appelée FUT11 qui ajoute un petit sucre, la fucose, à ces chaînes. En révélant précisément comment FUT11 agit au niveau atomique, les auteurs mettent au jour une astuce surprenante : l’enzyme courbe brièvement son partenaire sucré hors de sa forme stable pour favoriser une étape chimique difficile. Comprendre ce processus importe non seulement pour la biologie fondamentale, mais aussi pour concevoir des médicaments d’origine végétale plus sûrs, qui évitent de déclencher des réactions immunitaires indésirables chez l’humain.
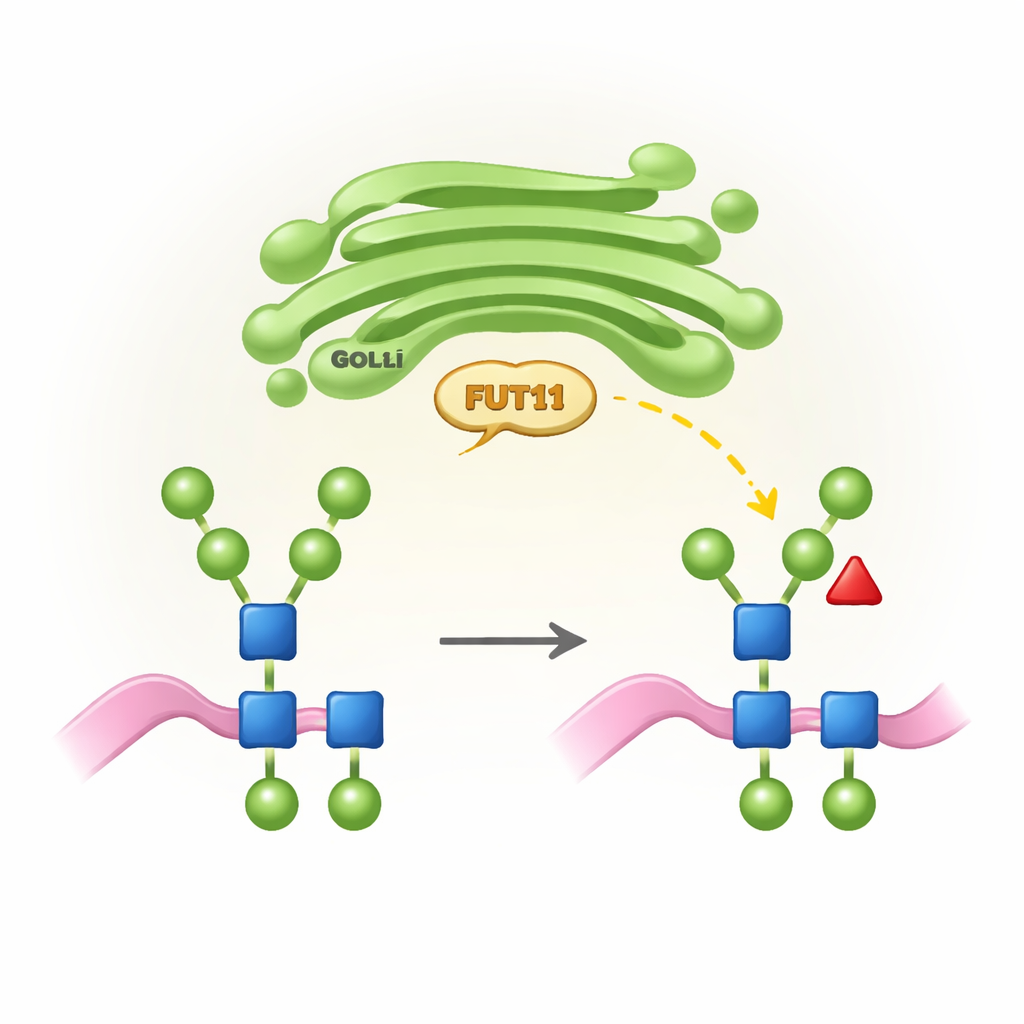
Étiquettes sucrées spécifiques aux plantes et leur importance
Tous les organismes supérieurs utilisent un processus appelé N-glycosylation pour attacher des chaînes de sucres (N-glycanes) à certains sites des protéines. Chez les animaux, ces chaînes sont remodelées dans l’appareil de Golgi pour former des structures élaborées qui se terminent souvent par des acides sialiques et portent une fucose centrale en une position spécifique. Les plantes, en revanche, suivent une « règle de conception » différente : leurs N-glycanes manquent typiquement d’acide sialique mais comportent une fucose centrale en une autre position (appelée b1,3) ainsi qu’un xylose supplémentaire. Ces caractéristiques propres aux plantes sont essentielles à la croissance et à la fertilité normales, mais elles peuvent être perçues comme étrangères par le système immunitaire humain. FUT11 est l’une des enzymes végétales clés qui installent cette fucose centrale, et son activité influence à la fois le développement des plantes et la manière dont les protéines thérapeutiques produites en plante seront perçues dans notre organisme.
Cartographier où FUT11 peut agir sur des ramifications sucrées complexes
Pour comprendre ce que FUT11 reconnaît, les chercheurs ont testé l’enzyme sur une microplaque contenant 144 structures différentes de N-glycanes. Ils ont découvert que FUT11 est assez sélective vis‑à‑vis d’une branche de l’arbre sucré — l’« embranchement b1,3 » — qui doit porter un élément particulier (un N‑acétylglucosamine terminal, ou GlcNAc) pour que la réaction ait lieu. En parallèle, FUT11 tolère d’autres décorations : elle fonctionne encore lorsque le mannose central porte un xylose propre aux plantes, et même lorsqu’une autre fucose a déjà été ajoutée à la position animale du cœur. L’embranchement opposé (b1,6) est en grande partie exposé au solvant et n’établit que des contacts faibles avec l’enzyme, ce qui explique pourquoi FUT11 peut accepter une grande variété de modifications à cet endroit. Ces préférences de liaison aident à expliquer pourquoi les plantes produisent un ensemble caractéristique de structures de N-glycanes et indiquent comment FUT11 pourrait être utilisée ou évitée dans le cadre de la modification génétique des cellules végétales pour la biotechnologie.
Un agencement structural unique pour saisir et positionner les sucres
Par cristallographie aux rayons X, l’équipe a résolu la structure tridimensionnelle de FUT11 liée à son donneur de sucre (GDP‑fucose) et à un accepteur N‑glycane. L’enzyme présente une architecture à deux lobes de type « GT‑B » : un lobe accueille le GDP‑fucose, tandis qu’un lobe accepteur anormalement élaboré, incluant un sous‑domaine N‑terminal spécifique aux plantes, enveloppe le N‑glycane. Ce sous‑domaine additionnel, relié au reste de l’enzyme par des ponts disulfure, ancre la partie centrale du glycan et aide à exposer l’unité réactive GlcNAc vers le donneur. Des mutations de résidus clés ont confirmé leurs rôles : changer un seul glutamate (Glu158) élimine l’activité, tandis que modifier deux résidus voisins affaiblit fortement la fucosylation dans des cellules humaines modifiées. Ces résultats relient des clichés structurels à la fonction cellulaire réelle, montrant exactement quelles parties de la protéine sont indispensables à la liaison et à la catalyse.
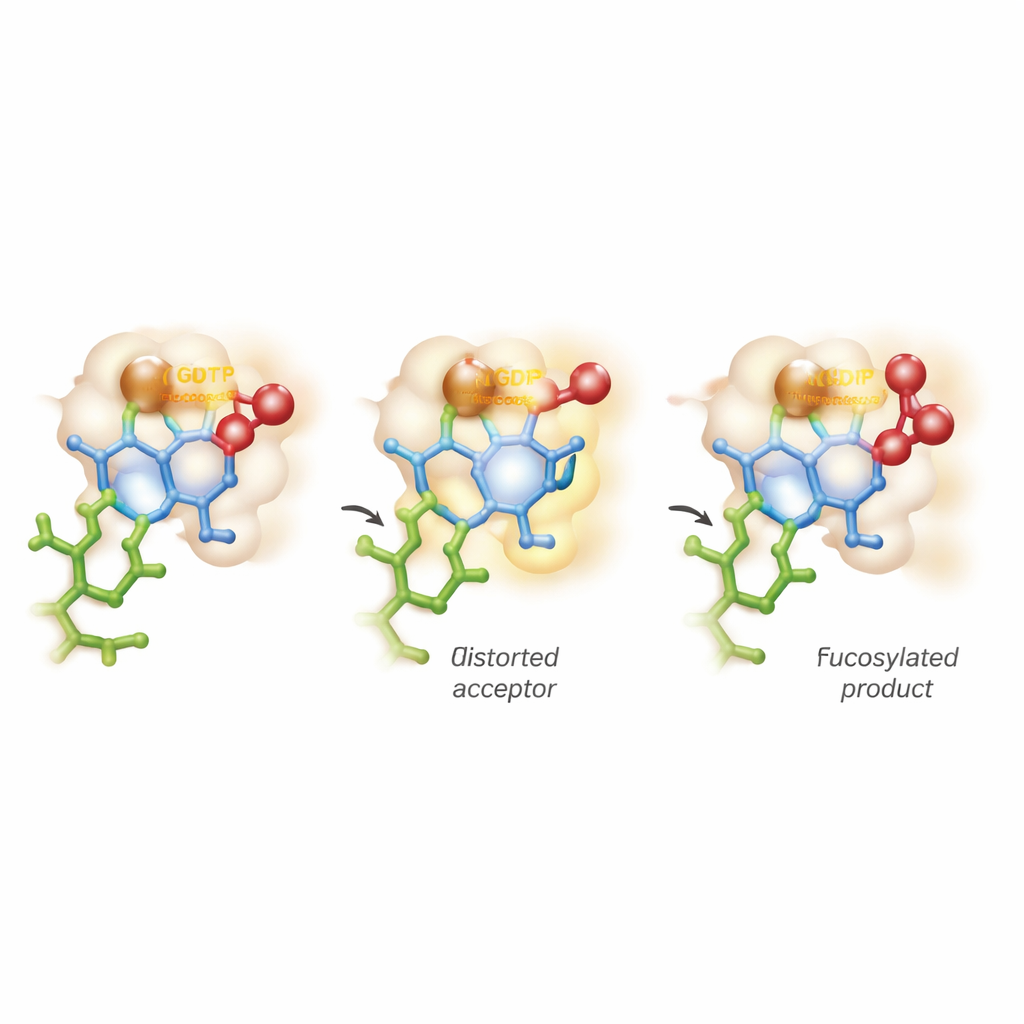
Déformer le sucre et naviguer entre deux voies réactionnelles
L’aperçu le plus frappant provient de simulations informatiques avancées combinant mécanique quantique et dynamique moléculaire. Les vues traditionnelles supposent que le sucre accepteur conserve sa forme stable en chaise pendant que l’enzyme active simplement le donneur. Ici, FUT11 se montre plus agressive : des interactions pilotées par Glu158 déforment temporairement l’anneau GlcNAc interne en une conformation moins confortable et plus « gauchie ». Dans cette posture contrainte, le groupe hydroxyle critique s’aligne parfaitement pour attaquer le donneur de fucose. Les calculs montrent que, lorsque la liaison chimique au GDP se rompt, un état bref et chargé positivement « de type oxocarbenioum » apparaît sur le sucre, avant que la nouvelle liaison à l’accepteur soit complètement formée. Cela signifie que la réaction ne se range pas strictement dans les catégories SN1 ou SN2 classiques, mais progresse le long d’un continuum, de façon asynchrone et quasi‑étape par étape.
Flexibilité cachée et échos évolutifs
En comparant FUT11 à une enzyme humaine apparentée, FUT9, les auteurs ont constaté que l’enzyme végétale peut aussi, quoique faiblement, modifier un autre motif sucré (LacNAc) pour former une structure connue sous le nom de Lewis X. Cette activité secondaire n’est probablement pas importante biologiquement chez les plantes, où Lewis X n’est pas normalement présent, mais elle met en évidence comment des échafaudages protéiques similaires peuvent être recyclés au cours de l’évolution pour agir sur des contextes sucrés différents. L’étude suggère que FUT11 et ses apparentées partagent un cadre modulaire pour reconnaître les N‑glycanes, avec des ajustements subtils qui déplacent la spécificité entre le cœur végétal et les antennes animales.
Pourquoi cette astuce de déformation compte pour la science et la médecine
Ensemble, les travaux montrent que FUT11 ne se contente pas de rapprocher deux partenaires sucrés : elle plie activement l’accepteur en une pose réactive et oriente la chimie via un intermédiaire chargé et fugitif. Pour un lecteur non spécialiste, cela signifie que le sucre sur la protéine n’est pas un simple site de docking rigide mais un participant flexible que l’enzyme modèle selon ses besoins. Cette nouvelle vision de la « catalyse par conformation » aide à expliquer comment les enzymes obtiennent à la fois vitesse et sélectivité et fournit une feuille de route pour redesigner les voies de glycosylation. Concrètement, connaître précisément comment FUT11 reconnaît et modifie les N‑glycanes végétaux peut guider l’ingénierie des plantes cultivées et des systèmes de production végétaux pour minimiser les motifs sucrés susceptibles de déclencher des réponses immunitaires dans les thérapies humaines, ou pour créer des glycoprotéines sur mesure avec des propriétés biologiques ciblées.
Citation: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Mots-clés: glycosylation végétale, fucosyltransférase FUT11, N-glycanes, mécanisme enzymatique, glico-ingénierie