Clear Sky Science · fr
Stimulation médullaire pour les troubles de la marche dans la maladie de Parkinson : essai pilote randomisé en double aveugle avec prolongation en ouvert
Quand marcher devient un combat quotidien
Beaucoup de personnes atteintes de la maladie de Parkinson constatent que la marche, auparavant automatique, devient une difficulté permanente. Leurs pieds peuvent soudainement sembler « collés » au sol, rendant les tâches quotidiennes risquées et épuisantes. Cette étude posait une question simple mais importante : un petit dispositif implanté qui envoie de douces impulsions électriques à la moelle épinière peut‑il, en toute sécurité, aider ces patients à mieux marcher, et vaut‑il la peine d’être testé dans des essais plus larges ?
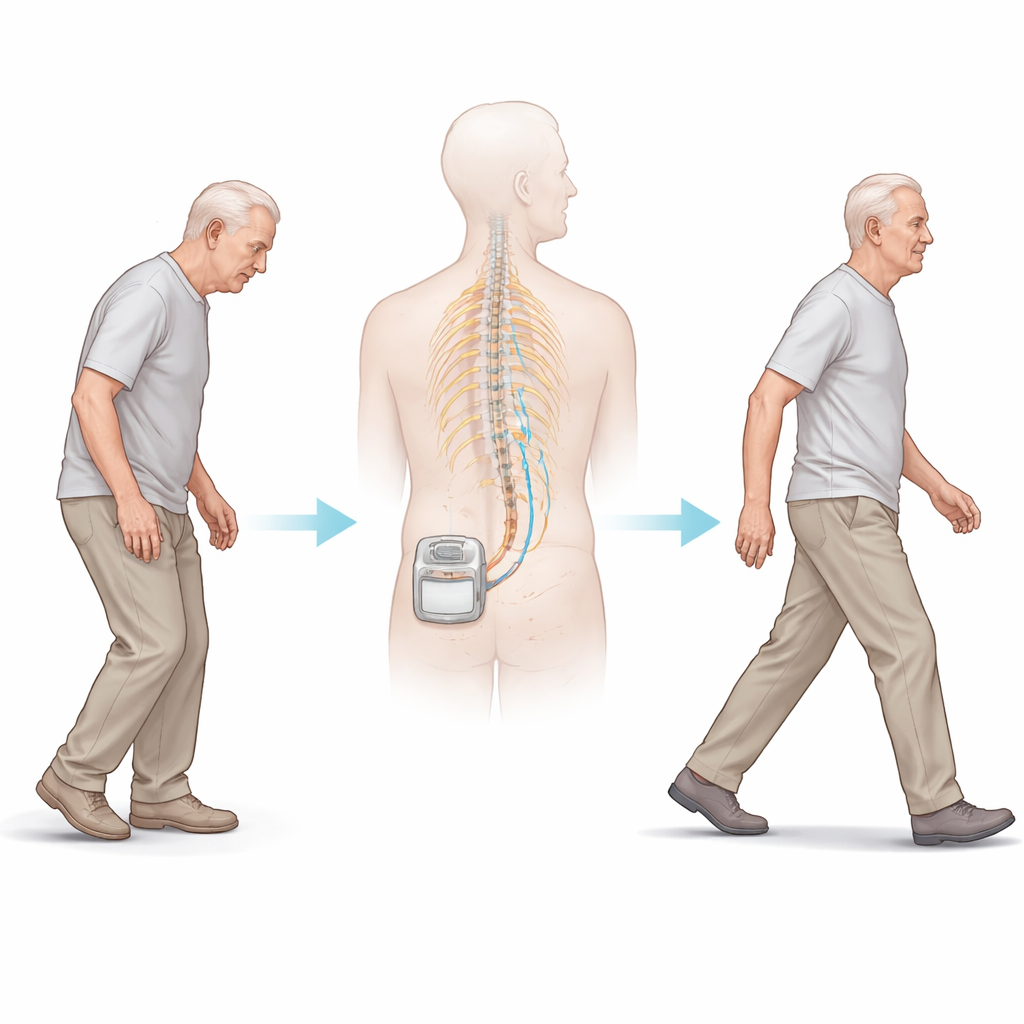
Une nouvelle application d’un traitement de la douleur
La stimulation de la moelle épinière est déjà utilisée pour soulager des douleurs sévères et chroniques. Les chirurgiens posent une fine électrode le long de la colonne vertébrale et la relient à un générateur d’impulsions alimenté par batterie sous la peau. L’appareil délivre de très brèves décharges électriques aux voies nerveuses. Au cours de la dernière décennie, des cliniciens ont rapporté que certaines personnes atteintes de Parkinson traitées ainsi pour des douleurs dorsales semblaient également marcher plus facilement. Cette observation a inspiré l’essai STEP‑PD, qui a testé un schéma spécifique de stimulation en « rafales » conçu pour ne pas provoquer de sensations de picotement, afin de permettre une comparaison équitable entre la stimulation réelle et une condition factice (appareil éteint).
Organisation de l’essai
Les chercheurs ont recruté des personnes atteintes de Parkinson souffrant d’un blocage de la marche malgré un traitement médicamenteux optimal. Après l’implantation du stimulateur médullaire au niveau du milieu du dos, douze participants ont entamé une phase de six mois en double aveugle : la moitié a été assignée aléatoirement à la stimulation en rafales, l’autre moitié à l’appareil éteint. Ni les patients ni les médecins évaluateurs ne savaient qui appartenait à quel groupe. Tous les participants ont ensuite poursuivi six mois supplémentaires en ouvert, où chacun a reçu la stimulation active. En cours d’étude, l’équipe a évalué l’équilibre et la marche à l’aide de scores moteurs standardisés, de tests de marche simples, de capteurs à domicile et de questionnaires sur la mobilité et la qualité de vie. Des examens cérébraux par TEP de deux types ont suivi l’activité cérébrale et un système de signalisation chimique lié à l’attention et au mouvement.
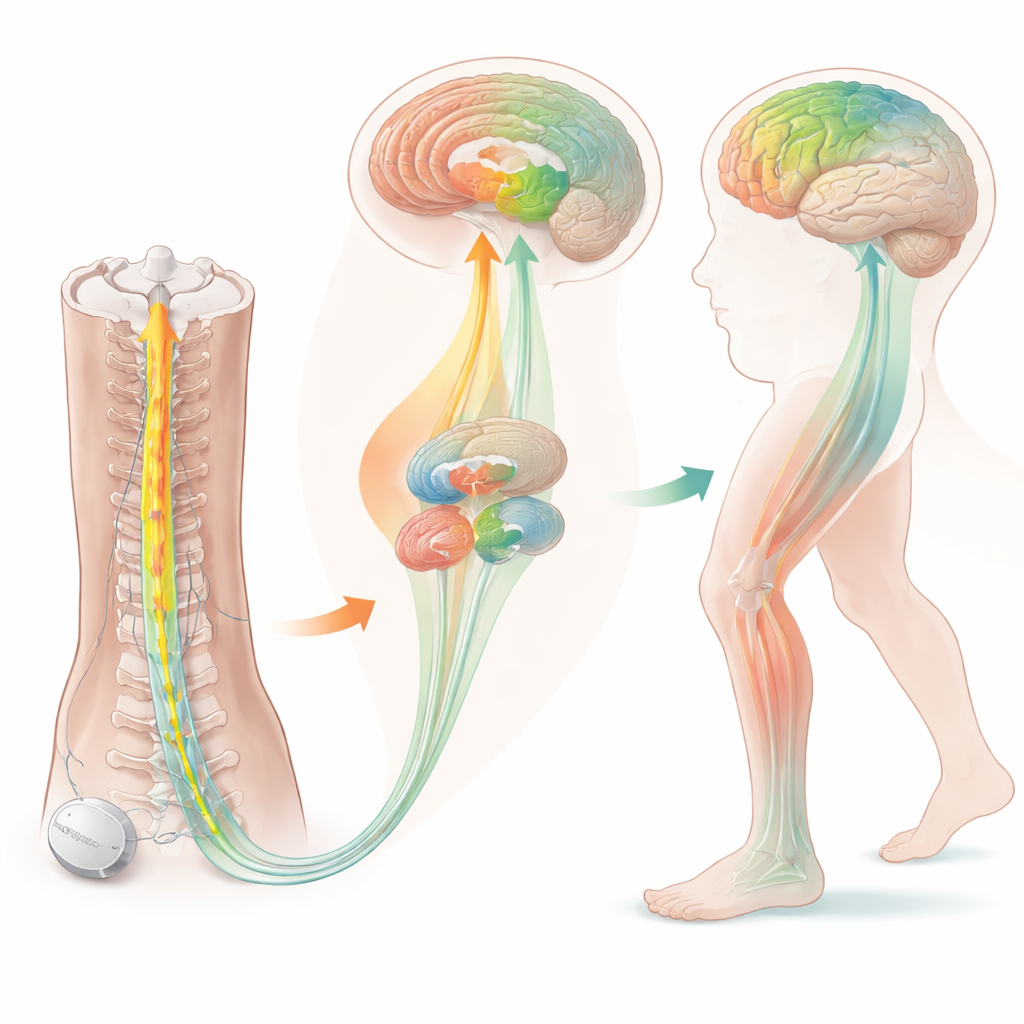
La sécurité d’abord, les signaux ensuite
L’essai a montré que ce type de stimulation médullaire était globalement sûr et acceptable. La plupart des complications étaient liées à la chirurgie elle‑même, comme des douleurs temporaires, un gonflement ou la nécessité de repositionner une électrode, et ces problèmes ont été traités sans séquelles durables. Fait important, le critère clinique principal de l’étude — un score global des troubles de l’équilibre et de la marche — ne s’est pas amélioré de façon significative après six mois de stimulation en rafales par rapport au groupe factice. Toutefois, en regardant de plus près, les chercheurs ont trouvé des signes encourageants : la raideur et la lenteur des jambes se sont améliorées pendant la stimulation, et un score détaillé « bas du corps et marche » a diminué au fil du temps, surtout après une année complète de traitement. Comparés à un groupe similaire tiré d’une large base de données sur la maladie de Parkinson, les patients sans stimulation avaient tendance à se détériorer sur un an, tandis que ceux traités par stimulation restaient stables ou s’amélioraient légèrement.
Ce que les images cérébrales ont révélé
Les imageries cérébrales ont fourni un aperçu des mécanismes possibles de la stimulation. Avant le traitement, les personnes présentant des blocages de la marche montraient une activité inhabituelle dans des régions impliquées dans l’attention et le contrôle du mouvement, notamment la région frontale droite et un point nodal appelé l’insula antérieure. Après plusieurs mois de stimulation, l’utilisation du glucose dans le thalamus — une station de relais qui aide à coordonner le mouvement — a diminué, et les signaux issus de certains terminaisons cholinergiques (utilisant l’acétylcholine) dans les régions motrices et attentionnelles ont également baissé. Plutôt que d’indiquer une lésion, ces changements traduisent probablement une normalisation de circuits hyperactifs que le cerveau utilisait pour compenser les problèmes de marche. Ces modifications biologiques correspondaient à l’allègement progressif de la rigidité et de la lenteur des jambes observé dans les évaluations cliniques.
Pourquoi des essais plus grands et mieux conçus sont nécessaires
Pour le grand public, le bilan est mitigé mais porteur d’espoir. Ce petit essai soigneusement contrôlé a montré que la stimulation médullaire en rafales n’apporte pas de solution nette et rapide aux difficultés de marche dans la maladie de Parkinson, et ne peut donc pas encore être recommandée comme traitement éprouvé de la marche. Cependant, la thérapie est apparue sûre et, avec le temps, elle a semblé réduire la raideur et la lenteur des jambes, les images cérébrales pointant vers des modifications significatives des réseaux du mouvement. L’étude a aussi mis en lumière des leçons de conception importantes — qui inclure, quels scores sont les plus sensibles, quelle durée de traitement — qui guideront des essais plus larges et déterminants. Autrement dit, si la stimulation médullaire n’est pas encore une cure de la marche, elle pourrait à l’avenir faire partie d’un arsenal pour aider les personnes atteintes de Parkinson à rester debout plus longtemps et en sécurité.
Citation: Terkelsen, M.H., Hvingelby, V.S., Johnsen, E.L. et al. Spinal cord stimulation therapy for gait impairment in Parkinson’s disease: a double-blinded, randomised feasibility trial with an open extension. Nat Commun 17, 2168 (2026). https://doi.org/10.1038/s41467-026-68782-w
Mots-clés: Maladie de Parkinson, troubles de la marche, stimulation médullaire, réseaux cérébraux profonds, neuromodulation