Clear Sky Science · fr
Base structurelle et implications pathologiques du complexe ERAD central dimérique OS9-SEL1L-HRD1
Le service de nettoyage cellulaire sous la loupe
À l’intérieur de chacune de nos cellules, une usine active convertit les instructions génétiques en protéines fonctionnelles. Comme dans toute usine, des erreurs surviennent. Lorsque les protéines sont mal repliées, elles peuvent encombrer le système et contribuer à des maladies. Cette étude s’attache à l’une des principales machines de contrôle qualité de la cellule — le complexe SEL1L‑HRD1 — pour en révéler la structure 3D détaillée et montrer comment de petites altérations génétiques peuvent perturber ce mécanisme et conduire potentiellement à des pathologies humaines.
Un tapis roulant caché dans la cellule
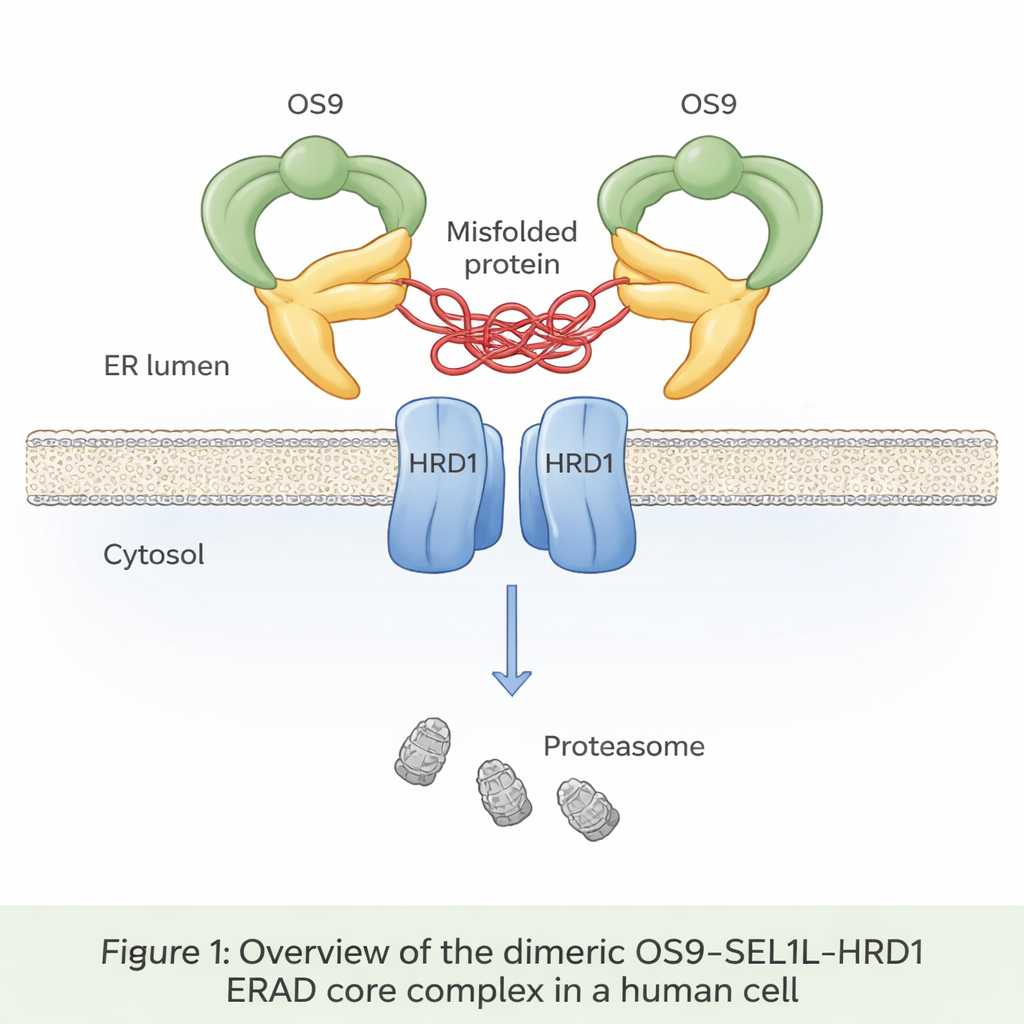
Jusqu’à un tiers de toutes les protéines récemment synthétisées pénètrent dans une compartimentation appelée réticulum endoplasmique (RE), où elles sont repliées et contrôlées. Les protéines mal repliées sont normalement détectées, extraites du RE puis détruites par un processus connu sous le nom de dégradation associée au RE (ER‑associated degradation, ERAD). Au cœur d’une voie ERAD majeure se trouve un trio de protéines : OS9, SEL1L et HRD1. OS9 fait office de détecteur pour les protéines défectueuses marquées par des sucres ; SEL1L sert d’échafaudage ; et HRD1 marque les protéines condamnées par l’ajout d’ubiquitine, signal les dirigeant vers les unités d’élimination cellulaires, les protéasomes. Jusqu’à présent cependant, personne n’avait observé en détail atomique comment ces trois éléments s’articulent dans les cellules humaines.
Révéler la forme de la machine centrale
Les auteurs ont utilisé la cryo‑microscopie électronique, une technique qui image des molécules vitrifiées à une résolution proche de l’atomique, pour visualiser le complexe OS9‑SEL1L‑HRD1 purifié de cellules humaines. Ils ont découvert qu’il forme un dimère — essentiellement deux copies identiques assemblées — plutôt que de rester en unités simples. Du côté de la lumière du RE (l’intérieur du RE), deux molécules d’OS9 et deux de SEL1L s’assemblent en une bague en forme de pince de crabe avec une ouverture centrale apparemment conçue pour saisir les protéines mal repliées. Dans la membrane elle‑même, deux molécules de HRD1 s’apparient pour former un canal partagé. Cet agencement place la « pince » directement au‑dessus de la porte HRD1, créant un chemin continu pour que les protéines défectueuses passent de la lumière du RE, à travers la membrane, vers la dégradation dans le cytosol.
Comment de minuscules changements rompent un grand système
Parce que des mutations de SEL1L et HRD1 ont été identifiées chez des patients présentant des troubles neurodéveloppementaux sévères et d’autres pathologies, l’équipe a cartographié plusieurs variants associés à des maladies sur leur structure et testé leur comportement dans des cellules. Deux mutations de SEL1L, G585D et S658P, se situent précisément aux points de contact avec OS9 et HRD1, respectivement. Dans des expériences cellulaires, G585D a presque annihilé la capacité de SEL1L à se lier à OS9, tandis que S658P a fortement affaibli son interaction avec HRD1 ; la combinaison des deux mutations a essentiellement rompu le complexe central, tout en laissant d’autres partenaires intacts. En conséquence, les cellules ont eu du mal à marquer et à éliminer un précurseur hormonal mal replié, permettant à des protéines défectueuses de persister.
Une mutation pathogène dans le canal membranaire
La structure montre également que le segment transmembranaire 3 de HRD1 est l’interface clé où deux molécules de HRD1 se rencontrent pour former le canal. Les chercheurs ont introduit des « poignées » cystéine à des positions spécifiques et ont utilisé un réticulant chimique pour confirmer que ces régions se rapprochent dans des cellules vivantes, prouvant que HRD1 dimérise bien in vivo. Lorsqu’ils ont perturbé un résidu hautement conservé (T93) à cette interface, le dimère s’est dissocié et l’activité ERAD s’est effondrée, même si le complexe continuait à s’assembler avec OS9 et SEL1L. Ils ont ensuite examiné un variant récemment découvert chez un patient, HRD1 A91D, identifié chez un enfant présentant des problèmes cardiaques et pulmonaires. Ce changement, également situé dans l’interface du dimère, a réduit d’environ moitié la dimérisation de HRD1 et gravement compromis l’élimination des protéines mal repliées, sans perturber l’interaction globale avec les partenaires.
Une nouvelle vision du contrôle qualité des protéines et des maladies
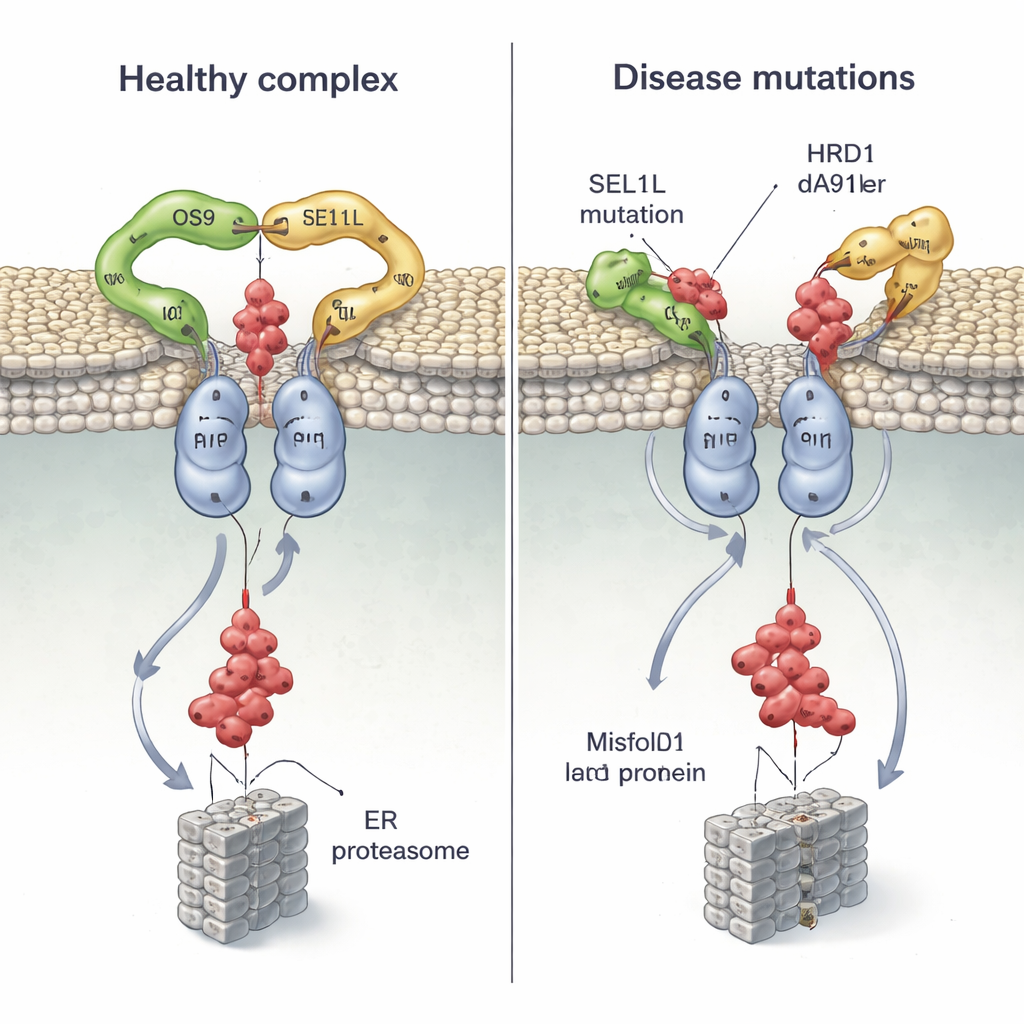
En combinant biologie structurale et essais cellulaires, ce travail montre que le complexe OS9‑SEL1L‑HRD1 fonctionne comme une machine dimérique appariée : un attrapeur en forme de pince relié à un canal partagé qui achemine les protéines défectueuses hors du RE. Les mutations qui relâchent la prise de la pince ou déstabilisent la paire HRD1 ne se contentent pas d’affiner l’efficacité — elles peuvent littéralement gripper le système, permettant l’accumulation de protéines endommagées et contribuant ainsi aux maladies humaines. Pour les non‑spécialistes, le message clé est que même des changements d’une seule lettre dans notre ADN peuvent déformer subtilement la forme de machines cellulaires essentielles, avec des conséquences majeures pour le développement cérébral, l’immunité et le fonctionnement des organes.
Citation: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Mots-clés: contrôle qualité des protéines, réticulum endoplasmique, ERAD, complexe SEL1L-HRD1, mauvais reploiement des protéines