Clear Sky Science · fr
Réaction stéréosélective de translocation du cyano activée par catalyse photoenzymatique
Déplacer de petites pièces pour un grand impact
Les chimistes cherchent souvent à modifier une molécule comme un ingénieur repositionnerait un engrenage dans une machine : déplacer une petite pièce sans tout reconstruire. Cet article montre comment des scientifiques peuvent faire glisser en douceur un groupe cyano, une petite mais puissante poignée chimique, d’un point à un autre d’une molécule en utilisant la lumière et des enzymes spécialisées. Le résultat est une manière plus précise et durable de construire les types de molécules employés en médecine et dans les matériaux avancés.
Pourquoi déplacer un petit groupe compte
Le comportement d’une molécule organique est largement dicté par ses groupes fonctionnels : ces petits ensembles d’atomes qui agissent comme des interrupteurs de contrôle. Déplacer un tel groupe même sur une courte distance le long d’une chaîne carbonée peut changer radicalement la façon dont la molécule se comporte dans l’organisme ou dans un matériau. Les chimistes savent comment provoquer ces migrations, notamment par des réactions radicalaires, mais ils peinent généralement à contrôler la « main » du produit. Comme la main gauche et la main droite, de nombreuses molécules existent sous formes images miroir, et souvent une seule de ces formes est utile ou sûre. Jusqu’à présent, obtenir la main désirée lors de ces réactions de déplacement de groupe a été très difficile.
Exploiter les enzymes et la lumière ensemble
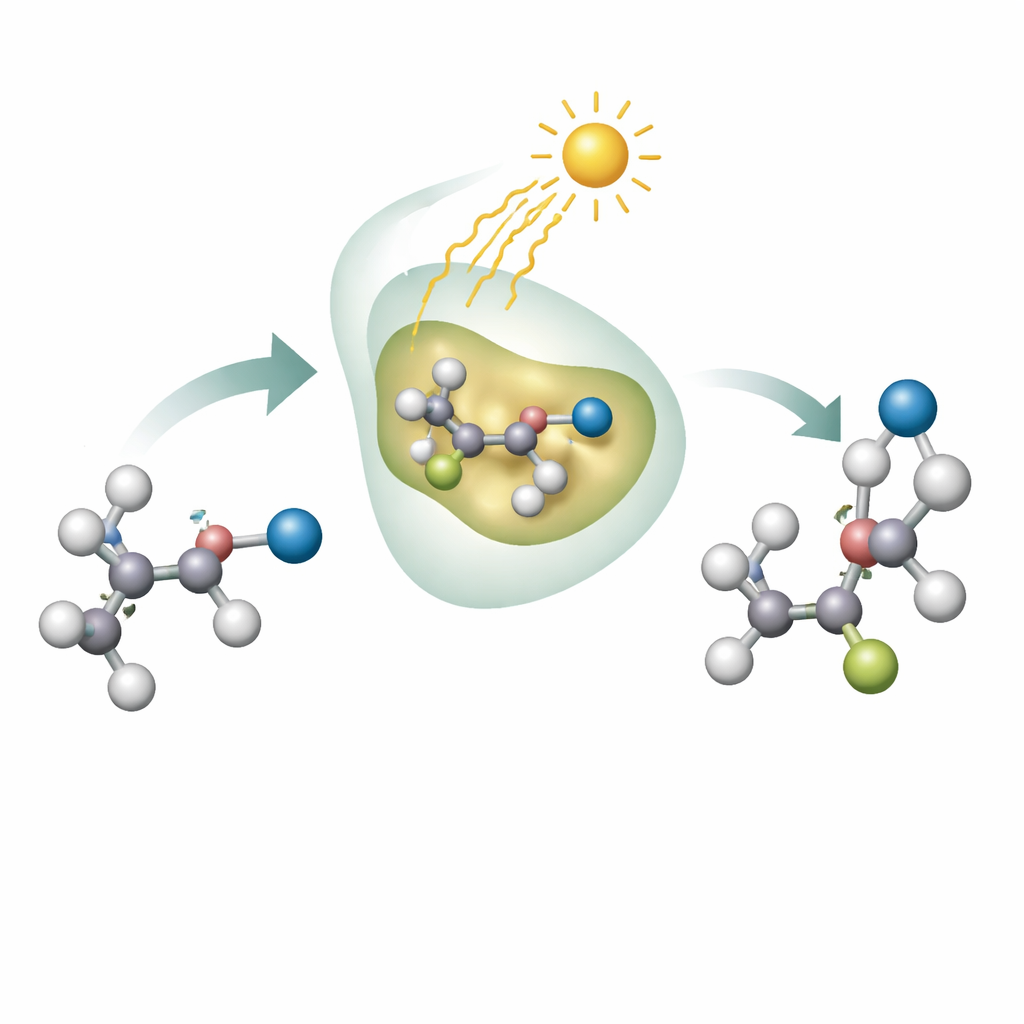
Les auteurs combinent les atouts des enzymes et de la lumière pour résoudre ce problème. Ils se concentrent sur le déplacement d’un groupe cyano (l’unité CN) le long d’une chaîne carbonée dans des molécules appelées nitriles alkyles, qui sont des blocs de construction importants pouvant être transformés en de nombreuses autres fonctions utiles. L’équipe utilise des enzymes dépendantes du flavine, une classe courante de protéines qui gèrent naturellement la chimie rédox dans les cellules. Lorsque la cofacteur flavine à l’intérieur de ces enzymes absorbe la lumière bleue, il atteint un état excité suffisamment réactif pour arracher un atome d’iode d’une molécule de départ, créant un radical hautement réactif. Dans le creux ajusté de l’enzyme, ce radical atteint le groupe cyano, déclenche une réarrangement qui le déplace, puis est soigneusement « éteint » par transfert d’un atome d’hydrogène depuis la flavine.
Produire une seule image miroir sur demande
Une réalisation clé de ce travail est que les enzymes ne se contentent pas de déplacer le groupe cyano : elles le font avec un excellent contrôle de la main. En criblant des enzymes naturelles puis en les affinant, les chercheurs identifient des systèmes qui donnent une image miroir du produit avec une très grande pureté, et d’autres qui favorisent l’image opposée. Ils montrent qu’un large éventail de molécules de départ, avec différentes nappes aromatiques et chaînes latérales, peut subir ce déplacement cyano induit par la lumière tout en conservant une forte préférence pour une seule main. L’ajustement électronique des matériaux de départ — l’ajout de groupes donneurs ou attracteurs d’électrons — influence en outre la propreté de la formation de la main préférée, révélant la délicatesse de l’équilibre réactif sous-jacent.
Observer la machine moléculaire de l’intérieur
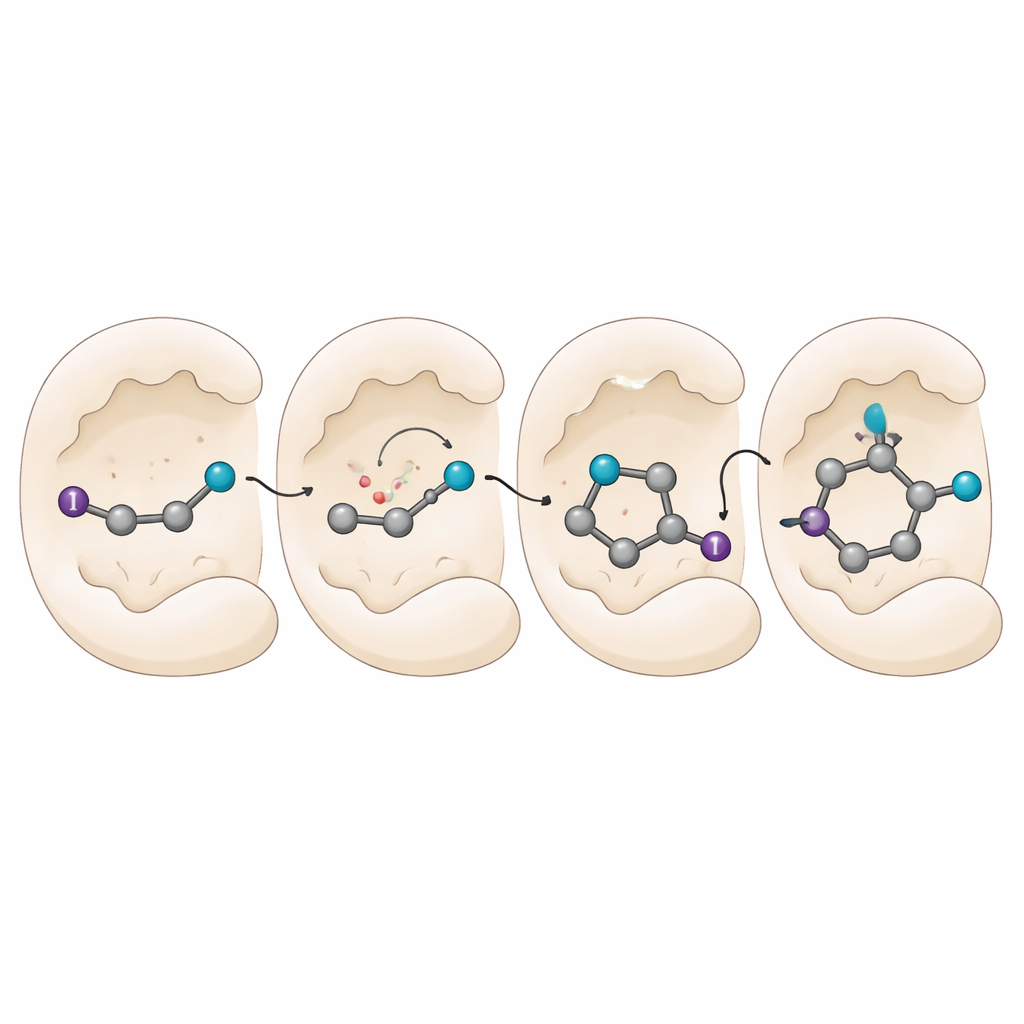
Pour comprendre comment les enzymes imposent un contrôle aussi précis, l’équipe réalise des expériences mécanistiques et des simulations informatiques. Des tests de piégeage de radicaux confirment que le processus passe bien par des intermédiaires radicalaires, mais une grande partie de la chimie est protégée à l’intérieur de l’enzyme, où les pièges externes peinent à interférer. Des mesures optiques révèlent que l’enzyme et le substrat forment un complexe particulier absorbant la lumière qui aide à initier la réaction. Les simulations du complexe enzyme–radical montrent que le groupe cyano est ancré par des acides aminés spécifiques, tandis que le reste de la molécule peut tourner en des conformations favorisées. Des interactions d’empilement subtiles entre l’anneau aromatique du substrat et certains acides aminés basculent l’équilibre vers une face du radical au moment de la livraison finale de l’atome d’hydrogène, verrouillant ainsi l’image miroir produite.
Un nouvel outil pour construire de meilleures molécules
En fin de compte, cette étude introduit une nouvelle manière de réarranger des molécules avec une finesse remarquable. En utilisant des enzymes photoactivées pour guider un déplacement cyano basé sur des radicaux, les auteurs montrent qu’il est possible de déplacer un groupe fonctionnel tout en décidant exactement quelle forme miroir le produit prendra. Pour la découverte de médicaments et la science des matériaux, cela offre une voie plus flexible et plus verte vers des structures moléculaires finement réglées, élargissant la boîte à outils dont disposent les chimistes pour concevoir des médicaments plus sûrs et des matériaux plus intelligents.
Citation: Duan, X., Xu, J., Bai, R. et al. Stereoselective cyano translocation reaction enabled by photoenzymatic catalysis. Nat Commun 17, 2133 (2026). https://doi.org/10.1038/s41467-026-68776-8
Mots-clés: catalyse photoenzymatique, migration de groupe fonctionnel, translocation du cyano, contrôle stéréochimique enzymatique, nitriles alkyles