Clear Sky Science · fr
Profilage des délétions d’exons au niveau unicellulaire révèle des événements d’épissage qui façonnent l’expression génique et la dynamique des états cellulaires
Comment de petites modifications de l’ARN peuvent changer le comportement cellulaire
Nos cellules lisent et épissent constamment les instructions ARN pour décider quelles protéines produire et comment répondre au stress, croître ou se diviser. Cette étude montre que modifier des fragments très petits de ces messages ARN—des segments uniques appelés exons—peut remodeler fortement l’activité génique et même modifier la façon dont les cellules traversent le cycle cellulaire. Le travail présente un outil puissant qui permet aux scientifiques d’examiner simultanément de nombreux de ces petits choix d’ARN, cellule par cellule, ouvrant de nouvelles voies pour comprendre les maladies et découvrir des cibles thérapeutiques.
Couper des mots sélectionnés dans le script génétique
Les gènes sont écrits sous forme de longues séquences d’ADN, mais les cellules ne les lisent pas de bout en bout. Elles découpent et recollent plutôt des blocs plus petits, appelés exons, pour construire un message ARN. En choisissant quels exons conserver, les cellules peuvent produire plusieurs versions protéiques à partir d’un seul gène, un peu comme réaliser différents montages d’un film à partir des mêmes rushes. De nombreuses maladies, dont le cancer et l’autisme, sont liées à des erreurs de ce processus, pourtant pour la plupart des choix d’exons nous ignorons encore leur fonction réelle. Les auteurs ont cherché à combler cette lacune en développant un système à grande échelle capable de supprimer des exons spécifiques de nombreux gènes puis d’observer, dans des milliers de cellules individuelles simultanément, comment ces modifications affectent le réseau interne de la cellule.
Un « moteur de recherche » unicellulaire pour la fonction des exons
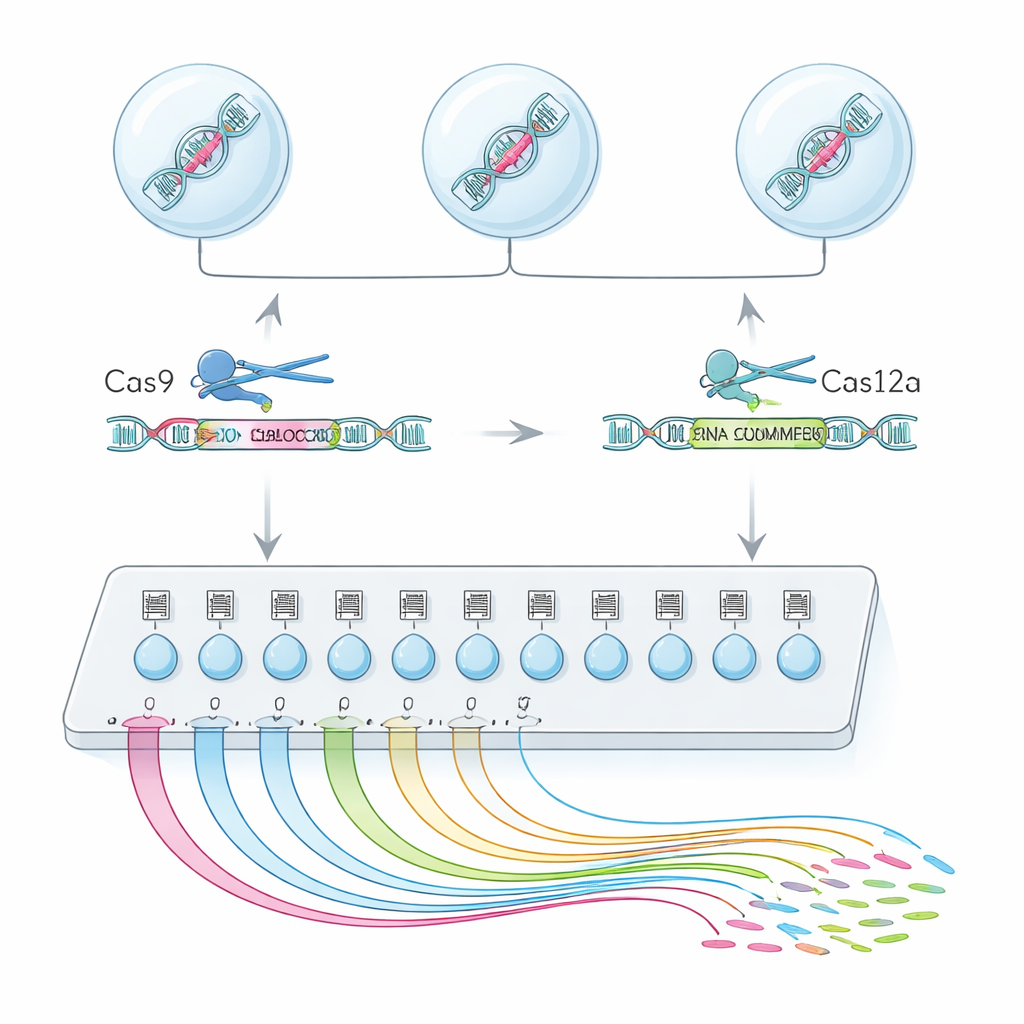
Pour cela, l’équipe a combiné deux enzymes d’édition du génome, Cas9 et Cas12a, en une plateforme hybride appelée CHyMErA. Chaque enzyme est guidée vers l’ADN par de courts ARN « adresses ». En dirigeant les deux enzymes pour couper juste avant et juste après un exon choisi, elles peuvent supprimer proprement ce segment tout en laissant le reste du gène intact. La nouvelle méthode, scCHyMErA-Seq, relie cette découpe précise au séquençage ARN unicellulaire. L’ARN de chaque cellule est capturé dans une goutte avec un code-barres et les ARN guides qui spécifient quel exon a été supprimé. Le séquençage révèle alors, pour des dizaines de milliers de cellules, à la fois l’édition reçue par chaque cellule et le profil détaillé des gènes activés ou réprimés.
Concevoir l’outil pour voir les deux lames des ciseaux
Un défi clé était de détecter de façon fiable les guides Cas12a aux côtés des guides Cas9 dans la même expérience unicellulaire. Les premières conceptions échouaient soit à capturer les ARN guides Cas12a, soit diminuaient l’efficacité d’édition. Les chercheurs ont résolu cela en redesignant soigneusement la séquence de la poignée de Cas12a pour supprimer des régions qui arrêtaient prématurément la transcription, en ajoutant un petit élément ARN stabilisant et une étape d’amplification ciblée. Ces ajustements ont augmenté la capacité à détecter les deux guides dans environ 90 % des cellules, tout en préservant une forte efficacité de suppression d’exons. Avec ce protocole optimisé, les auteurs ont testé 224 exons alternatifs répartis dans 161 gènes humains, en profilant plus de 200 000 cellules unicellulaires de haute qualité.
Découvrir des exons qui contrôlent des programmes géniques et le cycle cellulaire
Lorsque l’équipe a comparé l’activité génique des cellules éditées à celle des témoins, près de la moitié des exons testés ont provoqué des changements substantiels dans des centaines d’autres gènes. Les exons provenant de gènes impliqués dans le traitement de l’ARN et la transcription avaient tendance à se regrouper, produisant des empreintes d’expression similaires et révélant des voies biologiques partagées, comme la biogenèse des ribosomes ou la dégradation de l’ARN. Dans certains cas, la suppression d’un seul exon avait un effet clair et interprétable : enlever un exon des gènes TAF5 ou LSM11 perturbait le traitement correct des ARN histones, entraînant une accumulation inhabituelle de messages histones polyadénylés. L’ensemble de données a également mis en évidence des dizaines d’exons dont la perte changeait la répartition des cellules dans les différentes phases du cycle cellulaire, liant des événements d’épissage spécifiques aux décisions de la cellule concernant quand elle fait une pause, copie son ADN ou se prépare à se diviser.
Une étude de cas : un exon qui module un régulateur maître
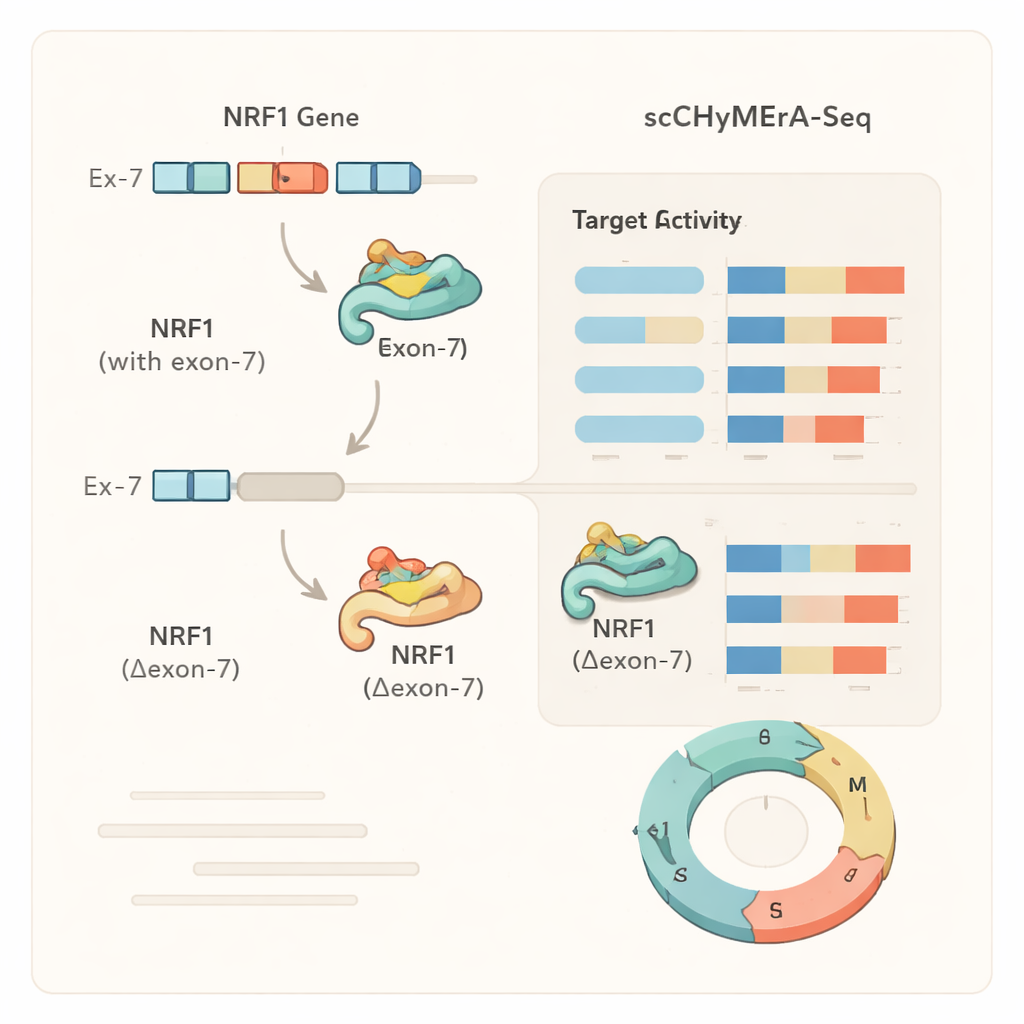
Un exemple marquant était l’exon 7 du gène NRF1, un facteur de transcription qui contrôle de nombreux gènes impliqués dans la production d’énergie cellulaire. Cet exon recouvre en partie la région de liaison à l’ADN de NRF1. Lorsque l’exon 7 a été supprimé, des centaines de gènes régulés par NRF1 ont modifié leur activité, et des expériences détaillées ont montré que la protéine NRF1 raccourcie se liant beaucoup moins efficacement à ses promoteurs cibles dans le génome. Les auteurs ont aussi identifié un régulateur d’épissage spécifique, SRSF3, qui favorise l’inclusion de cet exon, révélant une chaîne d’action depuis un facteur d’épissage, via le choix d’un exon dans NRF1, vers des changements étendus des programmes géniques et du métabolisme cellulaire. Des analyses similaires ont montré que, pour certains gènes, la suppression d’un exon imitait une suppression complète du gène, tandis que pour d’autres elle produisait un changement plus fin et dépendant de l’état, suggérant que les exons alternatifs peuvent moduler subtilement le comportement des protéines plutôt que de simplement les activer ou les désactiver.
Pourquoi cela compte pour la santé et les thérapies futures
Pour un non-spécialiste, le message clé est que les cellules s’appuient sur l’inclusion ou l’omission de segments ARN très courts pour ajuster le fonctionnement des gènes, et que ces réglages fins peuvent modifier des traits majeurs comme la division cellulaire ou la réponse au stress. La plateforme scCHyMErA-Seq agit comme un test en laboratoire à haut débit pour ces choix d’épissage, identifiant quels exons ont un impact fonctionnel réel et comment ils reconfigurent les états cellulaires. Étant donné que de nombreux cancers et troubles neurologiques impliquent des exons mal épissés ou des facteurs de transcription altérés, cette approche pourrait aider à prioriser les variants d’épissage à cibler par de futurs médicaments ou thérapies ARN, et fournir une feuille de route pour comprendre comment de petites modifications du script génétique entraînent de grands changements dans le comportement cellulaire.
Citation: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Mots-clés: épissage alternatif, séquençage ARN unicellulaire, dépistage CRISPR, régulation des gènes, cycle cellulaire