Clear Sky Science · fr
Nanozyme mimétique de la granzyme B pour des applications anticancéreuses ciblées par nanovésicules
Réinventer les tueurs du corps contre le cancer
Notre système immunitaire comprend des cellules spécialisées capables de traquer et d’éliminer les cancers, mais dans de nombreux tumeurs solides elles peinent à pénétrer, s’épuisent rapidement ou attaquent de mauvaises cibles. Cette étude décrit un système entièrement artificiel à l’échelle nanométrique qui imite l’une des armes les plus puissantes du système immunitaire et la délivre directement à l’intérieur des cellules tumorales. Ce travail est important car il ouvre la voie à des traitements contre le cancer qui se comportent comme des cellules immunitaires vivantes, tout en étant fabriqués à partir de matériaux stables et contrôlables plutôt que de cellules humaines fragiles.
Transformer un assassin naturel en plan
Les cellules T cytotoxiques, un type de globule blanc, tuent les cellules dangereuses en utilisant une enzyme appelée granzyme B. Une fois la cible reconnue, elles perforent légèrement sa membrane et injectent la granzyme B, qui active des programmes d’autodestruction à l’intérieur de la cellule. Cette stratégie est à la base de thérapies modernes comme les cellules CAR-T, qui peuvent guérir certains cancers du sang. Cependant, dans les tumeurs solides, les CAR-T échouent souvent parce qu’elles ne peuvent atteindre toutes les régions tumorales, s’épuisent ou atteignent par erreur des tissus sains. Les auteurs se sont demandé s’il était possible de construire un dispositif non vivant, à l’échelle nanométrique, reproduisant la fonction clé de la granzyme B — déclencher la machinerie d’autodestruction cellulaire — sans dépendre de cellules T vivantes.
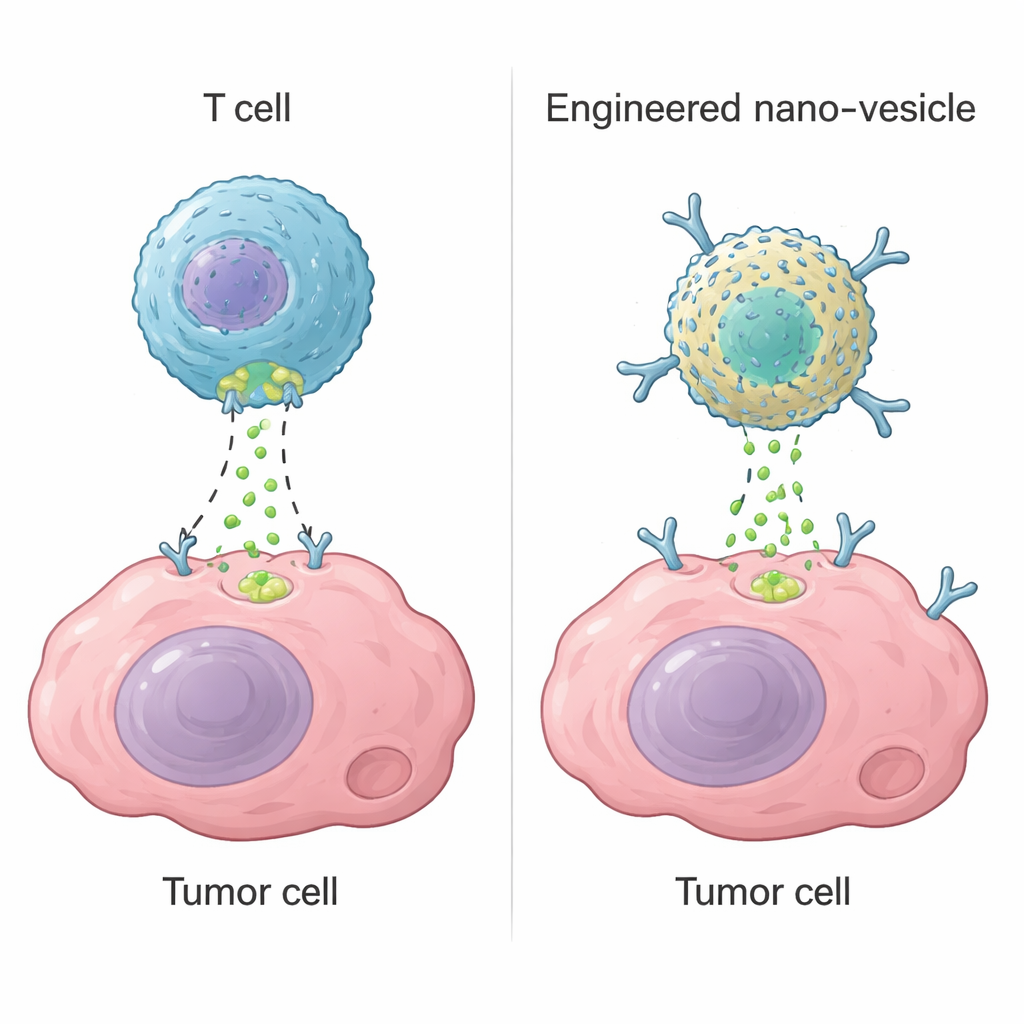
Concevoir une enzyme artificielle minuscule
L’équipe est partie de la ferritine, une protéine naturelle qui forme des nanocages creux et se produit facilement en grande quantité. En liant des ions palladium à la ferritine humaine, ils ont créé un « nanozyme » ayant un comportement apparenté à une enzyme. Des études structurelles soignées ont révélé que deux atomes de palladium s’inséraient dans un site précis à la surface de la protéine, maintenus en place par des acides aminés contenant du soufre et de l’azote ainsi que des molécules d’eau. Ce centre métallique binucléaire agit comme un site de coupure artificiel qui reconnaît la même courte séquence utilisée par la granzyme B sur une cible cruciale connue sous le nom de caspase-3. En tests in vitro, le nanozyme a efficacement clivé la caspase-3 au bon endroit, l’activant, tout en ignorant des protéines étroitement apparentées. L’enzyme artificielle était légèrement moins efficace que la granzyme B naturelle mais nettement plus stable sur une large gamme de températures et d’acidité.
Faire entrer le nanozyme dans les cellules tumorales
Les enzymes comme la granzyme B ne fonctionnent que si elles atteignent l’intérieur des cellules tumorales. Pour cela, les chercheurs ont emballé leur nanozyme palladium–ferritine à l’intérieur de nanovésicules lipidiques — de petites bulles souples constituées de molécules proches des graisses. Ils ont ensuite recouvert ces vésicules de fragments d’anticorps reconnaissant HER2, une protéine souvent surproduite par les cellules du sein et de la vessie cancéreuses. Lorsque ces vésicules déguisées rencontrent des cellules riches en HER2, elles se lient fortement et fusionnent avec la membrane cellulaire, permettant au cargo nanozymatique de glisser directement dans le cytoplasme au lieu d’être piégé et digéré dans les compartiments de recyclage cellulaires. La microscopie montrait les vésicules en surface cellulaire tandis que le nanozyme diffusait vers l’intérieur, préparant le terrain pour une autodéstruction contrôlée depuis l’intérieur.
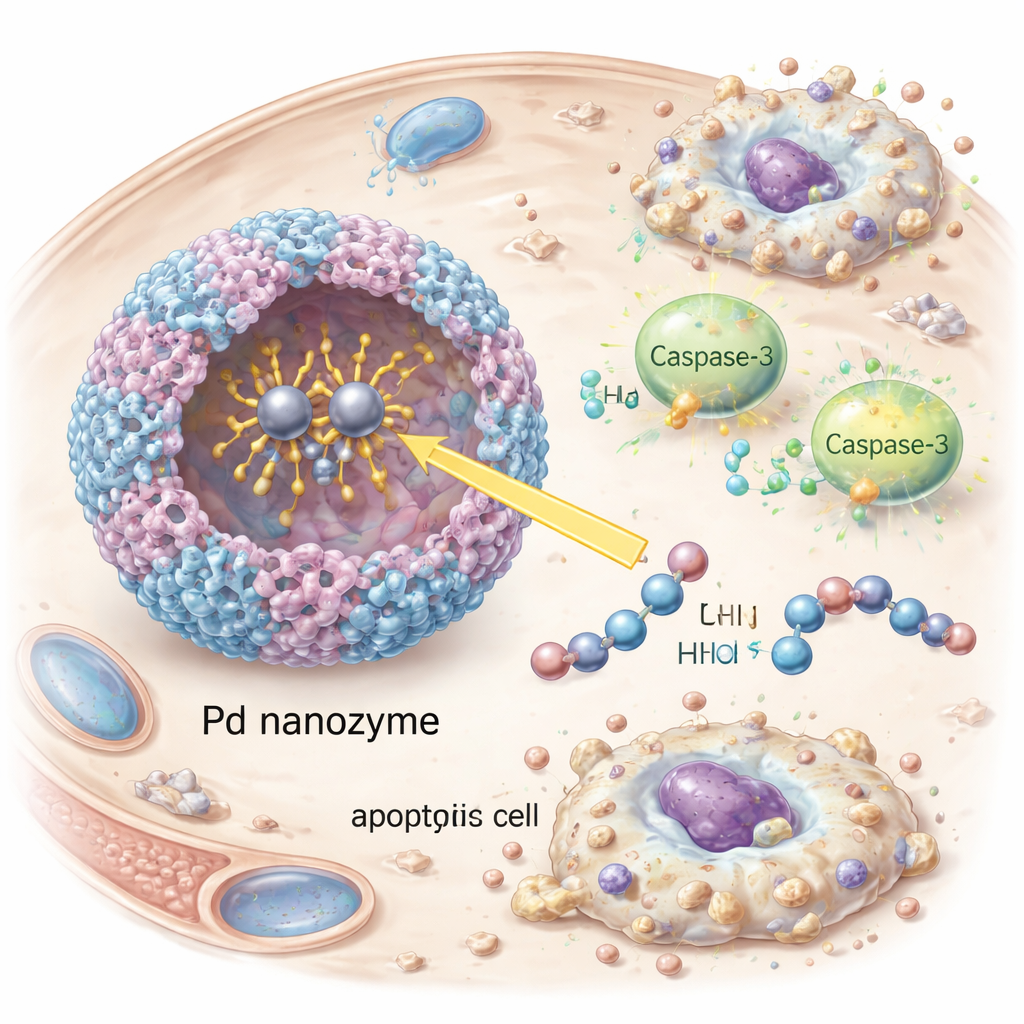
Déclencher précisément le suicide des cellules cancéreuses
Une fois à l’intérieur des cellules cancéreuses, le nanozyme a activé la caspase-3, un exécuteur central de la mort cellulaire programmée. Les chercheurs ont observé l’apparition de la caspase-3 activée et de sa cible en aval PARP, ainsi que des signes nets d’apoptose — rétrécissement et fragmentation des cellules — dans des lignées tumorales HER2-positives en culture. Inhiber la caspase-3 par interférence ARN a fortement réduit la mortalité cellulaire, confirmant que l’effet dépendait de cette voie plutôt que de dommages non spécifiques. Chez des souris porteuses de tumeurs HER2-positives, les vésicules décorées d’anticorps ont circulé plus longtemps dans le sang, se sont accumulées plus fortement dans les tumeurs et ont ralenti la croissance tumorale plus efficacement que des vésicules dépourvues soit des anticorps ciblants soit du cargo nanozymatique. Fait important, les animaux traités n’ont montré ni perte de poids évidente, ni anomalies sanguines, ni lésions tissulaires dans les principaux organes, suggérant un profil de sécurité favorable dans ces premiers tests.
Ce que cela pourrait signifier pour les soins futurs du cancer
Pour un public non spécialiste, le message central est que les chercheurs ont construit un petit dispositif non vivant qui se comporte comme une pièce clé de la machinerie immunitaire anti-cancer. Plutôt que d’ingénier des cellules T vivantes, ils ont conçu un nanoenzyme stable qui active le même interrupteur d’autodestruction à l’intérieur des cellules tumorales et l’ont enveloppé dans une coque de livraison intelligente ciblant des cancers spécifiques. Bien qu’il reste beaucoup de travail avant une utilisation humaine, cette approche offre une plateforme flexible : en principe, le revêtement anticorps pourrait être remplacé pour viser d’autres marqueurs tumoraux, et l’enzyme artificielle pourrait être encore optimisée. L’étude démontre une voie prometteuse vers une immunothérapie sans cellules, où des nanomatériaux soigneusement conçus, plutôt que des cellules immunitaires vivantes, sont utilisés pour traquer et détruire les tumeurs solides.
Citation: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Mots-clés: nanomédecine du cancer, immunothérapie, granzyme B, nanozyme, tumeurs HER2-positives