Clear Sky Science · fr
Chimie bioorthogonale activée par les espèces réactives de l’oxygène dans les systèmes vivants rendue possible par des dihydrotétrazines protégées par un boronate
Transformer le stress cellulaire en un interrupteur précis
De nombreuses maladies, du cancer aux troubles cardiaques, se caractérisent par des cellules soumises à un stress oxydatif, produisant des niveaux élevés d’espèces réactives de l’oxygène telles que le peroxyde d’hydrogène. Cette étude montre comment des chimistes peuvent exploiter ce stress comme un interrupteur intégré pour n’activer des thérapies puissantes que là où elles sont nécessaires. En concevant des composants médicamenteux qui ne réagissent que dans ces environnements stressés, les chercheurs visent à éliminer les cellules tumorales ou à détruire des protéines nuisibles tout en épargnant les tissus sains.
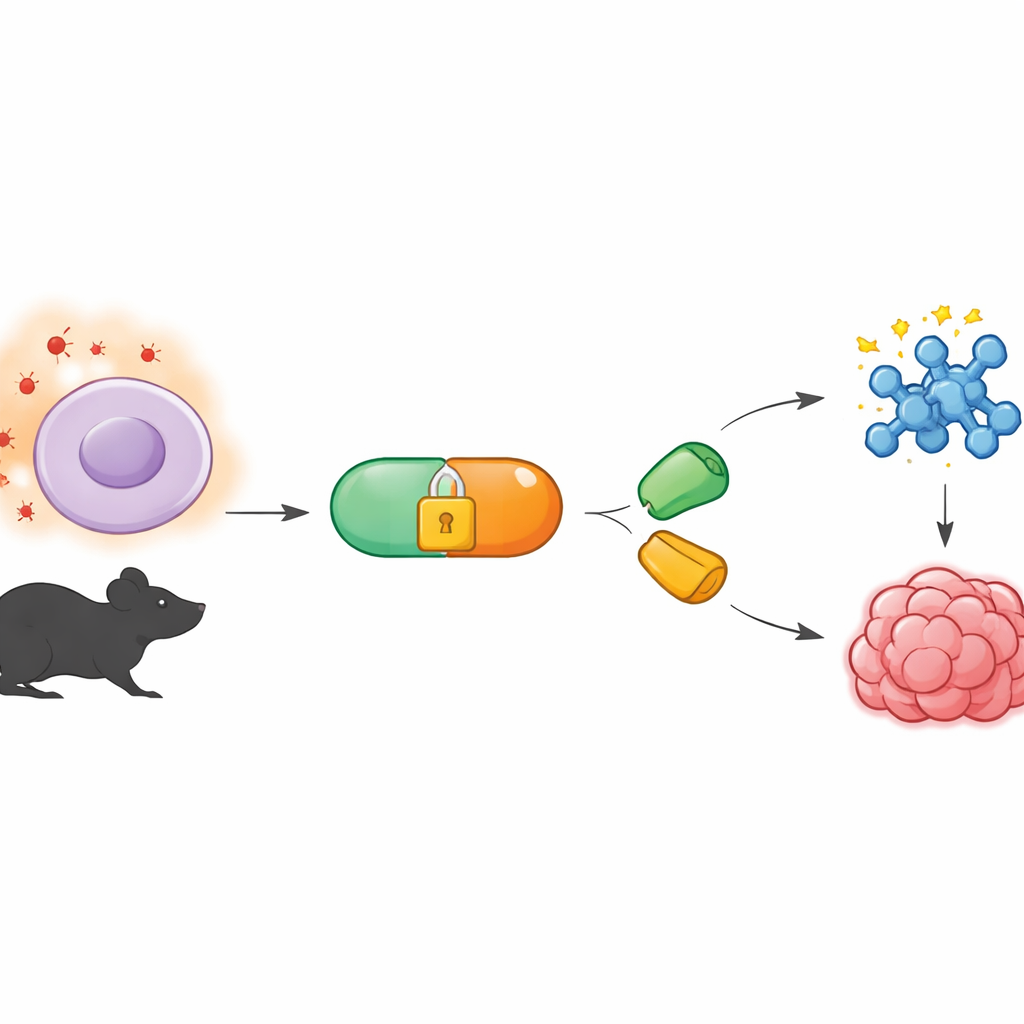
Un outil chimique qui agit discrètement en arrière‑plan
Le travail s’appuie sur un domaine appelé chimie bioorthogonale, qui développe des réactions pouvant se dérouler à l’intérieur d’organismes vivants sans perturber la biologie normale. Une version répandue utilise des paires particulières de molécules qui s’assemblent comme des pièces de puzzle, même dans l’intérieur encombré d’une cellule. L’un des partenaires, appelé tétrazine, réagit très rapidement avec un partenaire complémentaire en anneau, nommé diénophile. Jusqu’à présent, beaucoup de ces réactions étaient contrôlées par exposition à la lumière ou par ajout d’enzymes. Les auteurs ont voulu à la place un système qui écoute les signaux chimiques du corps — en particulier les niveaux anormalement élevés d’espèces réactives de l’oxygène présents dans les tumeurs et d’autres tissus malades.
Conception d’un déclencheur chimique sensible aux ROS
Pour cela, l’équipe a créé des précurseurs de tétrazine qu’ils appellent BTz, chimiquement « enfermés » pour rester inertes dans les tissus normaux. La cage est construite à partir d’un groupe boronate lié à une forme réduite de tétrazine. Lorsque le peroxyde d’hydrogène est rare, le BTz est stable en milieu aqueux et en culture cellulaire pendant de nombreuses heures. Mais lorsque le peroxyde d’hydrogène est abondant — à des niveaux similaires à ceux mesurés dans les tumeurs — le groupe boronate est oxydé et se décompose par une séquence d’autodestruction, révélant la tétrazine active. Dans des expériences en éprouvette, l’augmentation progressive des concentrations de peroxyde d’hydrogène conduisait à une augmentation correspondante de la quantité de tétrazine active générée, confirmant que la réaction est à la fois sélective et fortement dépendante de la dose.
Utiliser le stress cellulaire pour détruire une protéine impliquée dans le cancer
Les chercheurs ont d’abord utilisé leur interrupteur pour contrôler une stratégie médicamenteuse moderne appelée dégradation ciblée des protéines. Ils ont attaché BTz à la thalidomide, une petite molécule capable de recruter un complexe enzymatique responsable du marquage des protéines pour élimination. Dans les cellules cancéreuses, ce BTz–thalidomide restait inerte jusqu’à ce que les niveaux de peroxyde d’hydrogène augmentent, moment où la cage s’ouvrait pour former une tétrazine active. Cette tétrazine s’assemblait alors rapidement avec un partenaire correspondant lié à un médicament visant BRD4, constituant une chimère plus grande qui dirige la protéine liée au cancer BRD4 vers la machinerie d’élimination cellulaire. Dans des lignées cellulaires de cancer du poumon et du col de l’utérus, les niveaux de BRD4 chutaient fortement uniquement lorsque tous les éléments étaient présents et que le peroxyde d’hydrogène était disponible ; le blocage des espèces réactives de l’oxygène empêchait la dégradation, soulignant que le processus est réellement activé par le stress.
Libérer un médicament toxique uniquement là où il est nécessaire
Ensuite, l’équipe a transformé la même chimie en un système de délivrance précis pour la doxorubicine, une chimiothérapie puissante mais cardiotoxique. Ils ont lié la doxorubicine à un partenaire en anneau sous tension afin qu’elle soit verrouillée sous forme de prodrogue inactive. Lorsque cette prodrogue rencontrait le BTz dans un environnement riche en peroxyde d’hydrogène, la tétrazine nouvellement formée réagissait avec l’anneau selon un processus « click‑to‑release », assemblant les éléments et libérant la doxorubicine libre. Dans des cellules de cancer du côlon cultivées en plaque, ce système en deux étapes tuait les cellules presque aussi efficacement que le médicament libre, mais uniquement en présence de peroxyde d’hydrogène ; sans celui‑ci, les cellules restaient largement indemnes. Une prodrogue de doxorubicine plus simple et sensible au peroxyde d’hydrogène s’est montrée moins efficace et moins sélective dans ces essais, mettant en évidence l’avantage de séparer la détection et la libération en deux étapes coordonnées.
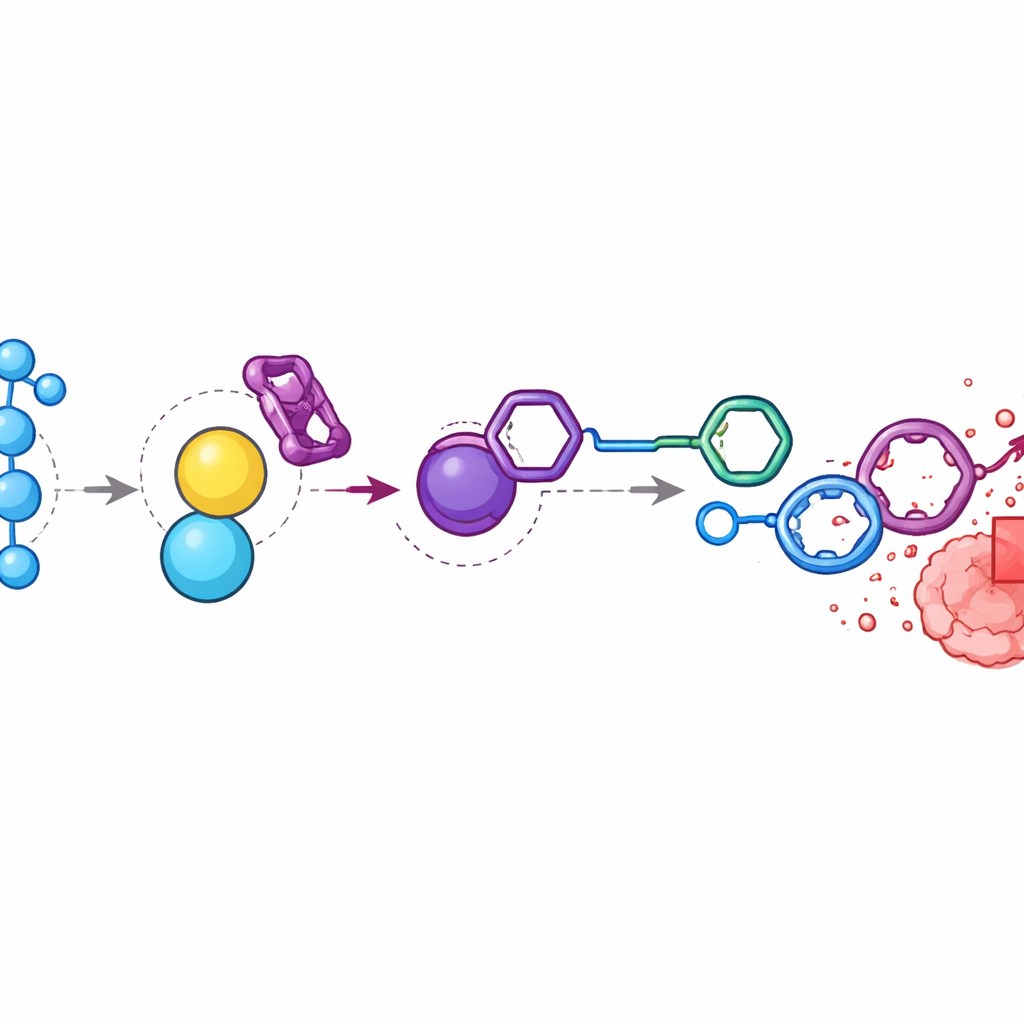
Concentrer la chimiothérapie à l’intérieur des tumeurs
Chez des souris porteuses de tumeurs du côlon, les chercheurs ont constaté que les niveaux de peroxyde d’hydrogène dans les tumeurs étaient presque neuf fois plus élevés que dans le muscle environnant. Ils ont injecté la prodrogue de doxorubicine et le BTz selon une séquence chronométrée de sorte que les deux s’accumulent près de la tumeur. L’analyse chimique a montré que les composants disparaissaient en grande partie du sang et des organes mais généraient des niveaux élevés de doxorubicine libre à l’intérieur des tumeurs. Comparés aux animaux traités par doxorubicine standard, ceux recevant le système activé présentaient une réduction tumorale similaire ou meilleure tout en maintenant un poids corporel stable et en évitant la toxicité sévère observée à des doses plus élevées. Lorsque l’équipe a interrompu le signal de peroxyde d’hydrogène en injectant de la catalase, une enzyme qui élimine le peroxyde d’hydrogène, la libération du médicament et l’accumulation sélective dans la tumeur ont été fortement réduites, confirmant que le stress oxydatif au site tumoral est le moteur clé.
Du signal de stress à la thérapie de précision
Ensemble, cette étude démontre une plateforme chimique polyvalente qui transforme une caractéristique des maladies — l’excès d’oxydant réactif — en un bouton de commande précis pour des réactions puissantes dans les systèmes vivants. En maintenant la poignée tétrazine réactive verrouillée jusqu’à sa rencontre avec le peroxyde d’hydrogène, l’approche permet aux chercheurs de construire des thérapies complexes à l’intérieur du corps uniquement là où elles sont nécessaires, qu’il s’agisse de démanteler une protéine favorisant le cancer ou de libérer un médicament toxique à l’intérieur d’une tumeur. Comme le stress oxydatif joue également un rôle dans le vieillissement, l’inflammation, le diabète et les troubles neurodégénératifs, des réactions sensibles au stress similaires pourraient finalement être adaptées à de nombreuses conditions où la précision et la sécurité sont primordiales.
Citation: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Mots-clés: chimie bioorthogonale, espèces réactives de l’oxygène, ligation de tétrazine, libération ciblée de médicaments, PROTAC