Clear Sky Science · fr
Analyse microfluidique électrochimique actionnée par membrane homotypique des vésicules extracellulaires pour un diagnostic précis du cancer
Transformer l’armure du cancer en outil diagnostique
Les membranes qui entourent les cellules cancéreuses sont parsemées de « drapeaux » moléculaires distinctifs. Cette étude montre comment des chercheurs peuvent détacher cette armure, l’étaler sur de petites puces d’or, puis l’utiliser pour capturer des particules révélatrices dans le sang. Le résultat est un test sanguin très sensible capable d’indiquer non seulement la présence d’un cancer du sein, mais aussi son sous-type — information cruciale pour choisir le traitement approprié.
Pourquoi le sous-type du cancer du sein importe
Le cancer du sein n’est pas une maladie unique. Les tumeurs se classent en sous-types tels que récepteur d’œstrogènes positif (ER+), HER2-positif et triple négatif, qui répondent différemment aux traitements hormonaux, aux thérapies ciblées ou à la chimiothérapie. Aujourd’hui, les médecins déterminent généralement le sous-type à partir d’une biopsie tissulaire prélevée sur la tumeur. Cette procédure est invasive, ne peut pas être répétée fréquemment et peut manquer des changements qui surviennent au cours de l’évolution de la maladie. Un test sanguin capable de suivre ces signatures de sous-type dans le temps permettrait aux cliniciens d’ajuster la thérapie plus tôt et plus précisément.
De minuscules messagers en suspension dans le sang
Les cellules cancéreuses libèrent en permanence des bulles nanoscale appelées vésicules extracellulaires (VE) dans la circulation sanguine. Les VE transportent protéines, lipides et matériel génétique qui ressemblent étroitement à ceux de leurs cellules d’origine, ce qui en fait des candidats attractifs pour des « biopsies liquides ». Mais il y a un défi : les VE issus de différents sous-types de cancer du sein peuvent paraître très semblables si l’on ne considère qu’une ou deux protéines. Les tests existants ciblent soit des marqueurs partagés — rendant la distinction des sous-types difficile — soit s’appuient sur des essais génétiques complexes, lents et parfois trompeurs. Les auteurs ont cherché à lire l’empreinte moléculaire plus complète à la surface des VE de manière simple et robuste.
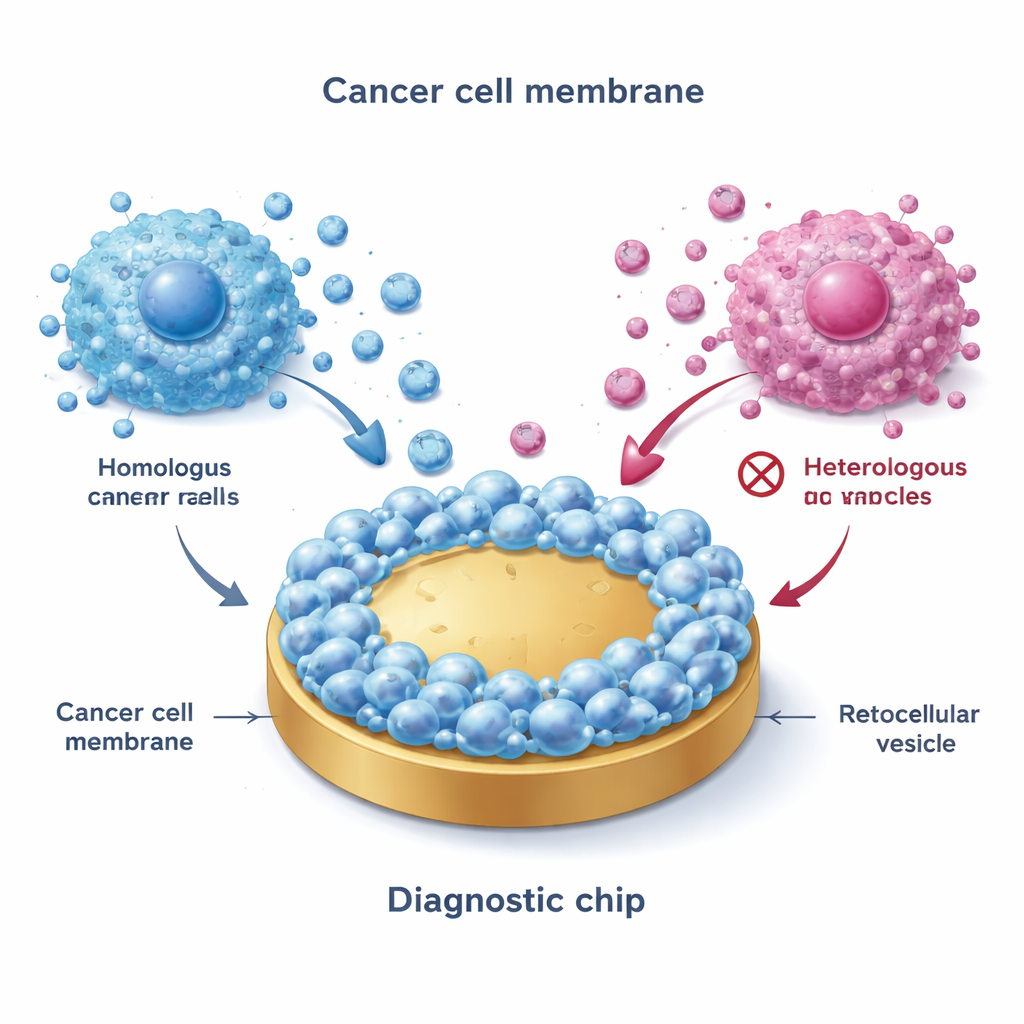
Construire un filet biomimétique
L’équipe a commencé par prélever des membranes de cellules cancéreuses du sein cultivées représentant les principaux sous-types : ER+ (comme MCF-7), HER2-positif et triple négatif. Par un processus de congélation–dégel, ils ont rompu les cellules, isolé les membranes externes, puis fusionné ces membranes sur des surfaces d’or plates. Cela a créé une « interface biomimétique » qui imite de près l’extérieur des cellules cancéreuses d’origine. Remarquablement, lorsque des VE étaient perfusées sur ces surfaces revêtues, seules les vésicules issues de sous-types correspondants ou proches adhéraient fortement — un phénomène appelé liaison homotypique. Des techniques d’imagerie avancées et des mesures électriques ont confirmé que les surfaces recouvertes de membrane étaient plus rugueuses, plus hydrophiles et beaucoup moins sujettes aux adhérences non spécifiques que l’or nu, les rendant adaptées à des mesures propres dans des fluides complexes comme le sang.
Convertir la capture de vésicules en signal électrique
Pour transformer la liaison en signal lisible, les chercheurs ont ciblé une protéine abondante sur la surface des VE, appelée CD47. Ils ont attaché des anticorps anti‑CD47 à des nanoparticules d’argent en utilisant un court pont d’ADN, créant de petites balises électroactives. Après que la surface recouverte de membrane ait capturé ses VE préférés, ces balises se fixaient sur le CD47 des vésicules liées. Exposées à une solution acide puis mesurées électrochimiquement, les particules d’argent produisaient un courant net et facilement quantifiable. L’intensité de ce signal augmentait de manière linéaire sur une large gamme de concentrations de VE, jusqu’à quelques centaines de vésicules par millilitre — bien plus sensible que des méthodes courantes comme les kits ELISA ou le suivi de nanoparticules. Chaque type de membrane cancéreuse produisait un signal fort uniquement avec ses VE correspondantes, même en présence de vésicules d’autres sous-types, de plaquettes ou de cellules non apparentées.
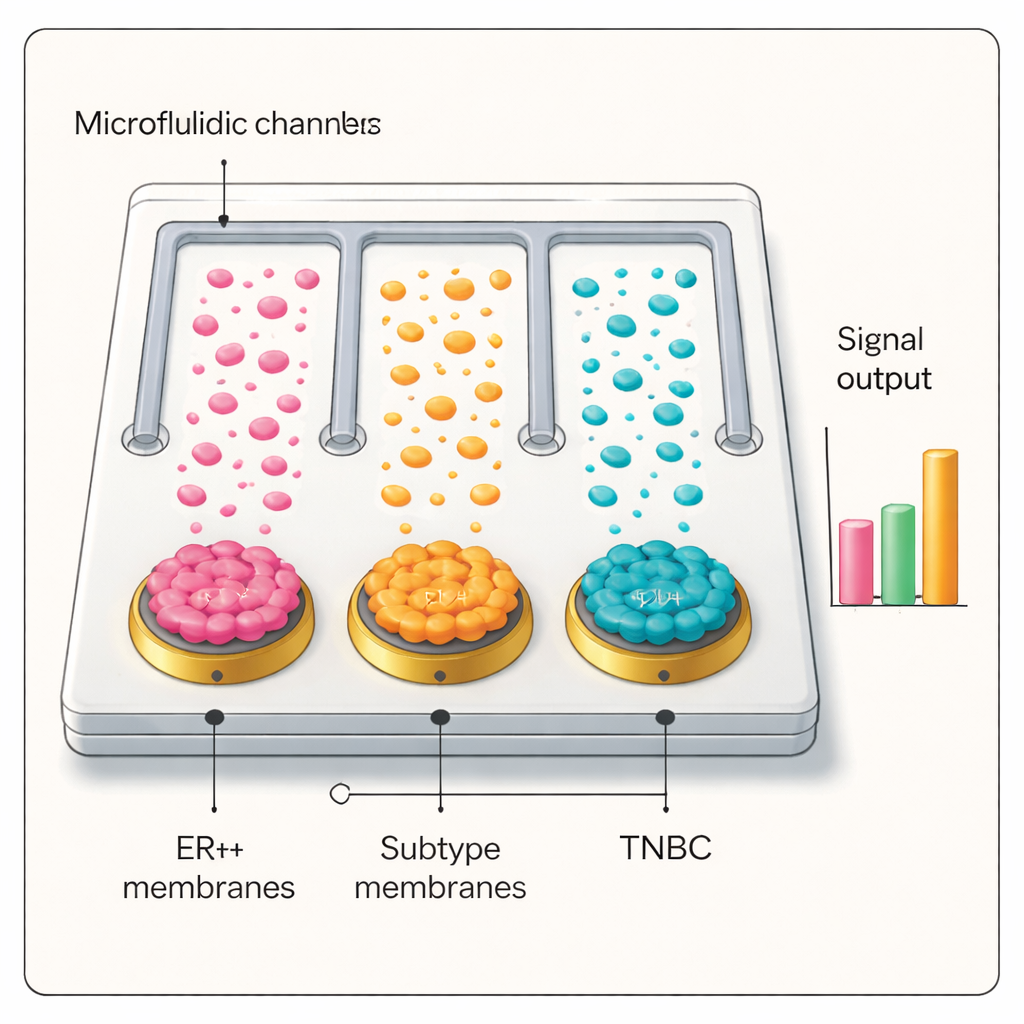
Du banc de laboratoire aux échantillons sanguins de patients
Équipée de cette interface sélective et sensible, l’équipe a construit une puce microfluidique contenant des canaux parallèles, chacun revêtu d’une membrane de cellule cancéreuse différente, plus un témoin non revêtu. Lorsque le plasma de patients était injecté dans la puce et sondé avec les balises argent‑anticorps, seul le canal dont la membrane correspondait au sous‑type tumoral du patient produisait un signal électrique élevé. Dans des tests en aveugle réalisés sur des dizaines de personnes — comprenant des patientes ER+ et triple négatif, des individus avec des maladies mammaires bénignes, des patients atteints de cancer du poumon et des volontaires sains — la plateforme a distingué avec précision le cancer du non‑cancer et a correctement identifié les sous‑types du cancer du sein. Les performances diagnostiques égalent ou dépassent celles de la pathologie standard dans de nombreux cas et montrent un potentiel pour le stadification de la maladie et le suivi de son évolution.
Ce que cela pourrait signifier pour les soins du cancer à venir
En termes simples, les chercheurs ont transformé l’enveloppe externe du cancer en un appât hautement sélectif pour les particules que les tumeurs libèrent dans le sang. En lisant la signature électrique du canal qui « s’allume », les médecins pourraient un jour déterminer non seulement la présence d’un cancer mais aussi son type, à partir d’un simple prélèvement sanguin. Bien que le système nécessite encore des améliorations — par exemple l’ajout de marqueurs et de types de membranes supplémentaires, et l’intégration d’analyses de données avancées — il indique une trajectoire vers un avenir où des tests sanguins routiniers et peu invasifs aideront à guider des traitements personnalisés et à surveiller l’évolution des tumeurs dans le temps.
Citation: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Mots-clés: sous-types du cancer du sein, biopsie liquide, vésicules extracellulaires, diagnostic microfluidique, capteurs à base de membrane cellulaire