Clear Sky Science · fr
Assemblages moléculaires cycliques pour l’imagerie et la perturbation du Golgi
Transformer le centre d’expédition de la cellule en une cible stratégique
À l’intérieur de chaque cellule animale se trouve l’appareil de Golgi, une station de tri active qui achève, emballe et expédie des milliers de protéines et de lipides. De nombreuses cellules cancéreuses dépendent fortement de ce centre pour modifier les signaux de croissance et sécréter des facteurs qui façonnent leur environnement. Cet article présente de petites molécules conçues qui se dirigent vers le Golgi, permettent son imagerie rapide et, une fois ré‑ingénierées, peuvent bloquer sélectivement ses opérations pour affaiblir les cellules cancéreuses tout en épargnant certaines cellules saines.
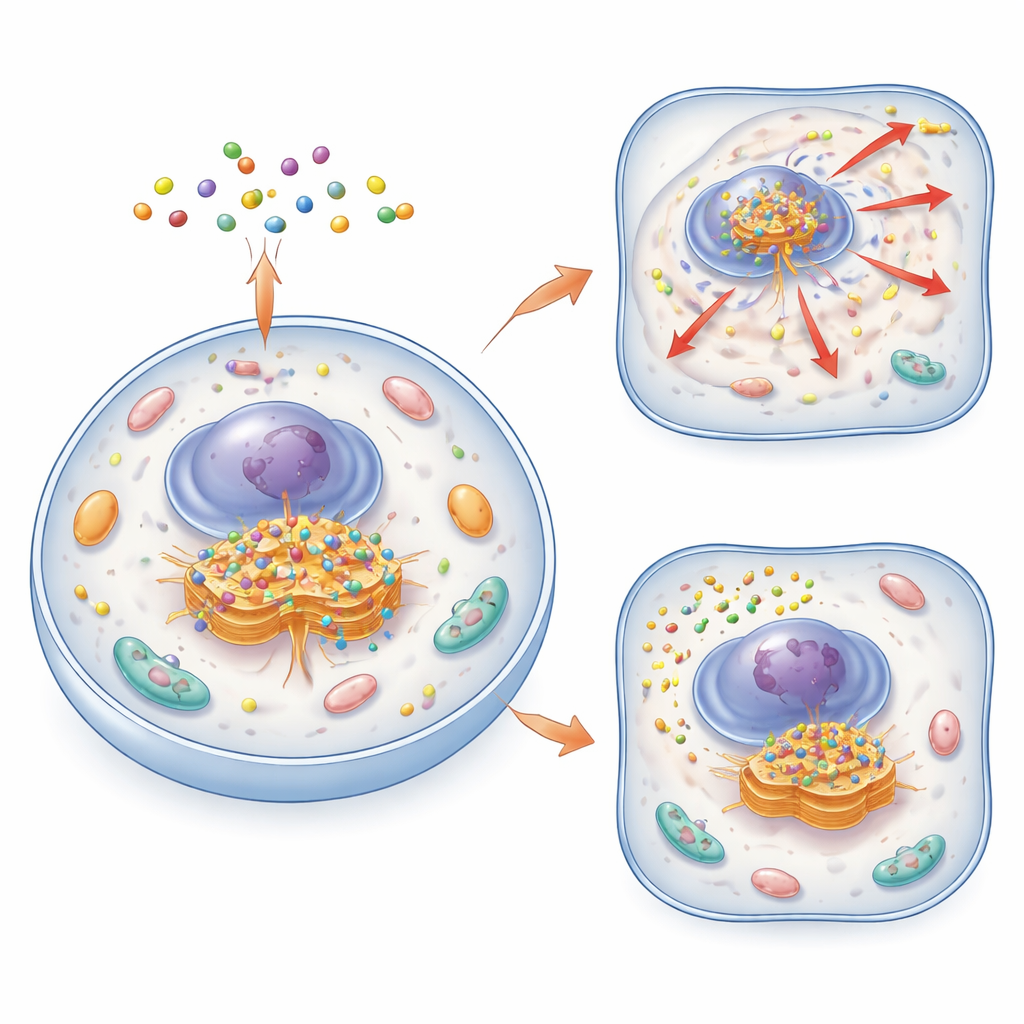
Une nouvelle façon de repérer et d’observer le Golgi
Les auteurs ont créé une famille de petites molécules intelligentes appelées assemblages moléculaires cycliques, ou CyMA. Ces molécules sont construites à partir de peptides courts qui peuvent à la fois traverser les membranes cellulaires et s’agréger en petits amas. Dans leur version « imagerie » (CyMA‑i), les peptides portent une sonde fluorescente qui s’allume fortement lorsque les molécules s’assemblent. Une fois à l’intérieur de la cellule, des enzymes enlèvent un capot protecteur du précurseur CyMA, exposant une poignée réactive. Des enzymes résidentes du Golgi attachent ensuite une chaîne grasse à cette poignée, rendant les molécules beaucoup plus adhésives et susceptibles de s’auto‑assembler précisément au niveau du Golgi. Parce que ce processus est rapide et utilise la machinerie cellulaire naturelle, les chercheurs peuvent dessiner la forme du Golgi dans des cellules vivantes en quelques minutes et à des concentrations de sonde très faibles.
Un cycle futile qui ancre les molécules au Golgi
Les CyMA ne sont pas de simples marqueurs : ils sont conçus pour participer à un « cycle futile » au Golgi. Un groupe d’enzymes ajoute des chaînes grasses au peptide, tandis qu’un autre les retire. À mesure que la cellule ajoute et retire ces chaînes, les peptides modifiés continuent de s’assembler et de se désassembler sur place. Ce va‑et‑vient constant piège un noyau de type solide d’assemblages sur les membranes du Golgi, tout en maintenant le renouvellement des molécules individuelles. La cellule doit sans cesse dépenser ses propres précurseurs en acides gras pour entretenir cette boucle, alimentant en fait les assemblages et aidant à leur persistance. Parallèlement, d’autres enzymes peuvent lentement couper une liaison ester distincte au sein des CyMA, les transformant en fragments plus hydrophiles qui dérivent. Parce que certaines cellules saines, comme les hépatocytes et certaines cellules immunitaires, sont riches en ces estérases, elles sont naturellement plus aptes à démanteler les CyMA et sont donc moins affectées.
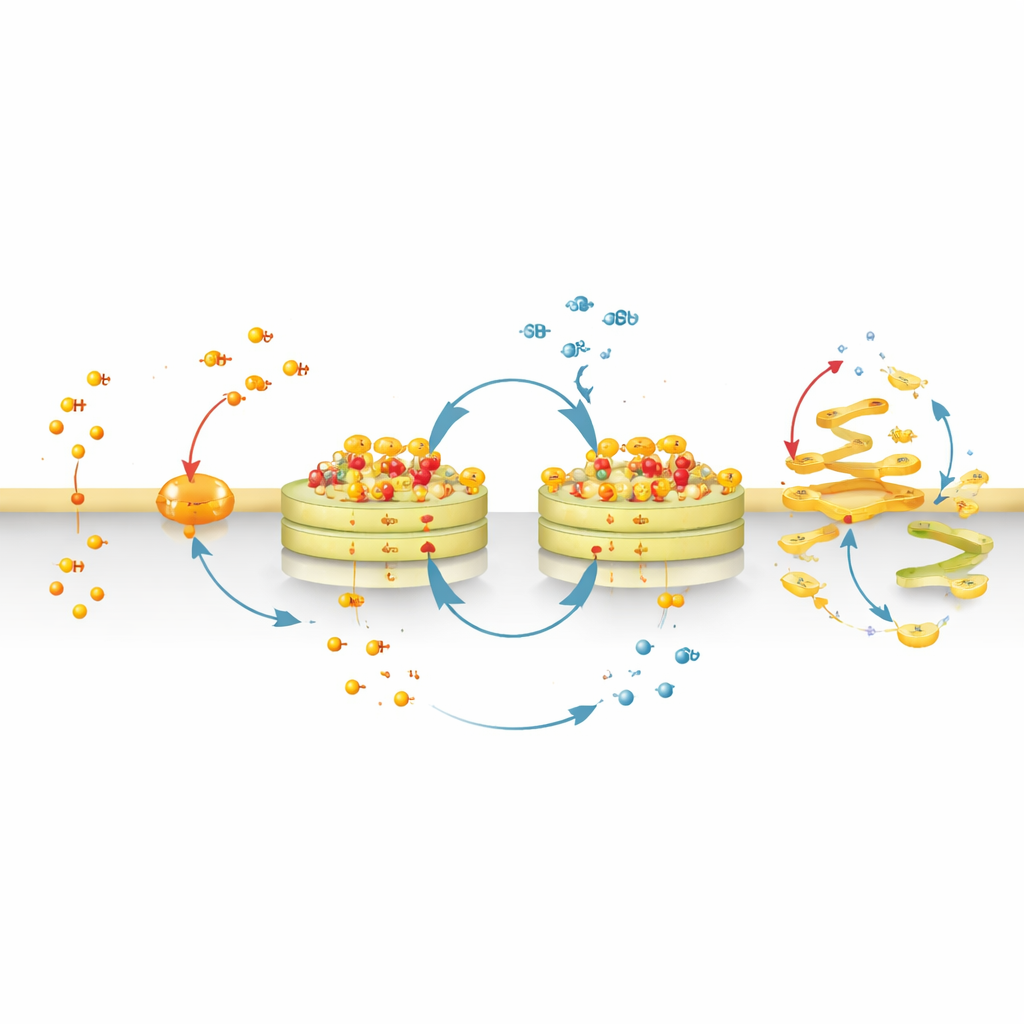
De l’outil d’imagerie doux au perturbateur du Golgi
En remplaçant la sonde fluorescente par un groupe chimique plus fortement attiré par les membranes, l’équipe a converti CyMA‑i en CyMA‑d, une version perturbatrice qui ne brille plus mais qui continue de cycler et de s’assembler au Golgi. Ces assemblages perturbent physiquement la structure du Golgi et le flux constant de vésicules vers et depuis celui‑ci. Les protéines qui normalement voyagent du réticulum endoplasmique vers le Golgi puis vers la surface cellulaire se retrouvent bloquées ou mal acheminées. Les voies d’entrée — depuis la surface cellulaire vers le Golgi ou du Golgi vers d’autres organites — sont également obstruées. En conséquence, des récepteurs de surface clés et des molécules de signalisation ne parviennent pas à leurs destinations ou s’accumulent aux mauvais endroits à l’intérieur de la cellule.
Brouiller les signaux cellulaires et les messages sécrétoires
Le Golgi est l’endroit où de nombreuses protéines reçoivent des finitions cruciales, comme des chaînes de sucres et des queues lipidiques. Les assemblages CyMA‑d réduisent la lipation et la glycosylation correctes de nombreuses protéines, y compris des acteurs connus du cancer comme Ras et d’importantes tyrosines kinases réceptrices. Ces altérations détournent des voies favorisant la croissance telles que AKT et mTOR. Parallèlement, la production sécrétoire de la cellule est atténuée : des facteurs importants comme TGF‑β1 et VEGF, que les tumeurs utilisent pour supprimer l’immunité et stimuler la néovascularisation, ne sont plus efficacement libérés. Le stress induit par cette panne provoque un réseau de réticulum endoplasmique embrouillé, des mitochondries altérées, une autophagie ralentie (le système de recyclage cellulaire) et une accumulation de protéines endommagées marquées par l’ubiquitine, poussant ensemble les cellules cancéreuses vers la mort.
Pression sélective sur les tumeurs et promesse thérapeutique
Parce que CyMA‑d dépendent d’un ensemble partagé d’enzymes et de métabolites que de nombreuses cellules cancéreuses surutilisent, ils peuvent tuer une large gamme de types tumoraux, y compris des modèles de cancer de l’ovaire résistants aux médicaments, à très faibles doses. Les cellules présentant des niveaux élevés d’estérases spécifiques démantèlent toutefois plus facilement les CyMA‑d et sont donc moins affectées, offrant un mécanisme intrinsèque de sélectivité. Dans des sphéroïdes tumoraux tridimensionnels, des cultures dérivées de patients et des modèles murins, CyMA‑d réduisent les tumeurs, diminuent les métastases et réduisent l’accumulation de liquide dans l’abdomen. Associés aux thérapies par inhibiteurs de points de contrôle immunitaire, ils renforcent encore le contrôle tumoral et la survie. En substance, ce travail montre que construire des matériaux dynamiques à l’intérieur du Golgi — plutôt que de cibler une protéine unique — peut mettre hors service plusieurs processus critiques pour le cancer en même temps.
Ce que cela signifie pour les traitements futurs
Pour un non‑spécialiste, l’idée principale est que les auteurs ont transformé le Golgi d’un spectateur passif en une cible thérapeutique active. En recrutant les propres enzymes de la cellule pour assembler et recycler de petites molécules à ce carrefour central, ils peuvent soit le mettre en évidence sans danger, soit progressivement submerger sa fonction. Cette plateforme à double usage suggère un nouveau type de traitement : au lieu de concevoir un médicament pour une protéine unique, on pourrait concevoir de petits précurseurs que les cellules transforment en matériaux auto‑organisés, capables de perturber des réseaux entiers de communication et de transport dont les cancers dépendent pour croître et se disséminer.
Citation: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
Mots-clés: Appareil de Golgi, assemblages moléculaires, trafic des protéines, thérapie contre le cancer, ciblage d’organites