Clear Sky Science · fr
PDLIM5 endothélial favorise la formation de filopodes des cellules tip et l’angiogenèse tumorale en régulant le rassemblement de l’actine dépendant d’ACTN1/ACTN4
Comment le cancer détourne les vaisseaux sanguins
Le cancer ne peut pas croître au‑delà d’une petite masse sans persuader les vaisseaux sanguins environnants d’apporter oxygène et nutriments. Cette étude révèle comment une protéine peu connue de l’endothélium vasculaire aide les tumeurs à faire pousser de nouvelles branches anormales. Comprendre ce mécanisme pourrait ouvrir la voie à des traitements plus intelligents qui non seulement affament les tumeurs, mais améliorent aussi l’efficacité de l’immunothérapie.
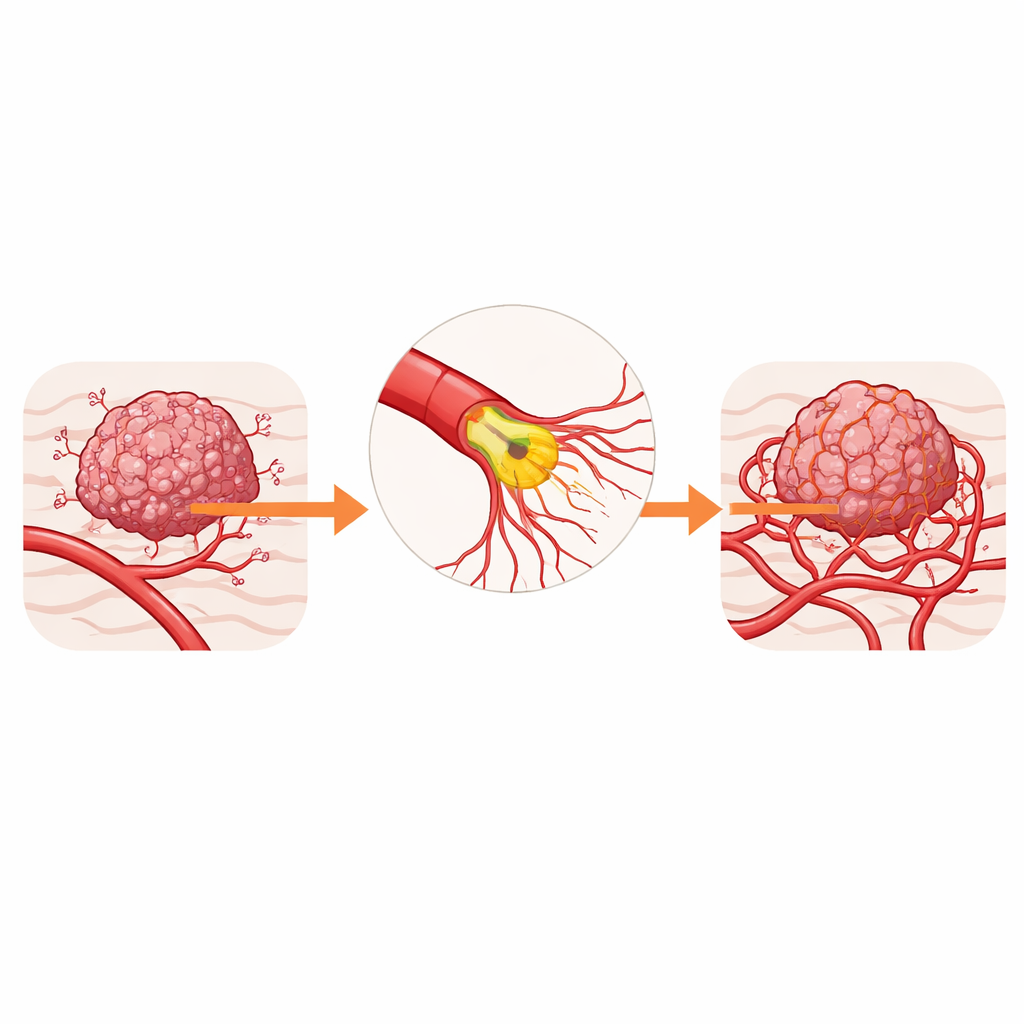
Les architectes cachés de l’apport sanguin tumoral
Les vaisseaux qui irriguent les tumeurs sont constitués de cellules spécialisées appelées cellules endothéliales, qui tapissent l’intérieur du vaisseau. À l’avant de chaque nouvelle branche se trouve une « cellule tip » qui émet de longues projections en forme de doigts, appelées filopodes. Ces projections détectent des signaux chimiques provenant de la tumeur et dirigent la croissance des nouvelles pousses vers les zones en déficit d’oxygène. Dans de nombreux cancers, ce bourgeonnement devient excessif, créant des vaisseaux fuyants et tortueux qui aggravent l’hypoxie et compliquent l’accès des médicaments et des cellules immunitaires à la tumeur.
Une protéine qui suralimente la croissance des pousses
En analysant des cellules individuelles issues de tumeurs pulmonaires humaines, les chercheurs ont constaté que les cellules endothéliales associées aux tumeurs activent fortement un ensemble de gènes contrôlant l’ossature interne de la cellule, en particulier une protéine nommée PDLIM5. PDLIM5 était plus abondante dans les vaisseaux tumoraux que dans les vaisseaux normaux, et les patients dont les vaisseaux tumoraux exprimaient davantage de PDLIM5 avaient tendance à présenter une survie plus courte. Dans des modèles murins de plusieurs cancers, l’augmentation de PDLIM5 dans l’endothélium a accéléré la croissance tumorale et entraîné des réseaux de vaisseaux plus denses, suggérant que cette protéine agit comme un puissant moteur de la néo‑vascularisation tumorale.
Comment PDLIM5 construit des « antennes » cellulaires
Pour comprendre l’effet de PDLIM5 sur le comportement des vaisseaux, l’équipe a utilisé des systèmes expérimentaux où l’on peut observer les nouvelles pousses en détail, comme la croissance vasculaire dans la rétine de souris et des cultures tridimensionnelles de cellules endothéliales. Lorsqu’on a éliminé PDLIM5 spécifiquement dans les cellules endothéliales, les pousses progressaient plus lentement, comportaient moins de cellules tip et produisaient beaucoup moins de filopodes. Au niveau microscopique, PDLIM5 relie deux protéines clés de groupement de l’actine, ACTN1 et ACTN4, aux longs brins d’actine qui forment l’ossature interne de la cellule. Cette action de liaison favorise l’assemblage des brins d’actine en faisceaux rigides qui soutiennent les filopodes. La mutation de deux résidus critiques de PDLIM5 (nommés S593 et F596) rompait cette connexion, affaiblissait le groupement de l’actine et empêchait PDLIM5 de restaurer le bourgeonnement normal, prouvant que cette interaction moléculaire est essentielle à la formation des « antennes » des cellules tip.
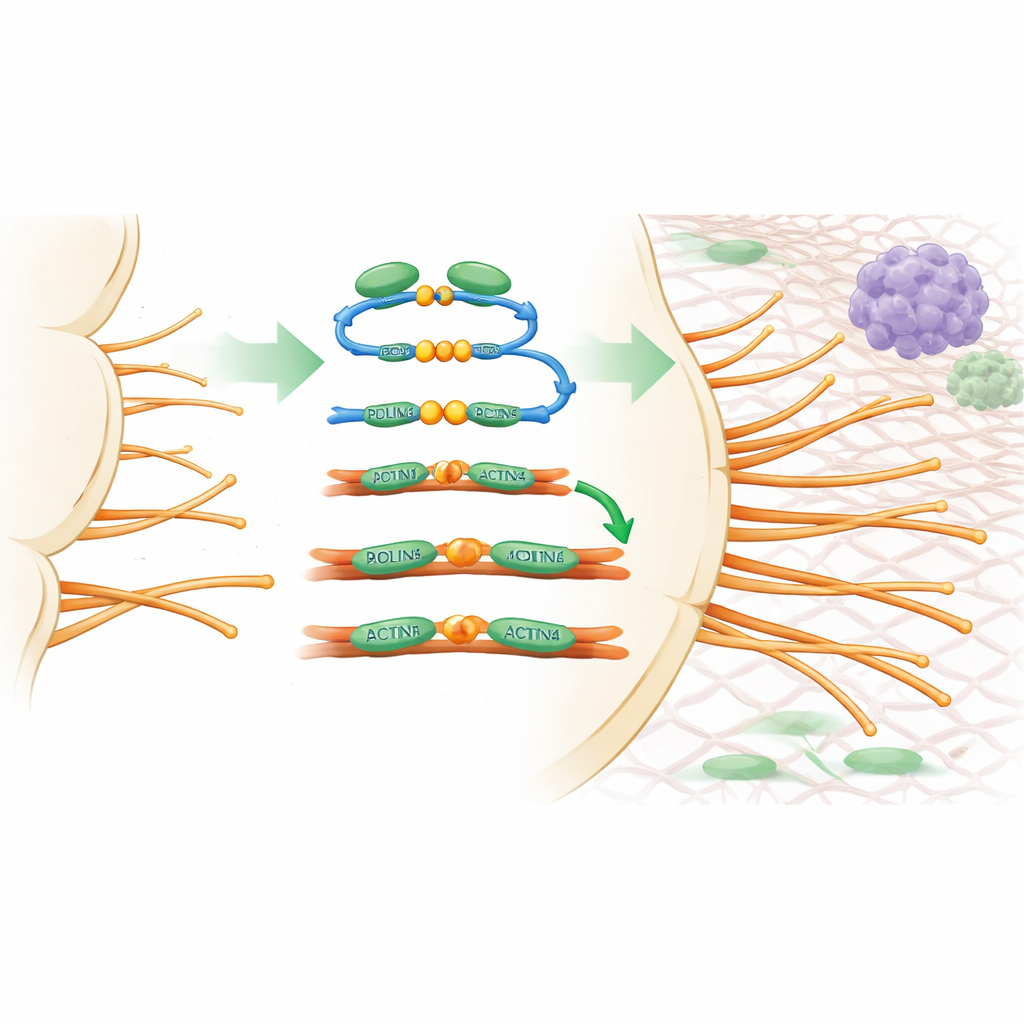
Reconfigurer les vaisseaux tumoraux pour aider le système immunitaire
De manière surprenante, bloquer PDLIM5 dans l’endothélium n’a pas seulement ralenti la croissance tumorale. Les vaisseaux tumoraux sont devenus plus réguliers, moins perméables et mieux couverts par des cellules de soutien stabilisatrices. Par conséquent, la distribution d’oxygène s’est améliorée et les zones d’hypoxie sévère ont diminué. Ces vaisseaux « normalisés » ont permis une plus grande infiltration des lymphocytes T dans la tumeur. La perte de PDLIM5 a aussi modifié l’organisation des molécules d’adhésion sur les cellules endothéliales, facilitant l’attachement des lymphocytes T aux parois vasculaires et leur passage dans le tissu tumoral. Dans des tumeurs murines habituellement résistantes aux inhibiteurs de points de contrôle immunitaire, la suppression de PDLIM5 a rendu le traitement par un anticorps anti–PD‑L1 beaucoup plus efficace, réduisant les tumeurs tout en augmentant à la fois les lymphocytes T auxiliaires et cytotoxiques à l’intérieur de celles‑ci.
Pourquoi cela importe pour les thérapies futures contre le cancer
Pris dans leur ensemble, ces résultats montrent que PDLIM5 agit comme un organisateur central de l’armature d’actine des cellules tip, permettant une forte formation de filopodes et un bourgeonnement vasculaire rapide vers les tumeurs. Supprimer ou neutraliser PDLIM5 dans les cellules endothéliales ralentit l’expansion de l’apport sanguin tumoral, redresse et stabilise les vaisseaux restants, soulage la privation d’oxygène et favorise l’entrée des cellules immunitaires dans la tumeur. Pour les patients, cela suggère que des médicaments visant à perturber le partenariat PDLIM5–ACTN1/ACTN4 pourraient à la fois priver les cancers de nouveaux vaisseaux et transformer une vascularisation tumorale chaotique en un réseau mieux adapté à la chimiothérapie et à l’immunothérapie.
Citation: Xu, Z., Shi, Y., Yang, Y. et al. Endothelial PDLIM5 promotes tip cell filopodia formation and tumor angiogenesis by regulating ACTN1/ACTN4-dependent actin bundling. Nat Commun 17, 2103 (2026). https://doi.org/10.1038/s41467-026-68765-x
Mots-clés: angiogenèse tumorale, cellules tip endothéliales, PDLIM5, cytosquelette d’actine, immunothérapie contre le cancer