Clear Sky Science · fr
Faire taire le catabolisme lipidique détermine la longévité en réponse au jeûne
Pourquoi arrêter de brûler les graisses peut être une bonne chose
Beaucoup pensent que le jeûne est bénéfique parce qu’il force l’organisme à brûler des graisses pour produire de l’énergie. Cette étude, menée chez le petit nématode Caenorhabditis elegans, renverse cette idée. Les chercheurs montrent que la clé d’une vie prolongée après un jeûne n’est pas l’intensité avec laquelle les cellules activent la combustion des graisses, mais la précision avec laquelle elles l’éteignent une fois la nourriture réintégrée. Comprendre ce mécanisme d’activation et d’arrêt dans un animal simple pourrait, à terme, orienter la conception de stratégies de jeûne et d’alimentation chez l’humain.
Un animal simple à métabolisme flexible
Les auteurs utilisent C. elegans, un ver microscopique dont le métabolisme et les voies du vieillissement partagent de nombreux traits avec les nôtres. Ils ont soumis des vers adultes jeunes à un jeûne de 24 heures suivi d’un réalimentation. Pendant le jeûne, les vers ont rapidement puisé dans leurs principales réserves de lipides — des triglycérides stockés dans des gouttelettes intestinales — tout en préservant le cholestérol essentiel. Lors du retour à la nourriture, les gouttelettes lipidiques et les profils d’acides gras libres sont revenus aux niveaux d’avant le jeûne, et les vers ont maintenu des niveaux normaux d’énergie (ATP) dans leurs muscles. Malgré cette stabilité énergétique, un seul cycle jeûne‑réalimentation a prolongé la durée de vie médiane d’environ 40 % et a préservé une plus grande vigueur des animaux à un âge avancé.
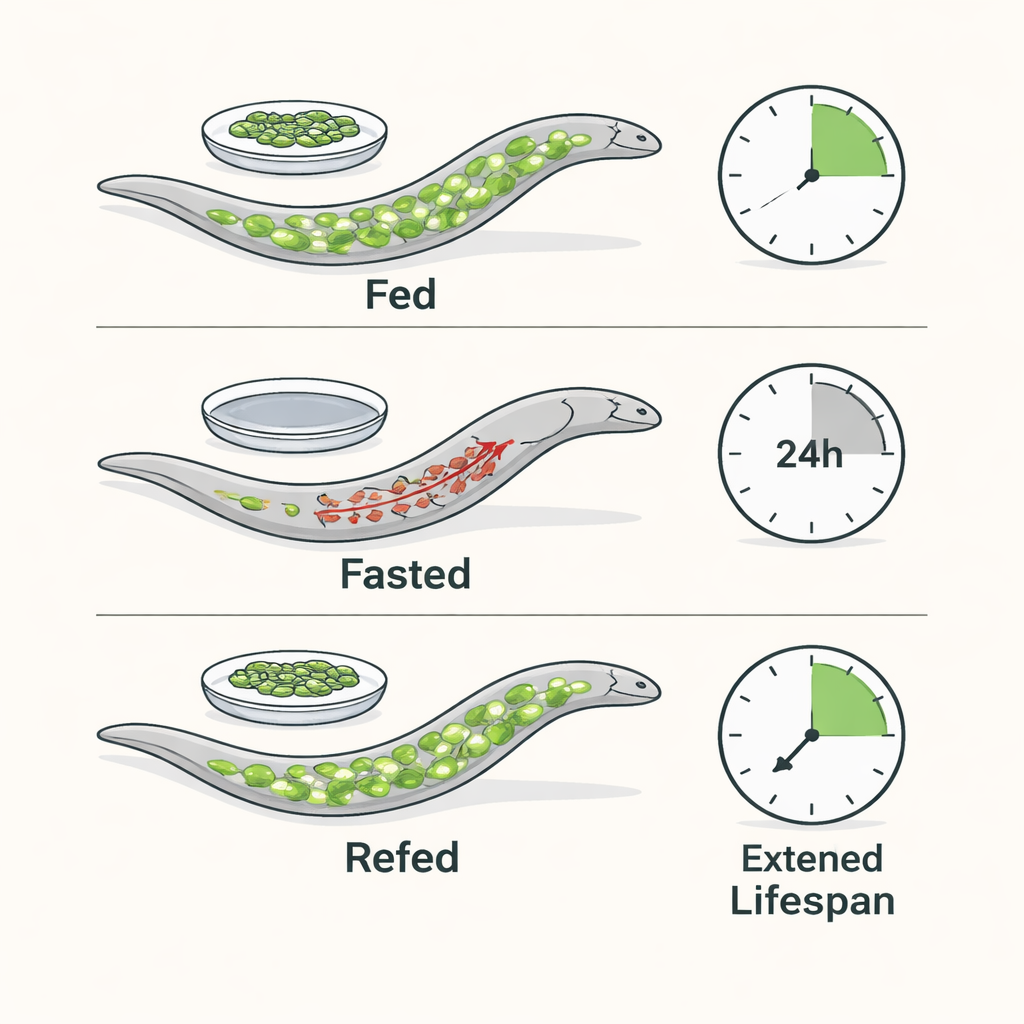
La combustion des graisses n’est pas nécessaire au bénéfice du jeûne sur la longévité
Parce que le jeûne pousse normalement les cellules à dégrader les graisses, l’équipe s’est demandé si cette combustion lipidique est réellement nécessaire pour allonger la vie. Ils se sont concentrés sur NHR‑49, un récepteur nucléaire qui active les gènes de la β‑oxydation mitochondriale, la principale voie de combustion des graisses. Les vers dépourvus de NHR‑49 ne pouvaient pas induire correctement ces gènes pendant le jeûne et présentaient des chutes d’ATP plus prononcées. Pourtant, de manière surprenante, ils ont tout de même bénéficié d’une forte extension de la durée de vie après le jeûne, similaire à celle des vers normaux. Il en a été de même lorsque les chercheurs ont bloqué génétiquement des étapes en amont de la dégradation lipidique. Ensemble, ces expériences montrent que l’activation robuste du catabolisme lipidique durant le jeûne est, en grande partie, superflue pour l’avantage en terme de longévité.
Un interrupteur temporel qui arrête la combustion des graisses
Si l’activation de la combustion des graisses n’est pas essentielle, son extinction pourrait l’être. L’étude révèle que NHR‑49 est contrôlé par un mécanisme indépendant d’un ligand — plutôt que d’être activé ou désactivé par une petite molécule de type hormonal, son activité est modulée par des marques chimiques ajoutées directement à la protéine. Lors de la récupération après le jeûne, NHR‑49 reçoit un motif spécifique de groupements phosphate sur des résidus sérine voisins dans une région « charnière » flexible. Ces marques chargées négativement affaiblissent l’affinité de NHR‑49 pour l’ADN et favorisent son retrait des gènes impliqués dans la combustion des graisses, les silencant ainsi au retour de la nourriture. En l’absence de cet arrêt programmé, les cellules risquent de rester bloquées dans un état de combustion excessive des graisses qui peut épuiser les réserves et perturber l’équilibre à long terme.
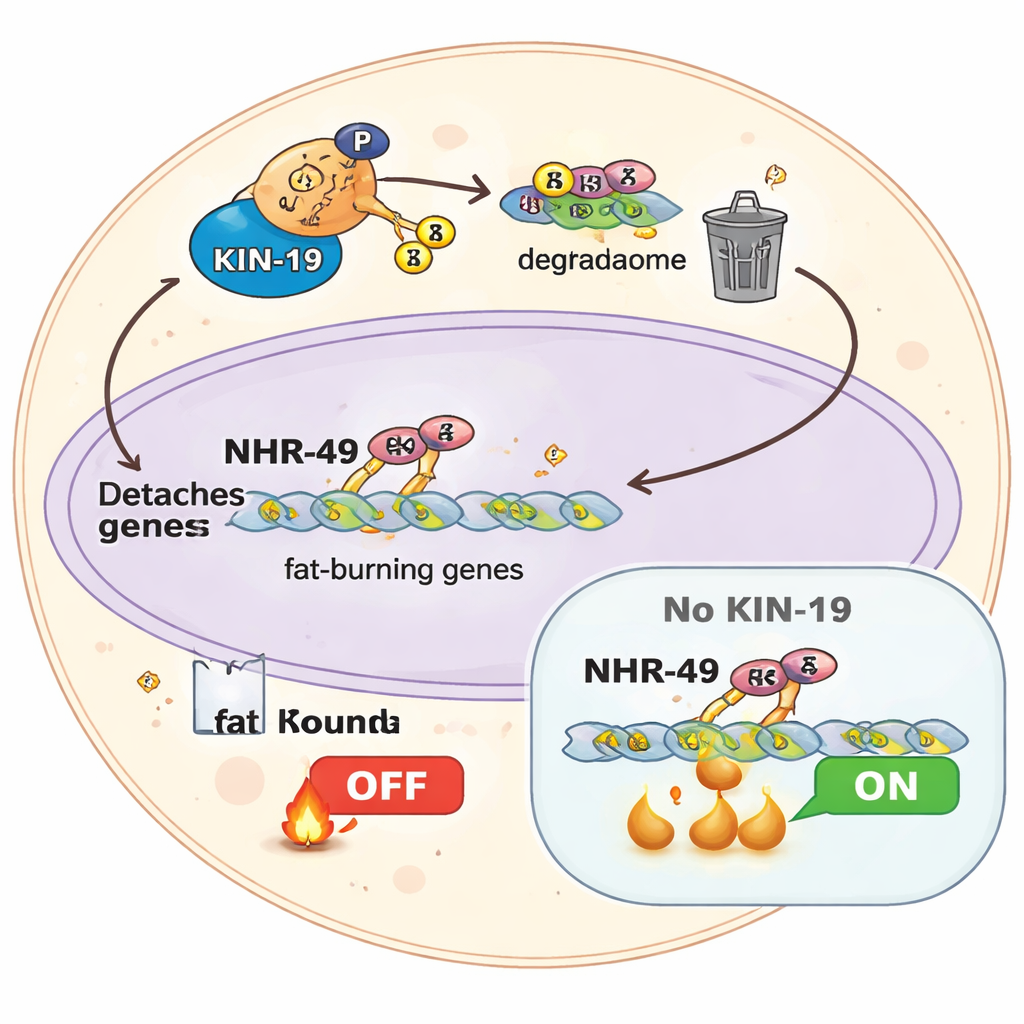
KIN‑19 : l’enzyme qui met fin au jeûne
Les auteurs identifient une kinase de type caseine, KIN‑19, comme un acteur central de ce système d’arrêt. Des essais biochimiques montrent qu’une fois NHR‑49 « amorcé » par une phosphorylation initiale, KIN‑19 ajoute efficacement d’autres phosphates aux résidus voisins. Les vers chez lesquels KIN‑19 est inactivée se comportent comme s’ils étaient en jeûne permanent : ils sont plus petits, ont de faibles réserves lipidiques, une morphologie mitochondriale modifiée et une consommation d’oxygène réduite, même en présence de nourriture. Leurs profils d’expression génique ressemblent à un état de jeûne chronique, et leurs niveaux d’énergie ne se rétablissent pas correctement après réalimentation. Surtout, lorsque KIN‑19 est déficiente, un jeûne de 24 heures n’allonge plus la durée de vie ; le gain de longévité se réduit à un effet minimal. Cela indique que l’arrêt de la combustion lipidique orchestré par KIN‑19 via NHR‑49 est essentiel pour que le jeûne favorise un vieillissement sain.
Ce que cela signifie pour le jeûne et le vieillissement sain
Pour un lecteur non spécialiste, le message central est que la capacité de l’organisme à changer de mode peut compter plus que l’intensité avec laquelle il reste dans un mode donné. Chez le ver, le jeûne est bénéfique non parce qu’il brûle le plus de graisses possible, mais parce qu’il permet une transition fluide vers un mode de stockage et de réparation quand la nourriture revient. L’enzyme KIN‑19 aide à terminer la phase de combustion des graisses en marquant et en éliminant NHR‑49, évitant ainsi un état d’« urgence » permanent et délétère. Bien que l’homme soit bien plus complexe, ce travail suggère que des stratégies de jeûne efficaces pourraient dépendre de périodes soigneusement synchronisées d’activation et de repos métabolique, plutôt que d’une perte de graisse continue et agressive.
Citation: Tatge, L., Kim, J., Solano Fonseca, R. et al. Silencing lipid catabolism determines longevity in response to fasting. Nat Commun 17, 1919 (2026). https://doi.org/10.1038/s41467-026-68764-y
Mots-clés: jeûne et longévité, métabolisme des lipides, récepteurs hormonaux nucléaires, flexibilité métabolique, vieillissement de C. elegans