Clear Sky Science · fr
Un chimère antigénique en tandem stabilisée qui suscite une puissante activité réduisant la transmission du paludisme
Pourquoi il est important d’arrêter la transmission par les moustiques
Les vaccins antipaludiques actuellement utilisés peuvent réduire fortement les formes graves et la mortalité chez les jeunes enfants, mais ils laissent une brèche majeure : les personnes qui ne ressentent pas de symptômes peuvent toujours porter des parasites capables d’infecter les moustiques et de maintenir la transmission. Cette étude présente une conception vaccinale de nouvelle génération visant non pas seulement à protéger un individu, mais à rompre la chaîne d’infection entre humains et moustiques. En contrôlant avec précision la manière dont des protéines clés du parasite sont exposées au système immunitaire, les chercheurs cherchent à générer des anticorps qui rendent les moustiques de mauvais hôtes pour le paludisme, aidant ainsi les communautés à se rapprocher de l’élimination.
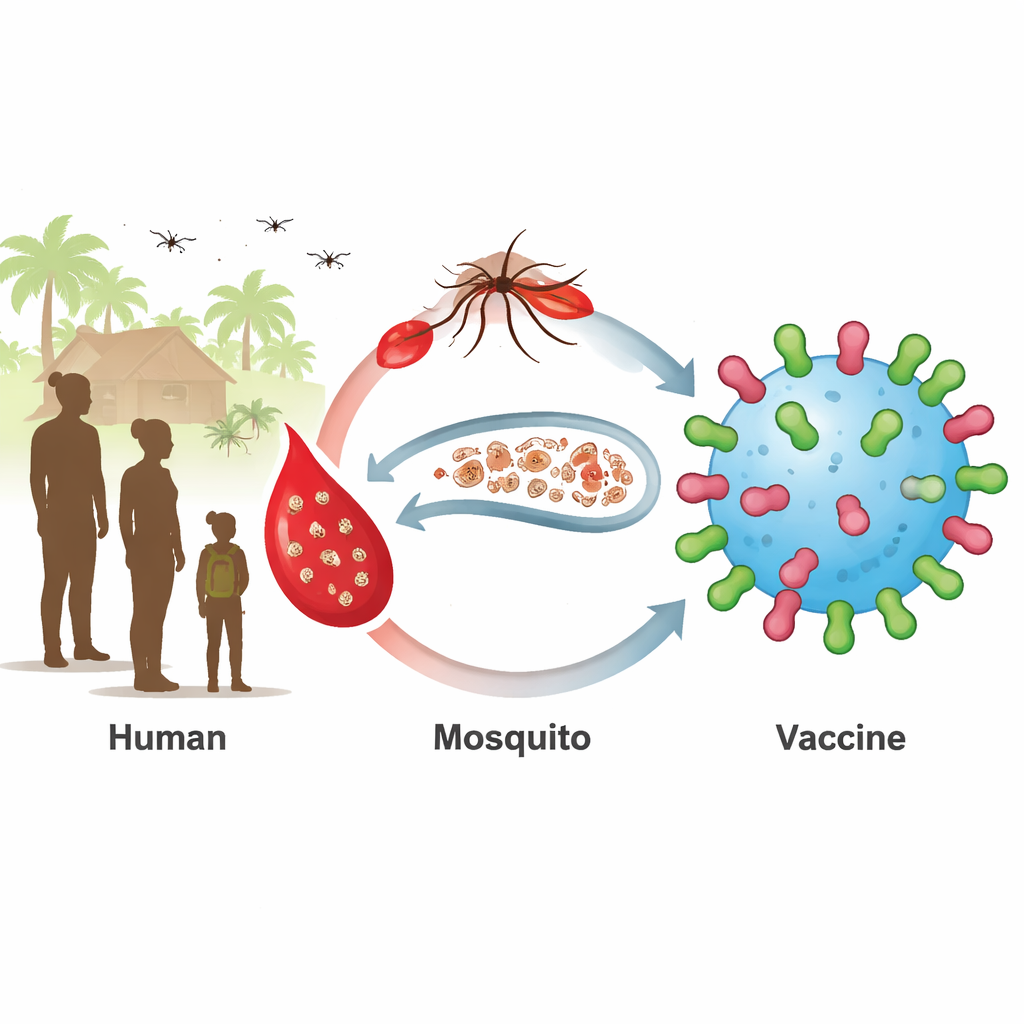
Un réservoir caché qui entretient le paludisme
Les vaccins actuels contre le paludisme ciblent les premiers stades de l’infection au niveau du foie et du sang. Ils sont les plus efficaces chez les jeunes enfants, mais les enfants plus âgés et les adultes hébergent souvent, sans symptômes, des parasites au stade sexué mature appelés gamétocytes. Quand des moustiques piquent ces personnes, ils prélèvent ces parasites et les propagent. Deux protéines de surface du parasite, connues sous les noms de Pfs230 et Pfs48/45, se trouvent à ces stades sexuels et constituent des cibles attrayantes pour les vaccins dits « bloquant la transmission ». Des vaccins basés sur des fragments de ces protéines ont été testés en essais cliniques, mais ils ont eu du mal à produire des réponses en anticorps robustes et durables chez tous les receveurs.
Concevoir un leurre plus intelligent pour le système immunitaire
Pour améliorer les conceptions précédentes, les auteurs ont adopté une approche de biologie structurale, examinant en détail atomique la manière dont de puissants anticorps humains se lient à Pfs230 et Pfs48/45. Ils ont identifié de petites régions, ou épitopes, particulièrement efficaces pour bloquer le développement du parasite dans le moustique. Tout aussi important, ils ont cartographié des épitopes « non fonctionnels » qui attirent des anticorps qui se lient mais n’empêchent pas la transmission—gastronomiquement parlant, une dépense d’énergie immunitaire. À l’aide de modélisation informatique et d’outils de génie protéique, ils ont fusionné la région la plus puissante de Pfs230 (son premier domaine) à la région clé de Pfs48/45 (son troisième domaine) en une seule protéine soigneusement arrangée qu’ils appellent une chimère antigénique en tandem stabilisée, ou STAC.
Cacher les cibles inutiles, garder les utiles
Le défi consistait à présenter ces deux domaines ensemble d’une manière qui imite leur position sur le parasite, tout en cachant physiquement les surfaces non fonctionnelles qui sont normalement enfouies dans la protéine intacte. L’équipe a repensé de façon itérative le court lien et l’interface entre les deux domaines, testant chaque version pour la stabilité, le repliement correct et la capacité à lier un panel d’anticorps bien caractérisés. Des logiciels de conception avancée ont suggéré des mutations qui resserraient l’interface et amélioraient l’expression dans des cellules en culture. Des études structurales par cristallographie aux rayons X, diffusion aux petits angles des rayons X et cryo‑microscopie électronique ont confirmé que, dans la construction STAC finale, les épitopes souhaités sont présentés avec une grande fidélité, tandis que les sites connus peu utiles sont bloqués stériquement.
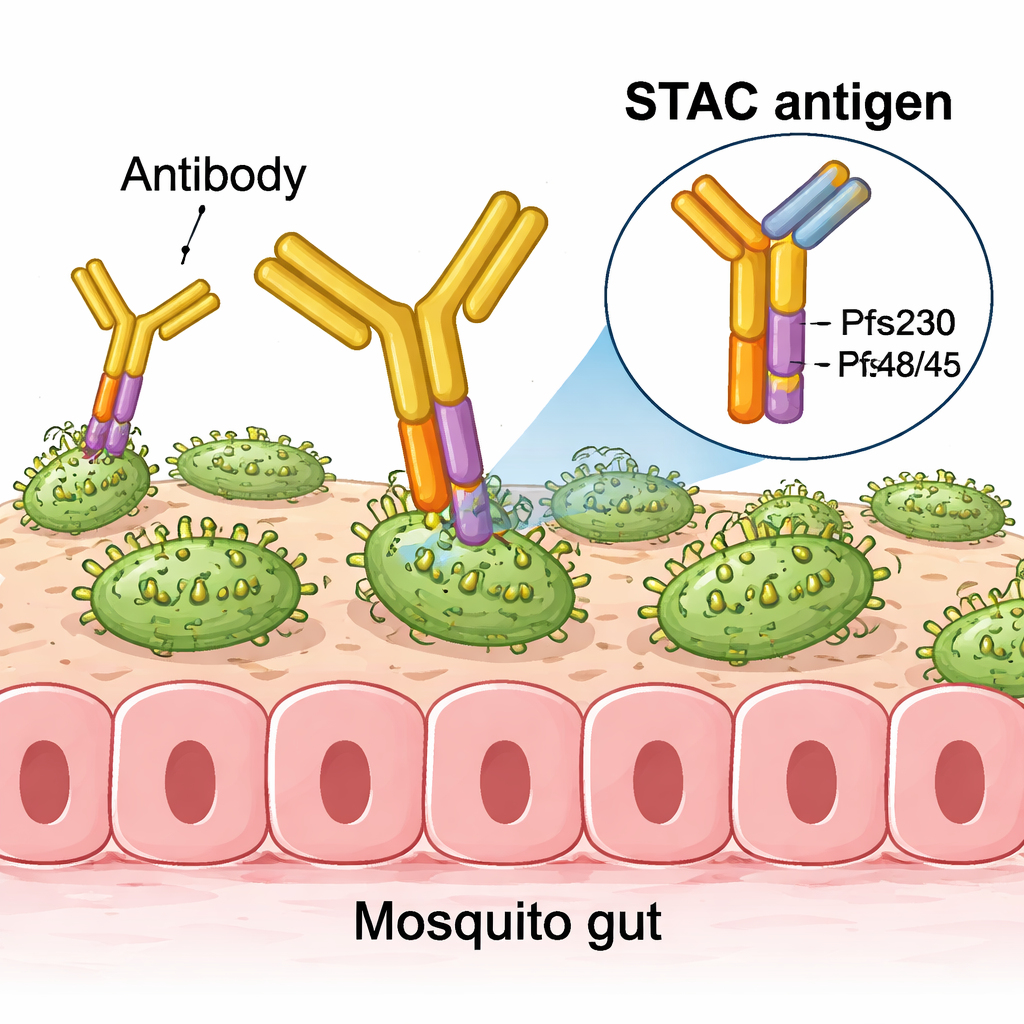
Des molécules isolées à des nanoparticules puissantes
Des essais chez la souris ont montré que lorsque le STAC était fixé à des liposomes spécialisés ou à des nanoparticules protéiques auto‑assemblées, il déclenchait des réponses en anticorps fortes capables de réduire nettement le développement du parasite dans des tests standard d’alimentation de moustiques. À doses égales ou plus faibles, le STAC égalait souvent ou surpassait des vaccins utilisant séparément des fragments de Pfs230 et Pfs48/45, qu’ils soient administrés seuls, mélangés ou co‑exposés sur la même particule. Dans des tests très sensibles où le sérum de souris était fortement dilué, les anticorps suscités par des nanoparticules décorées de STAC maintenaient mieux l’activité réduisant la transmission que ceux issus d’autres formulations, ce qui indique des réponses particulièrement puissantes et ciblées.
Ce que cela pourrait signifier pour le contrôle du paludisme
Pour les non‑spécialistes, l’idée clé est que le STAC est un leurre sur‑mesure qui montre au système immunitaire exactement les parties du parasite du paludisme qui comptent le plus pour bloquer la propagation, tout en cachant les régions distrayantes qui n’aident pas. Chez les modèles animaux, cette conception produit des anticorps qui empêchent les parasites de compléter leur cycle de vie dans les moustiques, même lorsque les niveaux d’anticorps sont relativement faibles. Si des résultats similaires se confirment chez l’homme, le STAC pourrait devenir un partenaire puissant des vaccins antipaludiques existants : protégeant les personnes vaccinées contre la maladie tout en réduisant le réservoir infectieux dans la communauté. Plus largement, ce travail illustre comment une compréhension structurale détaillée et le génie protéique peuvent être exploités pour concevoir des vaccins multi‑composants puissants, stables et potentiellement moins coûteux à fabriquer.
Citation: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Mots-clés: vaccins antipaludiques, blocage de la transmission, Pfs230, Pfs48/45, immunogène nanoparticule