Clear Sky Science · fr
Rôle essentiel de l’axe NONO‑HOXA1‑Wnt dans la différenciation des cardiomyocytes
Pourquoi ces petites cellules cardiaques nous concernent tous
Chaque battement de cœur dépend de milliards de cellules musculaires spécialisées qui se forment in utero. Lorsque ce processus déraille, des nouveau‑nés peuvent présenter de graves malformations cardiaques. Cette étude utilise des cellules souches humaines pour dévoiler un système de contrôle crucial — composé des molécules NONO et HOXA1 et d’un signal bien connu, Wnt — qui aide les cellules précoces à s’engager en tant que muscle cardiaque sain. Comprendre ce circuit caché pourrait à terme améliorer le diagnostic et le traitement des cardiopathies congénitales.
Du récit vierge aux premiers bâtisseurs du cœur
Les chercheurs ont commencé avec des cellules souches pluripotentes induites humaines — des cellules polyvalentes pouvant être orientées vers presque n’importe quel type cellulaire. À l’aide d’un protocole standard, ils ont dirigé ces cellules vers une différenciation en cardiomyocytes, les cellules battantes du cœur. Lorsqu’ils ont supprimé le gène NONO, beaucoup moins de cellules ont acquis une identité cardiaque. Les marqueurs précoces qui apparaissent normalement lorsque les cellules quittent leur état primitif pour la lignée cardiaque étaient fortement réduits. Le séquençage ARN unicellulaire a montré que de nombreuses cellules déficientes en NONO restaient bloquées à mi‑parcours, coincées dans un état mésendodermique immature au lieu d’évoluer vers un muscle cardiaque pleinement développé.
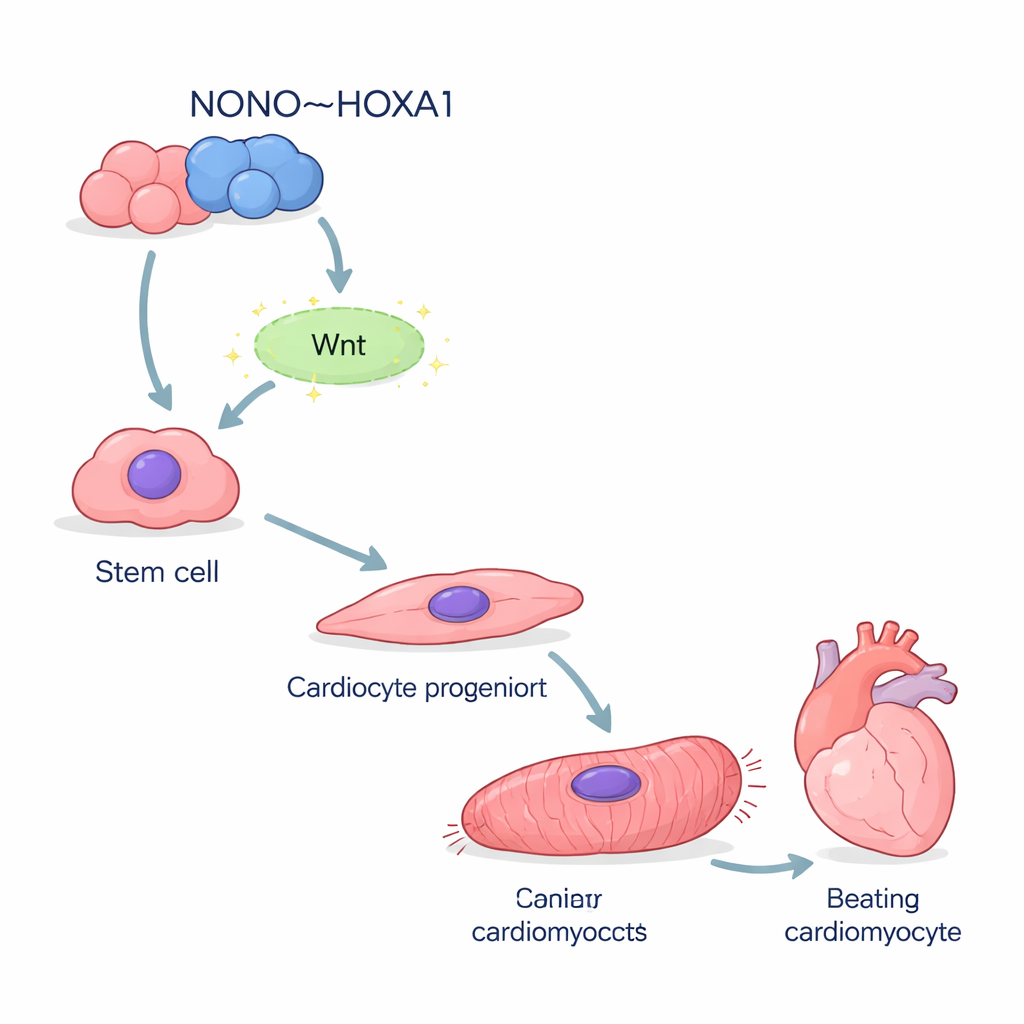
Quand l’ossature manque, les cellules cardiaques chancellent
Les cellules qui parvenaient à devenir cardiomyocytes en l’absence de NONO étaient loin d’être saines. Elles exprimaient des niveaux bien plus faibles de protéines structurelles constituant le sarcomère, la machinerie microscopique responsable de la contraction. Au microscope, la plupart des cellules mutantes montraient des fibres contractiles désorganisées et fragmentées au lieu des rayures régulières observées dans les cellules normales. La microscopie électronique a confirmé que les « barreaux » de type Z‑disc de l’échelle contractile étaient absents ou mal formés. Sur le plan fonctionnel, ces cellules battaient plus lentement et de façon irrégulière. Les mesures des flux calciques — événements électriques déclenchant chaque battement — révélaient des formes d’onde erratiques avec des pics retardés et une récupération lente, en accord avec les défauts d’expression des gènes impliqués dans la gestion du calcium.
Sauver le développement et révéler le partenariat NONO–HOXA1
Pour vérifier que ces anomalies provenaient bien de la perte de NONO, l’équipe a réintroduit NONO de manière contrôlée et inductible par médicament pendant les deux premiers jours de différenciation. Cette brève impulsion de NONO a en grande partie restauré l’activation des gènes cardiaques précoces, augmenté la proportion de cellules battantes et reconstruit des sarcomères et des Z‑discs organisés. Le profilage de l’expression génique a confirmé que de nombreux gènes liés à la contraction musculaire et au développement cardiaque revenaient vers des niveaux normaux. En revanche, des versions mutées de NONO dérivées de patients n’ont pas permis de restaurer la fonction, soutenant l’idée que de tels variants causent la maladie en perturbant ce programme précoce. Des expériences d’interaction protéique ont ensuite révélé que NONO se lie physiquement à un facteur de transcription nommé HOXA1, et que cette interaction stabilise HOXA1 et favorise la formation des dimères nécessaires à la liaison à l’ADN.
Activer le signal Wnt pour engager le destin cardiaque
La cartographie des sites d’ancrage de ces protéines sur le génome a montré que NONO et HOXA1 occupent souvent les mêmes régions régulatrices, y compris celles contrôlant des gènes précoces importants pour le cœur et la voie Wnt. Lorsque NONO manquait, l’adhérence de HOXA1 à bon nombre de ces sites s’en trouvait affaiblie, en particulier sur les gènes qui pilotent le mésoderme précardiaque — le tissu le plus précoce formant le cœur. La voie en aval Wnt/β‑caténine, qui aide normalement à déclencher le mésoderme et le développement cardiaque, était elle aussi atténuée : moins de β‑caténine s’accumulait dans le noyau et les tests rapporteurs sensibles à Wnt montraient une activité réduite. Renforcer le signal Wnt par une dose plus élevée d’un activateur de Wnt durant les tout premiers jours de différenciation a permis de compenser partiellement l’absence de NONO, restaurant davantage de cellules cardiaques et augmentant l’expression des gènes cardiaques.
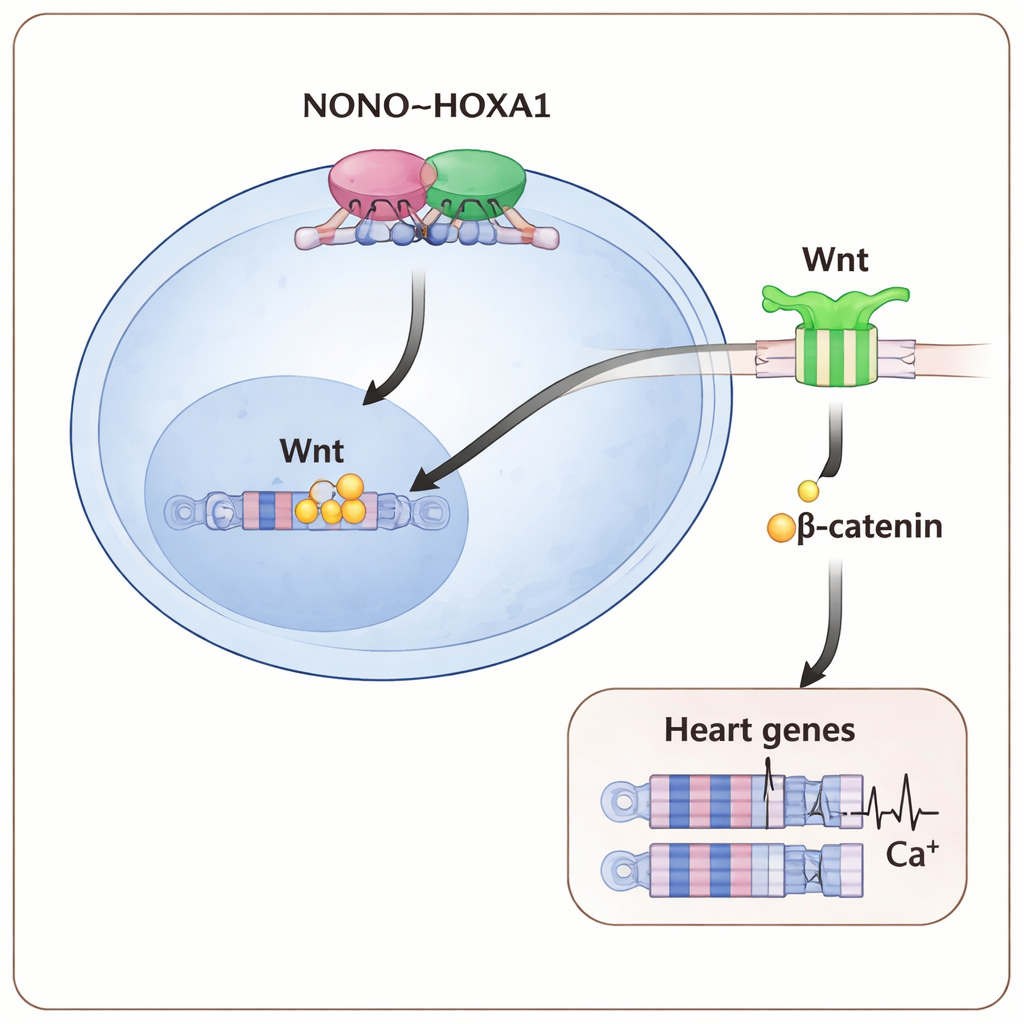
Ce que cela signifie pour la compréhension des malformations congénitales
Pour le grand public, le message central est qu’une petite équipe moléculaire — NONO travaillant main dans la main avec HOXA1 pour ajuster finement les signaux Wnt — agit comme un « régulateur de trafic » précoce qui indique aux jeunes cellules de devenir du muscle cardiaque et leur donne les moyens de battre correctement. Lorsqu’une partie quelconque de cet axe NONO–HOXA1–Wnt est perturbée, les cellules hésitent, des gènes cardiaques clés restent éteints, et les cardiomyocytes résultants sont fragiles sur les plans structurel et électrique. Ces découvertes apportent une explication moléculaire plus nette du lien entre les mutations de NONO et les cardiopathies congénitales, et elles ouvrent des pistes pour manipuler cette voie dans des modèles sur cellules souches ou, un jour, dans des thérapies visant à prévenir ou réparer les malformations cardiaques.
Citation: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Mots-clés: malformations cardiaques congénitales, différenciation des cardiomyocytes, signalisation Wnt, modèles cardiaques sur cellules souches, régulation des gènes