Clear Sky Science · fr
Base structurale de l’inversion de fourche et régulation de RAD51 par le complexe ubiquitine ligase SCF de l’hélicase F-box 1
Comment les cellules secourent une machine de copie de l’ADN bloquée
À chaque division, une cellule doit copier des milliards de lettres d’ADN rapidement et avec précision. Mais cette machinerie de copie se heurte souvent à des problèmes — lésions de l’ADN, séquences difficiles à recopier ou traitements médicamenteux peuvent faire stagner le processus. Dans ces situations, la cellule fait appel à des équipes de réparation d’urgence pour stabiliser et relancer les fourches de réplication. Cet article révèle, avec un niveau de détail structural sans précédent, comment l’un de ces chefs d’équipe — un complexe protéique centré sur l’hélicase FBH1 — remodèle l’ADN bloqué et maintient un autre acteur clé de la réparation, RAD51, strictement contrôlé. Comprendre cette chorégraphie aide à expliquer comment les cellules évitent des cassures dangereuses du génome et pourquoi des perturbations de ces facteurs sont liées au cancer.
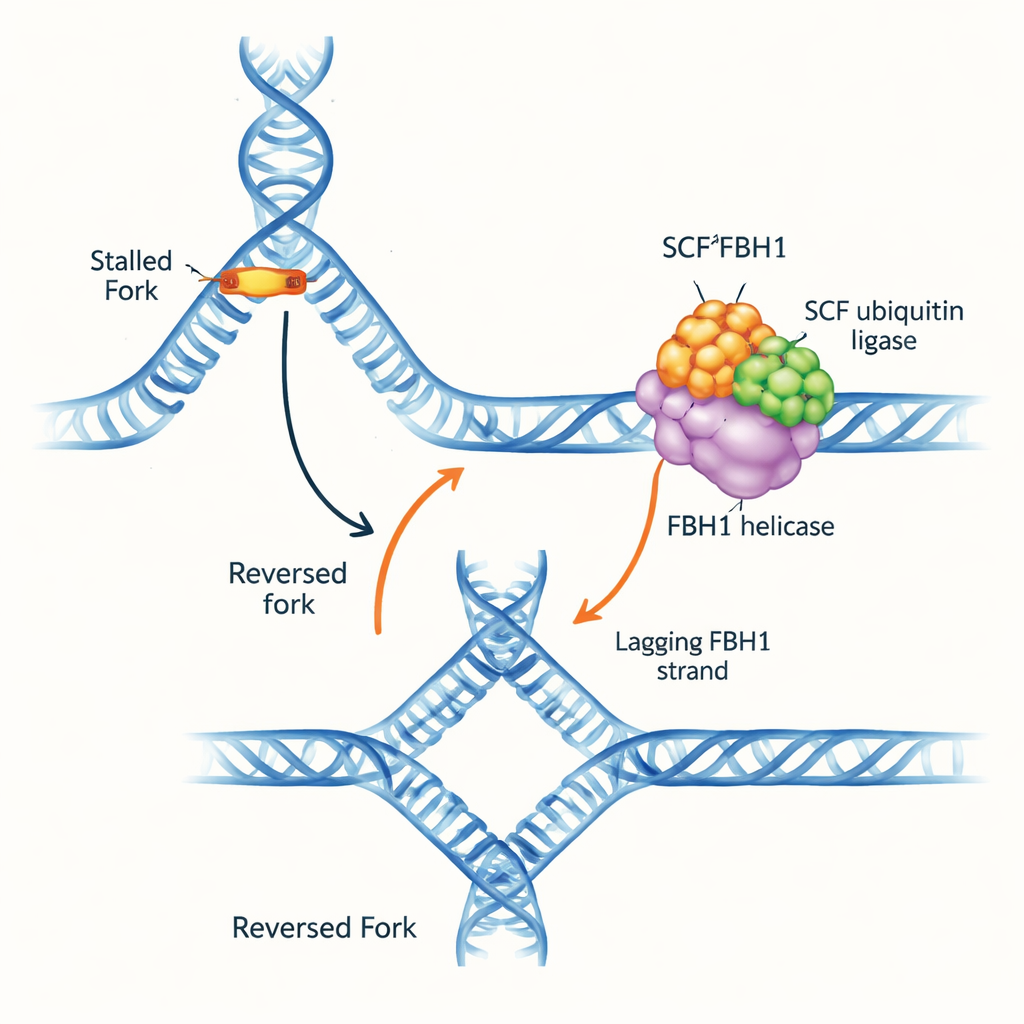
Un embouteillage sur l’autoroute de l’ADN
Les fourches de réplication sont des structures en Y où la double hélice est déroulée et copiée. Lorsqu’une fourche rencontre un obstacle, elle peut inverser sa progression : les brins parentaux se réapparient et les nouveaux brins se mettent en paire, formant une jonction d’ADN à quatre branches. Cette « inversion de fourche » permet de gagner du temps pour réparer et relancer la réplication en toute sécurité, mais mal gérée elle crée aussi un ADN fragile susceptible de se casser. Plusieurs moteurs moléculaires sont connus pour pousser les fourches en arrière en saisissant l’ADN double brin en avant de la fourche. FBH1 se distinguait toutefois par un comportement différent et est souvent altéré dans les tumeurs, ce qui suggère qu’il agit via une voie distincte et d’intérêt médical.
Un spécialiste des fourches avec un côté préféré
Les auteurs ont purifié le complexe humain SCFFBH1, qui associe l’hélicase FBH1 à un module d’ubiquitination (SCF). Ils ont d’abord cherché quelles formes d’ADN FBH1 préfère. À l’aide d’essais de liaison et de déroulement, ils montrent que SCFFBH1 favorise nettement des structures réellement en forme de fourche, en particulier lorsqu’il existe un court segment d’ADN simple brin sur le brin matrice « retardé » — le côté copié par petits fragments. Sur ces structures, FBH1 déroule l’ADN des centaines de fois plus vite que sur une simple extrémité libre, indiquant que l’engagement correct au niveau de la jonction de la fourche suralimente son activité motrice. Des pinces magnétiques à molécule unique ont confirmé que le complexe peut dérouler puis parcourir des milliers de bases sur de l’ADN simple brin sans se détacher, se comportant comme un moteur puissant et processif.
Inverser la fourche en tirant depuis l’arrière
Pour comprendre comment ce moteur inverse réellement les fourches, l’équipe a testé des substrats de fourche artificiels avec ou sans lacunes simple brin. Contrairement à d’autres remodelateurs de fourche, SCFFBH1 ne peut pas agir sur une fourche entièrement appariée ; il requiert une lacune sur le brin retardé et se déplace dans le sens 3′–5′ le long de ce brin simple. Ce mouvement de « tirage depuis l’arrière » force les brins parentaux à se réapparier tandis que l’enzyme reste verrouillée à la jonction de la fourche. Une structure obtenue par cryo‑microscopie électronique de SCFFBH1 lié à une fourche bloquée montre comment : un patch chargé positivement particulier, un « motif de liaison à la jonction » dans un sous‑domaine de FBH1, se loge précisément au point de branchement où les trois bras d’ADN se rencontrent. Lorsque les chercheurs ont muté deux acides aminés clés de ce motif, l’inversion de fourche a chuté d’environ 25 fois in vitro, alors que la machinerie de base de déroulement fonctionnait encore raisonnablement bien. Dans les cellules, la même mutation empêchait le ralentissement normal des fourches de réplication en réponse à un médicament induisant du stress, un signe caractéristique d’une inversion de fourche défaillante.
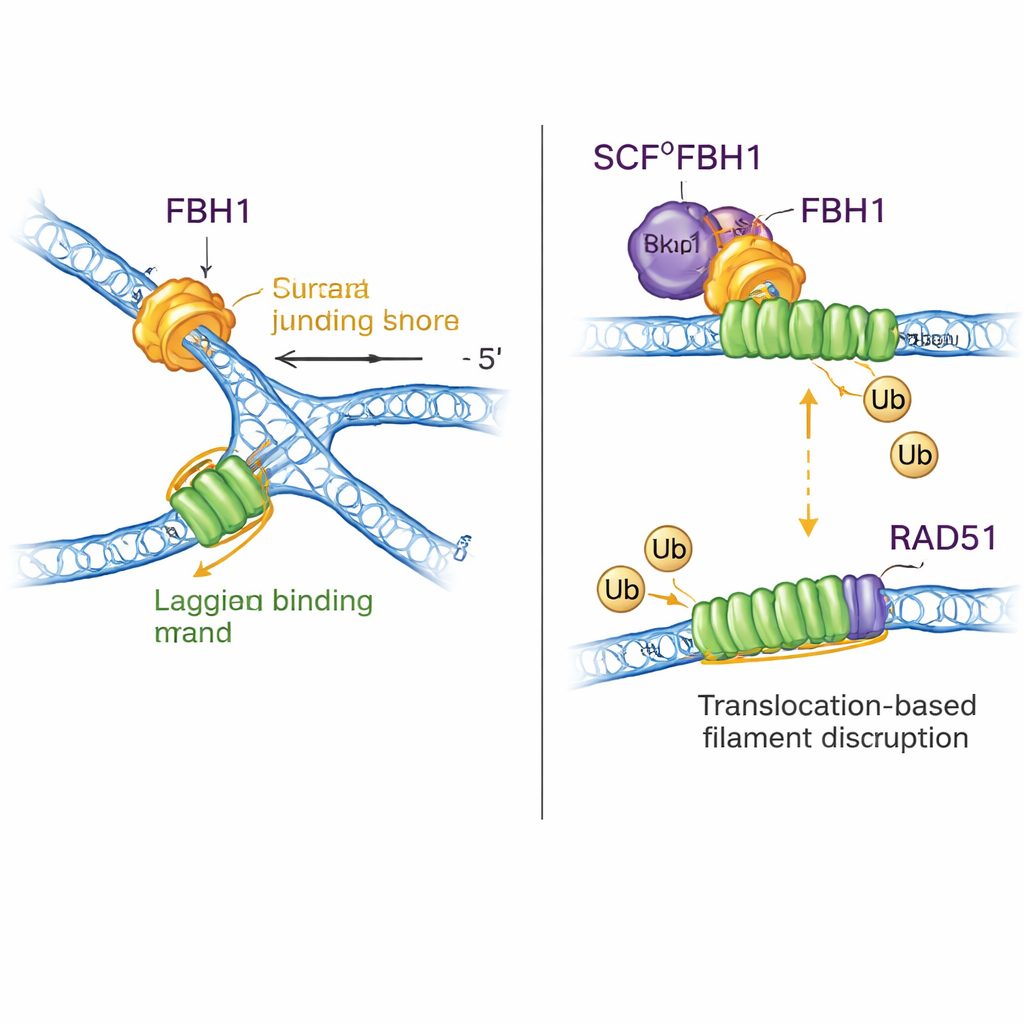
Un double rôle : remodeler l’ADN et éliminer RAD51
FBH1 n’est pas qu’un moteur ; via le complexe SCF il participe aussi à l’ajout de petites étiquettes ubiquitine sur des protéines. Les nouvelles structures assemblent quasiment l’ensemble du complexe SCFFBH1–ADN et montrent que la « tête » de transfert d’ubiquitine de la ligase se trouve à moins de 45 angströms du brin retardé sortant de FBH1. En intégrant des structures connues d’autres ligases d’ubiquitine, les auteurs proposent que cette géométrie place RAD51 — une enzyme qui forme des filamentssur l’ADN pour favoriser le recombinaison — directement dans l’axe d’action sur le brin retardé d’une fourche bloquée. Des travaux antérieurs montraient que FBH1 peut mécaniquement déloger RAD51 de l’ADN et aussi le marquer par ubiquitine pour empêcher sa réassociation rapide. Le nouveau modèle unifie ces idées : à mesure que FBH1 tire le long du brin retardé pour remodeler la fourche, le module SCF proche peut marquer les sous‑unités de RAD51, contribuant à démanteler ou à prévenir des filaments RAD51 excessifs qui pourraient autrement bloquer le traitement correct de la fourche.
Ce que cela signifie pour la stabilité du génome et le cancer
Pris ensemble, l’étude montre que SCFFBH1 inverse les fourches de réplication bloquées par un mécanisme distinct des autres remodelateurs connus : il saisit fermement le point de branchement tout en se déplaçant le long de la matrice retardée depuis l’arrière, favorisant le réappareillage sûr des brins parentaux sans former une jonction mobile à quatre branches de longue durée. Simultanément, sa ligase d’ubiquitine intégrée est idéalement positionnée pour retirer RAD51 du même brin, prévenant une recombinaison incontrôlée pendant le stress de réplication. Parce que FBH1 est fréquemment perdu ou muté dans les cancers, ces aperçus structuraux et mécanistiques aident à expliquer comment de telles tumeurs accumulent des dommages à l’ADN et pourquoi elles peuvent répondre différemment aux médicaments qui provoquent un stress de réplication ou ciblent des voies associées.
Citation: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Mots-clés: stress de réplication de l’ADN, inversion de fourche, hélicase FBH1, régulation de RAD51, stabilité du génome