Clear Sky Science · fr
Cartographie automatisée de la progression des fourches de réplication de l’ADN dans les cellules humaines avec ForkML
Pourquoi il est important de suivre la vitesse de copie de l’ADN
Chaque fois qu’une cellule humaine se divise, elle doit copier rapidement et fidèlement plus de trois milliards de « lettres » d’ADN. Si ce processus de copie ralentit ou s’arrête, le génome peut être endommagé, contribuant au cancer et à des troubles du développement. Pourtant, jusqu’à présent, les scientifiques ne disposaient pas d’un moyen simple de visualiser la vitesse à laquelle chaque « machine » de copie d’ADN progresse le long de segments précis du génome humain. Cet article présente ForkML, une nouvelle technique qui utilise le séquençage nanopore et l’apprentissage automatique pour automatiser cette tâche à une échelle sans précédent.
Observer les machines de copie de la cellule en action
L’ADN est dupliqué par de petites machines moléculaires appelées fourches de réplication qui se déplacent le long de la double hélice en synthétisant de nouveaux brins. ForkML permet aux chercheurs de « voir » indirectement ces fourches en incorporant un marqueur chimique inoffensif, la BrdU, dans l’ADN nouvellement synthétisé pendant deux très courtes impulsions séparées par un intervalle de temps fixe. Comme la BrdU est détectable dans des molécules d’ADN uniques par les séquenceurs nanopore, les scientifiques observent deux « bandes » marquées sur chaque brin d’ADN correspondant au passage d’une fourche pendant les deux impulsions. En mesurant la distance entre ces bandes et en la divisant par l’intervalle de temps connu, ils peuvent calculer la vitesse de chaque fourche dans cette région du génome. 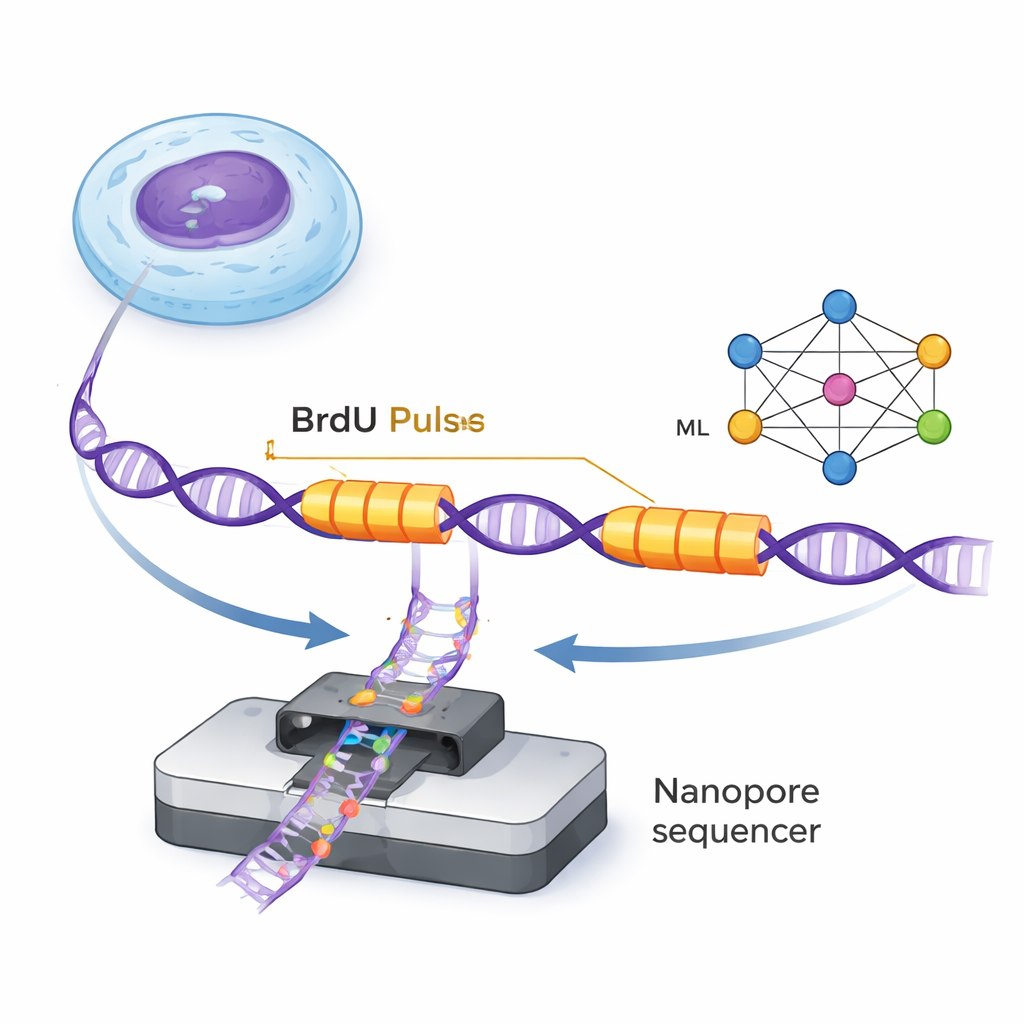
Apprendre à un ordinateur à lire les traces chimiques
Dans des travaux antérieurs sur la levure, les auteurs pouvaient repérer ces traces de BrdU à l’aide de règles simples, mais dans les cellules humaines les signaux sont plus faibles et plus complexes. Les experts humains reconnaissent encore le motif caractéristique — une montée nette de BrdU au début de l’impulsion, suivie d’une décroissance progressive lors du rinçage —, mais l’examiner manuellement sur des millions de fragments d’ADN est impossible. ForkML résout ce problème en entraînant un réseau de neurones, une forme d’apprentissage automatique, sur des milliers d’exemples annotés manuellement. Le modèle apprend à classer chaque segment d’ADN comme bruit de fond ou comme fourche se déplaçant vers la droite ou vers la gauche, et à repérer avec haute précision le début de chaque impulsion de BrdU. Cela permet la cartographie entièrement automatisée de milliers de vitesses de fourches individuelles à partir d’un seul run de séquençage.
Mesurer le stress et les différences le long du génome
En appliquant ForkML à une lignée de cellules cancéreuses du côlon humain, l’équipe a obtenu plus de 2 000 mesures de vitesse de fourche par expérience et a constaté qu’une fourche typique se déplace à environ 1,2 kilobase par minute, en accord avec des méthodes antérieures à plus faible débit. Lorsqu’ils ont traité les cellules avec des médicaments connus pour ralentir la réplication de l’ADN, ForkML a détecté clairement ce ralentissement, démontrant sa sensibilité à mesurer le stress de réplication. Parce que chaque fourche est cartographiée sur sa position dans le génome de référence, les auteurs ont pu associer la vitesse à d’autres caractéristiques, comme la période du cycle cellulaire où une région est normalement répliquée, la compaction de sa chromatine et son niveau d’activité en transcription. 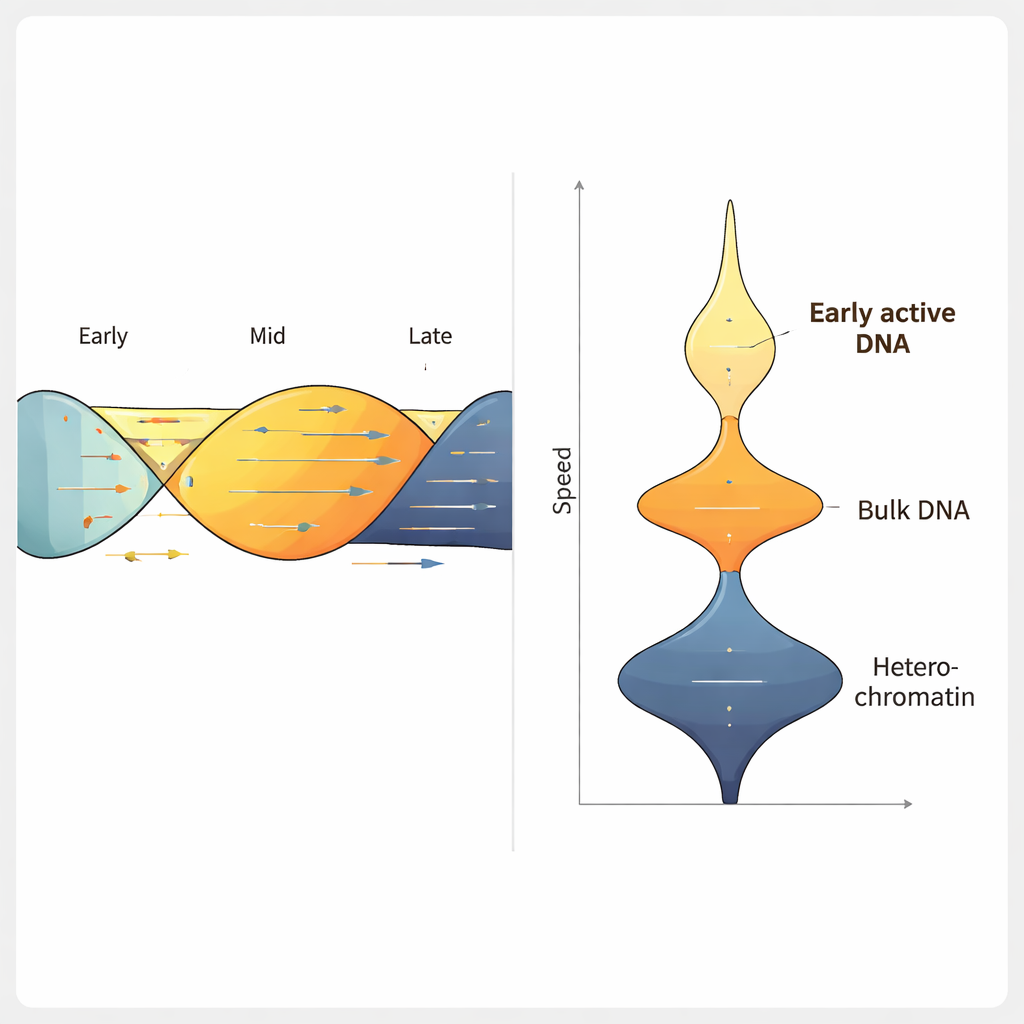
Révéler où commence la réplication et comment se différencient les brins
Au-delà de la vitesse, ForkML identifie également où la réplication de l’ADN commence et s’arrête, en repérant les points où les fourches divergent ou convergent sur une même molécule. En cartographiant plus de 20 000 sites d’initiation, les auteurs confirment que les cellules humaines adoptent une stratégie mixte : certaines répliques commencent dans des zones d’initiation bien définies, mais la plupart des départs sont dispersés à travers le génome. En combinant la direction des fourches avec l’information sur le brin d’ADN lu par le séquenceur, ForkML peut aussi distinguer les vitesses de synthèse du brin continu (leading) et du brin discontinu (lagging), ce que les tests basés sur les fibres traditionnelles ne permettent pas. Des essais sur six lignées cellulaires humaines différentes — normales et cancéreuses — montrent que les mêmes conditions simples de marquage à la BrdU fonctionnent de manière générale et fournissent des estimations de vitesse robustes dans chaque cas.
Une modernisation numérique d’une technique classique
Pour les non-spécialistes, ForkML peut être considéré comme une version moderne et numérique du classique test des fibres d’ADN : il utilise un schéma de marquage similaire, mais remplace la microscopie manuelle par du séquençage à lectures longues et de l’apprentissage automatique. Cela apporte un débit beaucoup plus élevé, le positionnement direct de chaque mesure sur le génome et des informations plus détaillées sur l’endroit et la vitesse de la copie de l’ADN. Parce que le protocole est simple, compatible avec le matériel nanopore actuel et adaptable à d’autres organismes, ForkML est en bonne position pour devenir un outil standard pour l’étude de la réplication de l’ADN. En termes pratiques, il offre aux chercheurs un moyen puissant de relier la vitesse locale de copie de l’ADN — normale ou soumise au stress — à l’activité des gènes, à l’état de la chromatine et aux altérations du génome liées aux maladies.
Citation: Rojat, V., Ciardo, D., Tourancheau, A. et al. Automated mapping of DNA replication fork progression in human cells with ForkML. Nat Commun 17, 1975 (2026). https://doi.org/10.1038/s41467-026-68750-4
Mots-clés: Réplication de l’ADN, vitesse des fourches de réplication, séquençage nanopore, marquage BrdU, apprentissage automatique en génomique