Clear Sky Science · fr
Une atlas protéogénomique de 1032 métastases cérébrales identifie des sous-types moléculaires, des paysages immunitaires et des vulnérabilités thérapeutiques
Pourquoi les cancers prennent racine dans le cerveau
À mesure que les soins contre le cancer s’améliorent, davantage de personnes vivent suffisamment longtemps pour que leurs tumeurs se propagent vers de nouveaux organes, y compris le cerveau. Ces métastases cérébrales sont désormais une complication fréquente et souvent dévastatrice ; pourtant, les médecins les traitent encore principalement en fonction du site d’origine — poumon, sein, peau, côlon — plutôt qu’en fonction de la manière dont le cancer s’est adapté à la vie dans le cerveau. Cette étude a construit un « atlas » détaillé de plus d’un millier de métastases cérébrales pour comprendre leur biologie cachée, comment elles interagissent avec les cellules et le système immunitaire du cerveau, et où pourraient se trouver de nouvelles opportunités thérapeutiques.
Construire une carte géante des tumeurs cérébrales
Les chercheurs ont réuni des données provenant de 1 032 métastases cérébrales issues de différents cancers primaires, ainsi que des dizaines de tumeurs primaires correspondantes et quelques tumeurs cérébrales primaires agressives pour comparaison. Ils ont combiné plusieurs approches de pointe : séquençage de l’ADN et de l’ARN, mesures à grande échelle des protéines et des métabolites, cartographies unicellulaires et spatiales des cellules tumorales et immunitaires, et organoïdes dérivés de patients cultivés en laboratoire. En intégrant tous ces niveaux, l’objectif n’était pas seulement d’énumérer des gènes, mais de voir comment des systèmes biologiques entiers se comportent à l’intérieur des métastases cérébrales.
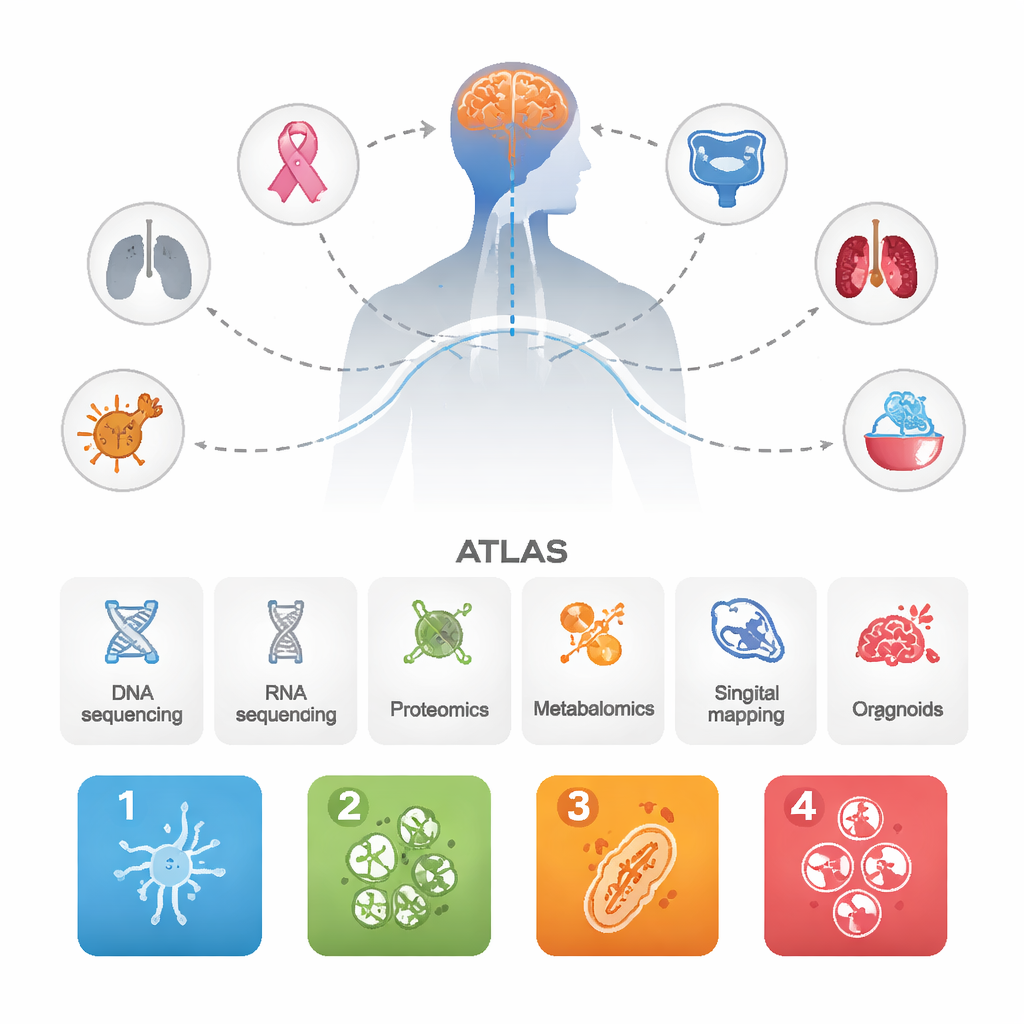
Quatre « personnalités » récurrentes des métastases cérébrales
Malgré leurs origines variées, les métastases cérébrales se regroupent de façon répétée en quatre principaux sous‑types moléculaires. Le premier, nommé BrMS1, apparaît « de type neural » : les cellules tumorales et les tissus environnants expriment de nombreux programmes propres au cerveau et aux neurones, et montrent une surveillance immunitaire relativement active. BrMS2 est « infiltré par le système immunitaire » : il regorge de cellules immunitaires, en particulier de lymphocytes T, et présente un programme connu sous le nom de transition épithélio‑mésenchymateuse (EMT), qui relâche les attachements cellulaires et remodèle l’environnement local. BrMS3 est « métabolique », dominé par des cellules tumorales très actives qui réorganisent leur utilisation de l’énergie — utilisant des voies telles que le métabolisme des acides gras et la phosphorylation oxydative. BrMS4 est « prolifératif », caractérisé par une division cellulaire rapide, des traits proches des cellules souches et une instabilité génomique élevée, mais de manière remarquable avec peu de cellules immunitaires.
Ce que révèle l’environnement tumoral
En observant à l’échelle unicellulaire et spatiale, l’équipe a montré que chaque sous‑type occupe un quartier distinct au sein du cerveau. Les lésions BrMS1 sont riches en cellules de soutien cérébral telles que les astrocytes et les neurones, suggérant que la tumeur imite et détourne étroitement le tissu cérébral normal. Les tumeurs BrMS2, au contraire, sont parsemées d’amas denses de lymphocytes T, dont de nombreux T « épuisés » exprimant des molécules de point de contrôle comme PD‑1, et présentent des vaisseaux activés et des signaux inflammatoires. Les lésions BrMS3 se situent dans des zones métaboliquement actives, tandis que les lésions BrMS4 forment des îlots de cellules en division rapide entourés d’un territoire relativement pauvre en cellules immunitaires. De façon générale, l’étude a constaté que, dans les métastases cérébrales — mais pas dans les tumeurs primaires — une forte activation de la transition épithélio‑mésenchymateuse s’accompagne souvent d’une infiltration accrue de lymphocytes T, ce qui suggère que ce programme pourrait aider à ouvrir la voie à l’entrée des cellules immunitaires.
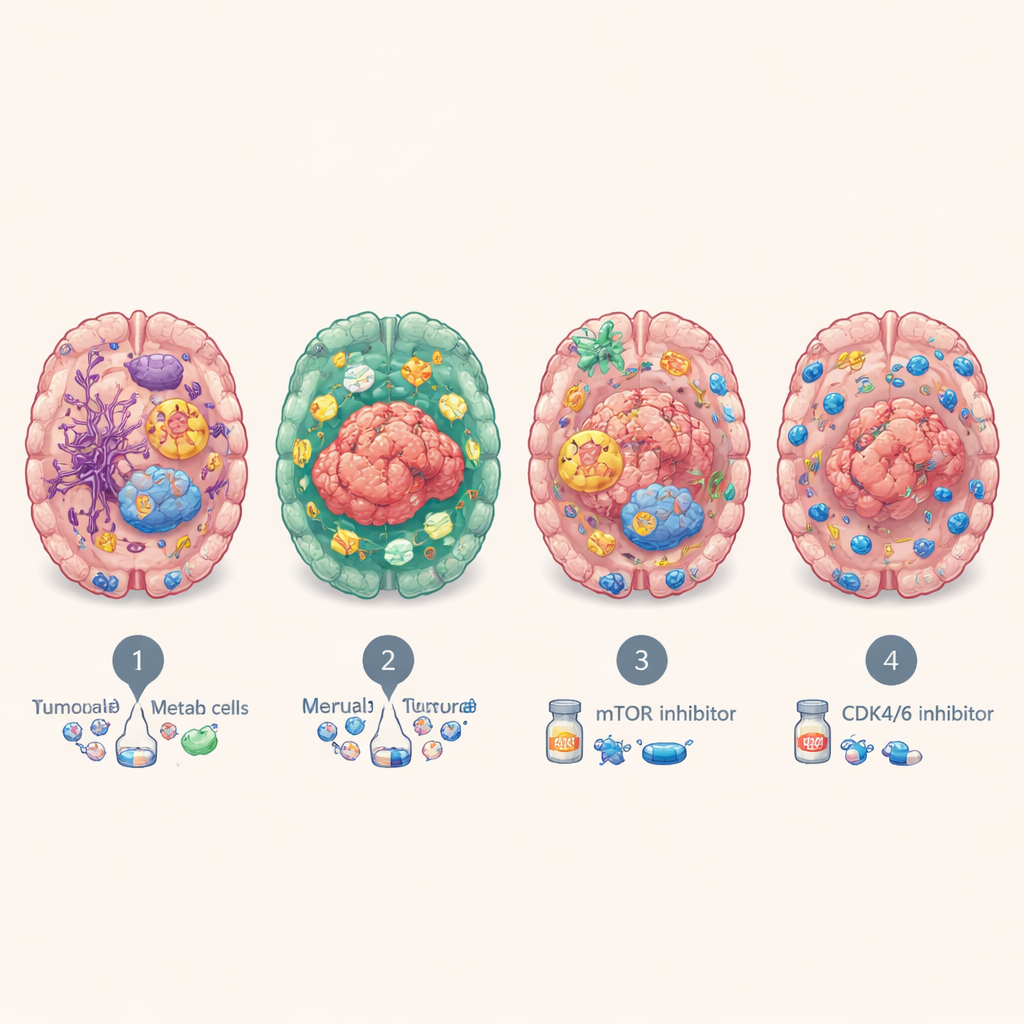
Indices pour le traitement et l’évolution des patients
Ces « personnalités » moléculaires n’étaient pas purement théoriques. Les patients dont les métastases étaient du sous‑type immuno‑infiltré BrMS2 avaient tendance à vivre plus longtemps que ceux ayant des tumeurs du sous‑type prolifératif BrMS4, qui présentait systématiquement les pires pronostics. En testant des médicaments sur des organoïdes dérivés de patients, l’équipe a constaté que les tumeurs métaboliques BrMS3 étaient particulièrement sensibles au blocage de la voie de signalisation mTOR, qui régule la croissance cellulaire et le métabolisme, et que les tumeurs BrMS4 à division rapide étaient plus vulnérables aux inhibiteurs de CDK4/6, des médicaments qui ralentissent le cycle cellulaire. Des analyses séparées suggèrent que les tumeurs BrMS1 pourraient mieux répondre à la radiothérapie, tandis que l’environnement inflammatoire et riche en points de contrôle de BrMS2 pourrait favoriser une réponse aux immunothérapies visant à réactiver les lymphocytes T épuisés — ce qui nécessite toutefois confirmation chez des patients porteurs de métastases cérébrales.
Ce que cela signifie pour les personnes atteintes de métastases cérébrales
Cet atlas montre qu’une fois que les cellules cancéreuses atteignent le cerveau, elles tendent à converger vers quelques états biologiques partagés, indépendamment de leur origine. Savoir si la métastase cérébrale d’un patient est de type neural, riche en immunité, métabolique ou fortement proliférative pourrait à terme orienter des traitements plus personnalisés — par exemple en choisissant entre radiothérapie, immunothérapie ou médicaments ciblant le métabolisme ou la division cellulaire. Bien que ces résultats ne modifient pas encore la prise en charge standard, ils fournissent une feuille de route détaillée pour la recherche et les essais cliniques futurs visant à transformer ces vulnérabilités moléculaires en thérapies plus précises et efficaces pour les patients atteints de métastases cérébrales.
Citation: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Mots-clés: métastase cérébrale, sous-types tumoraux, immunothérapie contre le cancer, métabolisme du cancer