Clear Sky Science · fr
La composition en phospholipides influence fortement l’assemblage des protéines en baril β dans des membranes externes bactériennes purifiées
Pourquoi les enveloppes bactériennes comptent
Les « super‑bactéries » résistantes aux médicaments représentent une menace croissante parce que de nombreux antibiotiques ne parviennent tout simplement pas à franchir leurs défenses externes robustes. Cette étude examine de près un élément clé de cette défense chez les bactéries à Gram négatif comme E. coli : une couche externe protectrice remplie de protéines en forme de baril et de lipides spécialisés. En analysant comment le mélange de ces lipides contrôle la construction de la couche externe, les auteurs mettent en lumière des points faibles qui pourraient être exploités pour concevoir de futurs antibiotiques.
Le bouclier à double paroi
Les bactéries à Gram négatif sont particulières en ce qu’elles possèdent deux membranes. La membrane interne gère les fonctions cellulaires courantes, tandis que la membrane externe agit comme un imperméable robuste qui empêche de nombreux toxines et antibiotiques d’entrer. Cette couche externe est composée de deux types de lipides : des phospholipides courants du côté interne et un lipide sucre‑gras rigide appelé lipopolysaccharide (LPS) du côté externe. Traversant cette enveloppe se trouvent de nombreuses protéines « β‑baril »—des cylindres creux qui forment des pores et des portes pour les nutriments. Une machine moléculaire appelée BAM (pour barrel assembly machine) est responsable du repliement de ces protéines et de leur insertion dans la membrane externe.
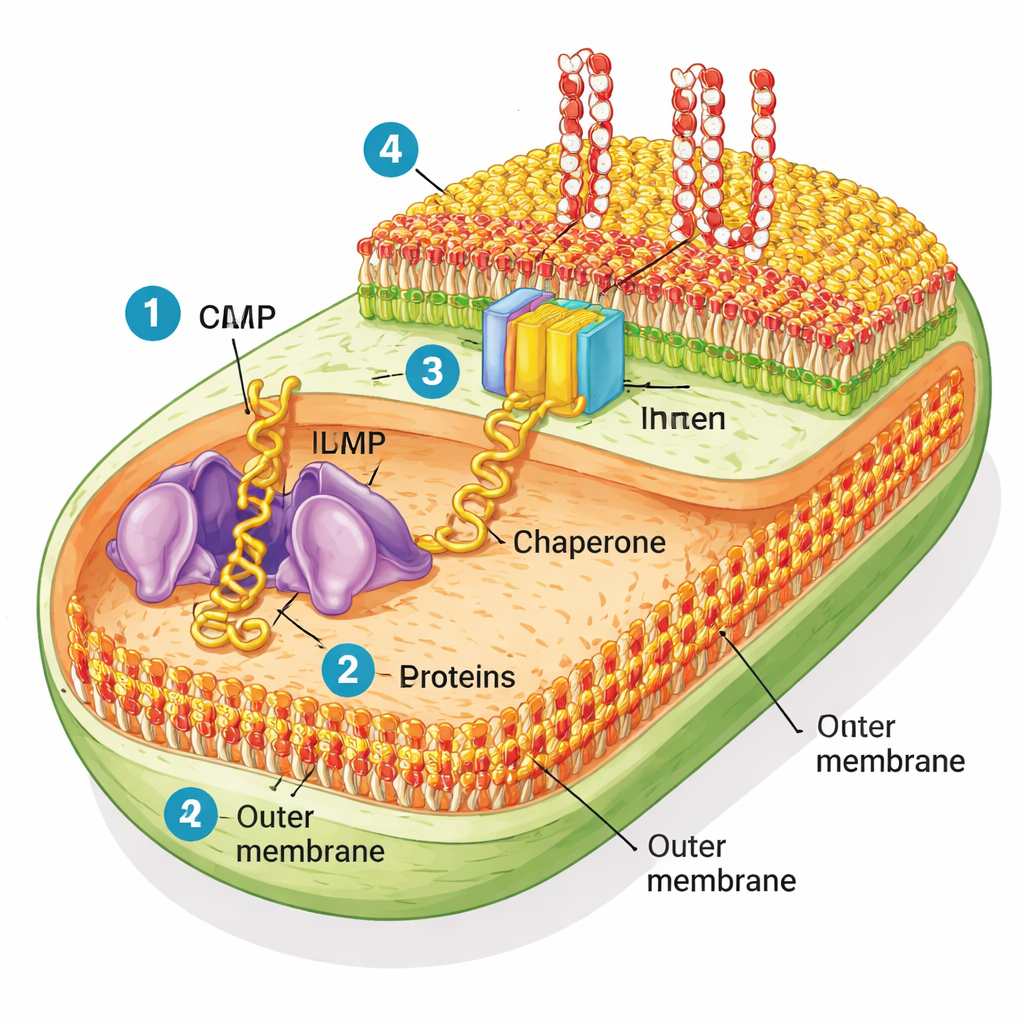
Recréer la couche bactérienne en éprouvette
Pour évaluer l’efficacité de BAM dans un contexte réaliste, les chercheurs ont purifié des fragments de la membrane externe d’E. coli, créant de petites bulles qu’ils appellent « OM natives ». Contrairement aux membranes artificielles simples utilisées dans de nombreuses études en laboratoire, ces membranes natives conservent leur mélange complet de protéines et de lipides. L’équipe a ensuite utilisé une usine protéique sans cellules pour fabriquer de nouvelles protéines de la membrane externe à partir de zéro et a observé si BAM présent dans ces bulles natives pouvait les replier et les insérer. Ils se sont concentrés sur une protéine modèle en β‑baril appelée EspP, ainsi que quelques autres. En présence de la protéine chaperonne SurA, BAM dans les membranes natives repliait efficacement EspP, et ce processus était bloqué par un antibiotique connu ciblant BAM, la darobactine — une preuve claire que la machinerie naturelle restait active.
Quand le mélange de lipides se dérègle
Les auteurs se sont ensuite demandé ce qui se passe lorsque l’équilibre lipidique de la membrane externe est perturbé. Ils ont étudié des souches mutantes d’E. coli dépourvues de systèmes clés qui corrigent normalement les phospholipides mal placés dans la couche externe. Un système, MlaA, ramène les phospholipides égarés vers la membrane interne ; un autre, l’enzyme PldA, les découpe. En utilisant des membranes natives issues de ces mutants, l’équipe a constaté que l’assemblage d’EspP dépendant de BAM diminuait nettement dans les souches sans MlaA et était gravement compromis en l’absence de PldA. Ces effets ne résultaient pas d’une perte de BAM lui‑même ou d’autres protéines majeures, qui étaient toujours présentes à des niveaux normaux, ce qui pointe plutôt vers l’environnement lipidique altéré comme cause.
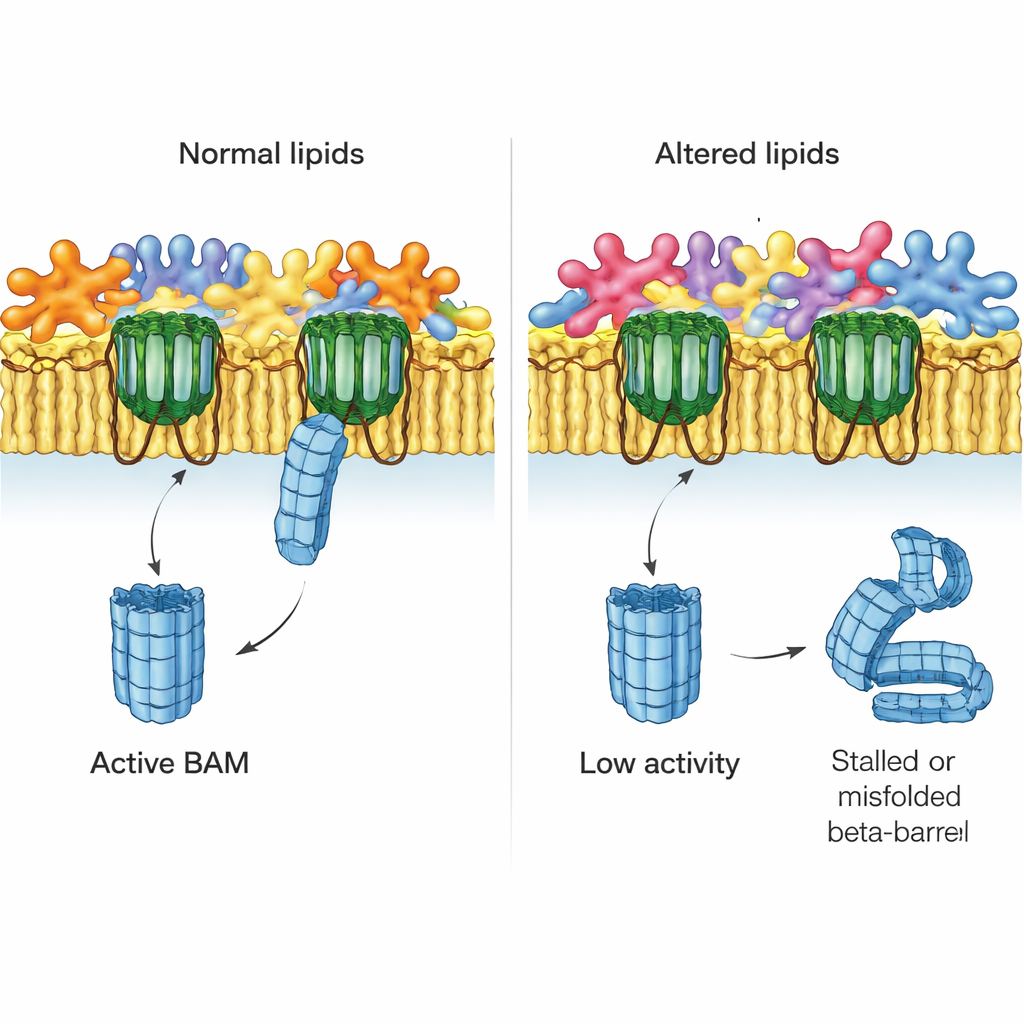
Cartographier le paysage lipidique en détail
Pour relier la fonction à la chimie, les chercheurs ont développé une méthode sensible de spectrométrie de masse pour inventorier des centaines de phospholipides individuels dans des cellules entières et dans des membranes externes purifiées. Chez E. coli normal, ils ont confirmé qu’un type de lipide (la phosphatidyléthanolamine, ou PE) est enrichi dans la membrane externe, tandis que d’autres (la phosphatidylglycérol et la cardiolipine) y sont relativement appauvris. Ils ont également trouvé que les « lyso‑lipides », qui n’ont qu’une seule queue grasse et tendent à courber les membranes, sont étonnamment concentrés dans la membrane externe. Dans les souches mutantes, en particulier celles dépourvues de PldA, ces profils étaient brouillés : les différences habituelles entre membrane interne et externe s’atténuaient voire s’inversaient, et la longueur et le type des queues grasses changeaient. Les souches présentant les profils lipidiques les plus perturbés étaient les mêmes où BAM fonctionnait le moins bien.
Implications pour les stratégies antibiotiques
Pris ensemble, ces travaux montrent que la membrane externe n’est pas seulement un échafaudage passif pour les protéines. Sa composition précise en phospholipides influence fortement la capacité de BAM à construire les pores en β‑baril essentiels à la survie bactérienne. Lorsque l’équilibre lipidique est perturbé, moins de complexes BAM fonctionnent correctement, et certains fonctionnent plus lentement. Bien que les bactéries vivantes puissent compenser de telles modifications de façons qu’un système en éprouvette ne reproduit pas, cette étude souligne comment régler ou perturber des lipides spécifiques pourrait affaiblir la couche externe. Cette piste ouvre de nouvelles possibilités pour des médicaments qui ciblent soit directement BAM, soit déséquilibrent subtilement les lipides de la membrane externe, rendant même les bactéries à Gram négatif les plus résistantes plus vulnérables.
Citation: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
Mots-clés: Bactéries à Gram négatif, protéines de la membrane externe, assemblage des β-barils, lipides bactériens, résistance aux antibiotiques