Clear Sky Science · fr
La kynurénine médie la toxicité intestinale induite par la chimiothérapie via la modulation du microbiote intestinal
Pourquoi cela importe pour les personnes sous chimiothérapie
La chimiothérapie sauve des vies, mais elle s’accompagne souvent d’effets secondaires pénibles au niveau intestinal — douleurs, diarrhée, perte de poids — qui peuvent contraindre les médecins à réduire les doses ou à interrompre le traitement prématurément. Cette étude met au jour une chaîne de réactions cachée entre une molécule circulante, des cellules immunitaires et les microbes intestinaux, qui aide à expliquer pourquoi un médicament anticancéreux courant, l’oxaliplatine, peut être si agressif pour les intestins, et indique de nouvelles pistes pour protéger les patients sans affaiblir leur traitement anticancéreux.
Un lien chimique entre le traitement et les lésions intestinales
Les chercheurs ont commencé par des patients atteints de cancer colorectal recevant une chimiothérapie à base d’oxaliplatine. Ils ont comparé des prélèvements sanguins de personnes ayant développé des effets intestinaux sévères à ceux de personnes ayant mieux toléré le traitement. Par profilage ciblé des métabolites, ils ont trouvé que plusieurs produits de dégradation de l’acide aminé tryptophane étaient plus élevés dans le groupe à forte toxicité, une molécule — la L‑kynurénine — se distinguant comme la plus fortement augmentée. Les patients présentant davantage de L‑kynurénine dans le sang montraient aussi plus de signes d’inflammation et des chiffres de globules blancs plus bas, suggérant que cette molécule pourrait être directement liée aux dommages induits par le traitement.
Établir la causalité chez la souris
Pour aller au‑delà de la corrélation, l’équipe s’est tournée vers des modèles murins. Lorsque des souris saines ont reçu des doses élevées d’oxaliplatine, elles ont développé des signes classiques de lésion intestinale : perte de poids, côlons raccourcis, épaississement de la paroi intestinale, diminution des cellules en division et augmentation des cellules mourantes dans l’épithélium intestinal. Ces souris présentaient aussi une forte augmentation de la L‑kynurénine dans le sang, en écho aux données humaines. Quand les chercheurs ont administré de la L‑kynurénine supplémentaire aux souris traitées par l’oxaliplatine, les lésions intestinales se sont aggravées — alors que l’efficacité du médicament contre les tumeurs restait intacte. À l’inverse, lorsque l’enzyme IDO1, qui convertit le tryptophane en L‑kynurénine, a été supprimée ou bloquée, les souris étaient beaucoup plus résistantes à la toxicité intestinale tout en bénéficiant toujours de la chimiothérapie.
Cellules immunitaires et microbes intestinaux pris entre deux feux
En approfondissant, les scientifiques ont cherché quelles cellules produisaient l’excès de L‑kynurénine pendant le traitement. Ils ont découvert que l’oxaliplatine stimule certaines cellules immunitaires (lymphocytes T CD8) à libérer la protéine de signalisation interféron‑gamma, qui active ensuite IDO1 dans des cellules myéloïdes voisines — une classe de globules blancs. Des souris génétiquement modifiées pour ne pas exprimer IDO1 dans leurs seules cellules myéloïdes produisaient beaucoup moins de L‑kynurénine et étaient protégées des lésions intestinales, tandis que la suppression d’IDO1 uniquement dans les cellules de la muqueuse intestinale avait peu d’effet. Parallèlement, la composition du microbiote intestinal se modifiait. Chez les souris normales, l’oxaliplatine et des niveaux élevés de L‑kynurénine étaient associés à la perte d’une bactérie bénéfique, Lactobacillus johnsonii. En revanche, les souris avec moins de L‑kynurénine conservaient des niveaux plus élevés de L. johnsonii. Lorsque les bactéries intestinales étaient éliminées par des antibiotiques, l’effet protecteur d’un faible taux de L‑kynurénine disparaissait, et lorsque le microbiote de souris à faible kynurénine était transplanté à des souris normales, ces receveuses devenaient plus résilientes aux lésions intestinales induites par l’oxaliplatine.
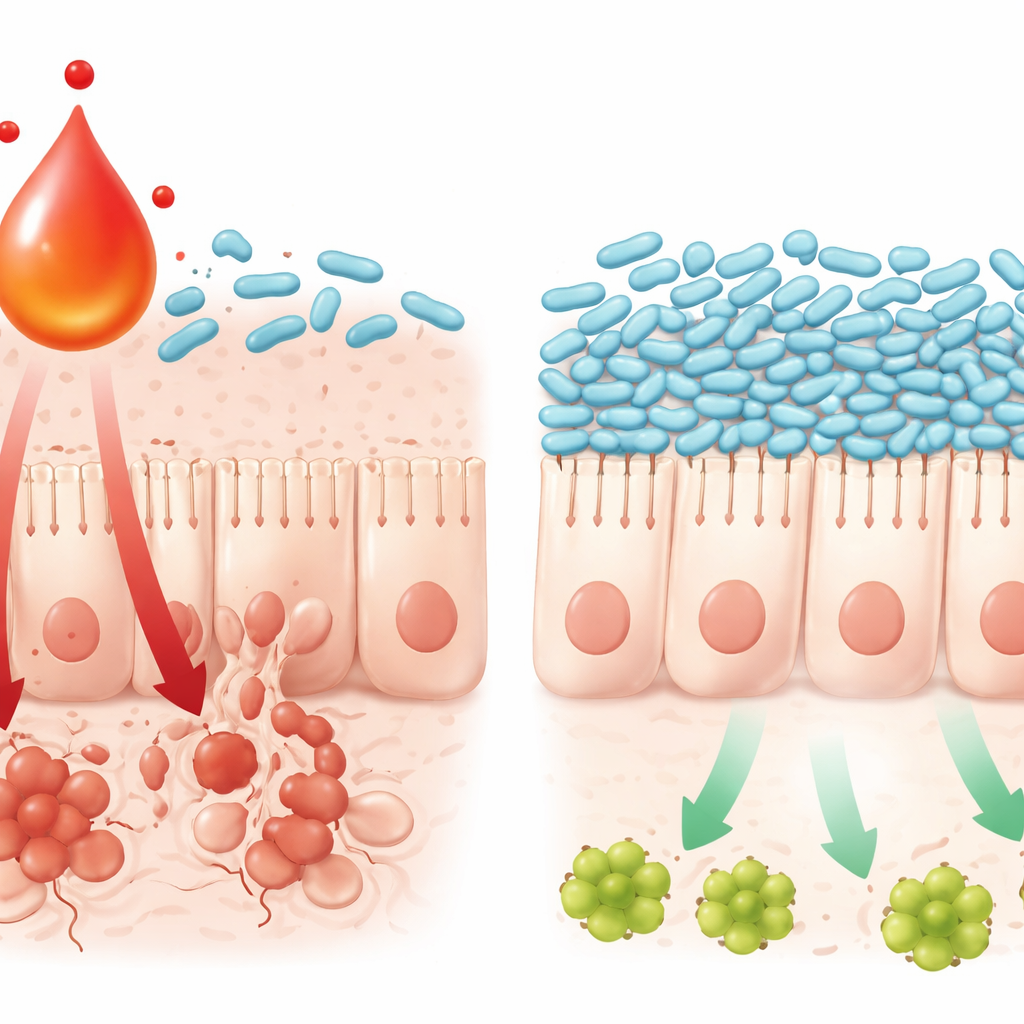
Comment un métabolite provoque la mort cellulaire dans l’intestin
L’étude a aussi retracé comment cette interaction chimie–microbes blesse la muqueuse intestinale. Des niveaux élevés de L‑kynurénine étaient associés à une activité accrue d’une voie inflammatoire bien connue dans le tissu intestinal, la voie TNFα/JNK, qui pousse les cellules vers la mort programmée. En culture cellulaire, la combinaison d’oxaliplatine et de L‑kynurénine rendait les cellules intestinales plus susceptibles d’activer cette voie et de mourir, tandis que l’ajout de L. johnsonii atténuait le signal et préservait la survie cellulaire. La L‑kynurénine elle‑même pouvait ralentir la croissance et compromettre les mécanismes de survie de L. johnsonii en boîtes de Pétri, ce qui aide à expliquer pourquoi la bactérie disparaît lorsque le métabolite s’accumule. Ensemble, ces résultats décrivent une boucle auto‑entretenue : la chimiothérapie déclenche un signal immunitaire, les cellules immunitaires augmentent la L‑kynurénine, cela perturbe les bactéries amies comme L. johnsonii, et la communauté microbienne altérée amplifie à son tour des signaux inflammatoires qui tuent les cellules intestinales.
Nouvelles façons de protéger les patients pendant le traitement
De manière encourageante, le travail pointe aussi vers des stratégies pratiques. Traiter les souris avec un médicament appelé épacadostat, qui inhibe IDO1, a réduit les niveaux de L‑kynurénine et nettement atténué les lésions intestinales induites par l’oxaliplatine sans diminuer le contrôle tumoral. Dans une approche complémentaire, l’équipe a conçu une souche inoffensive d’E. coli capable de surproduire une enzyme qui dégrade la L‑kynurénine dans l’intestin. Les souris recevant ces bactéries modifiées étaient elles aussi protégées de la toxicité intestinale, là encore sans compromettre les effets anticancéreux de la chimiothérapie. La supplémentation en L. johnsonii elle‑même a également atténué les symptômes et préservé la structure intestinale.
Ce que cela signifie pour les personnes atteintes de cancer
Pris dans leur ensemble, ces travaux montrent qu’un seul métabolite induit par le traitement — la L‑kynurénine — joue le rôle d’intermédiaire central entre la chimiothérapie, le système immunitaire, les microbes intestinaux et les lésions intestinales. En démontrant que bloquer sa production, favoriser sa dégradation ou restaurer des bactéries protectrices peut tous atténuer les effets de la chimiothérapie sur l’intestin, la recherche ouvre la voie à des thérapies complémentaires qui permettraient aux patients de rester plus forts et plus à l’aise pendant leur combat contre le cancer.
Citation: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Mots-clés: effets secondaires de la chimiothérapie, microbiome intestinal, métabolisme du tryptophane, L-kynurénine, cancer colorectal