Clear Sky Science · fr
Réduction électrochimique du CO2 au niveau de l’ampère vers des oxygénés multi‑carbonés en électrolyte acide via la reconstruction du microenvironnement de surface
Transformer un problème climatique en liquides utiles
Le dioxyde de carbone issu de la combustion des combustibles fossiles réchauffe notre planète, mais il représente aussi une matière première potentielle. Cette étude explore comment convertir le CO2 en produits chimiques liquides de valeur, tels que l’éthanol et l’acide acétique, à l’aide de l’électricité. Les chercheurs montrent qu’en redesignant soigneusement l’environnement immédiat d’une électrode de cuivre, ils peuvent rendre cette transformation plus rapide, plus efficace et compatible avec des conditions acides sévères qui sabotent généralement ces réactions.
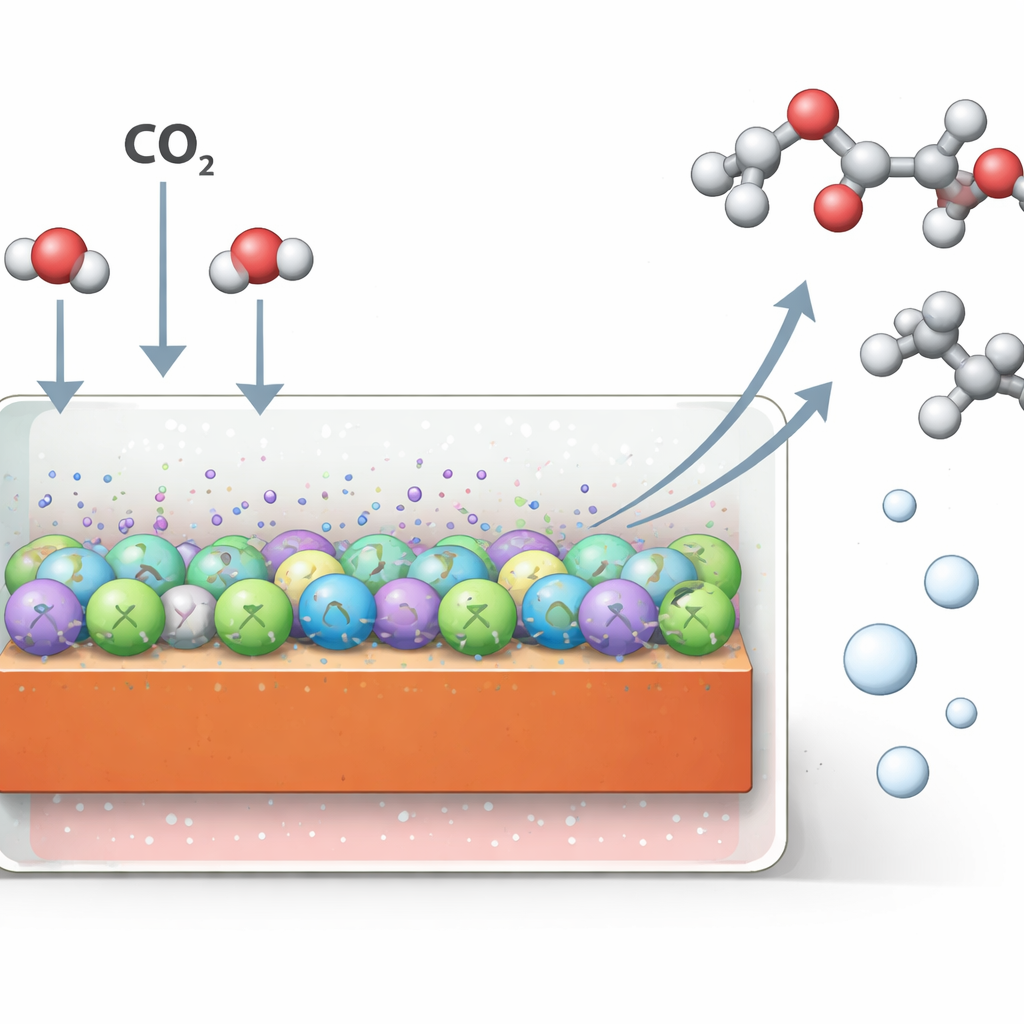
Pourquoi il est difficile de fabriquer des carburants liquides à partir du CO2
Les scientifiques rêvent depuis longtemps d’utiliser l’électricité renouvelable excédentaire pour convertir le CO2 en produits riches en énergie, stockant le soleil et le vent sous forme chimique. Le cuivre est l’un des rares matériaux capables d’assembler le CO2 en molécules à plusieurs atomes de carbone, y compris des alcools et des acides déjà employés par l’industrie. Jusqu’à présent, la plupart des progrès ont eu lieu en milieux alcalins (basiques), qui entraînent la formation de carbonates invisibles et le colmatage des dispositifs par des sels, gaspillant ainsi le CO2. Les électrolytes acides évitent ces problèmes, mais dans ces conditions le cuivre a tendance à retirer l’oxygène des intermédiaires prometteurs, favorisant des gaz simples comme l’éthylène et l’hydrogène plutôt que des liquides oxygénés.
Concevoir une surface de cuivre plus intelligente
Pour surmonter ce compromis, l’équipe a créé une électrode de cuivre modifiée qu’ils nomment IL@Cu. Ils l’ont obtenue en réduisant de l’oxyde de cuivre dans une solution aqueuse contenant un liquide ionique spécialement choisi, un sel liquide proche de la température ambiante. Les composants chargés positivement de ce liquide ionique, basés sur une molécule appelée Bmim, s’attachent uniformément à de minuscules nanoparticules de cuivre, conférant à la surface une légère charge positive. Des microscopies avancées et des techniques aux rayons X ont confirmé que le cuivre sous‑jacent reste métallique tandis que le liquide ionique forme une fine couche bien ancrée qui modifie la façon dont les autres ions et l’eau se disposent à l’interface où le CO2 est converti.
Porter les performances au niveau industriel
Lorsque les chercheurs ont testé IL@Cu dans une solution acide de sulfate de potassium en écoulement, ils ont atteint des courants électriques très élevés — jusqu’à deux ampères par centimètre carré, comparables à l’électrolyse industrielle. Dans ces conditions exigeantes, le cuivre modifié a produit des produits multi‑carbonés avec une efficacité faradique d’environ 83 %, ce qui signifie que la majorité des électrons ont servi à fabriquer les molécules désirées plutôt qu’à des réactions secondaires inutiles. Encore plus impressionnant : environ 60 % du courant a été dédié spécifiquement à des produits liquides contenant de l’oxygène, l’éthanol représentant à lui seul près de la moitié de cette fraction. L’appareil a également utilisé le CO2 entrant de façon très efficace : presque quatre cinquièmes du gaz traversant le dispositif ont été convertis en un seul passage, et le catalyseur a conservé son activité et sa structure pendant plus de 100 heures de fonctionnement.
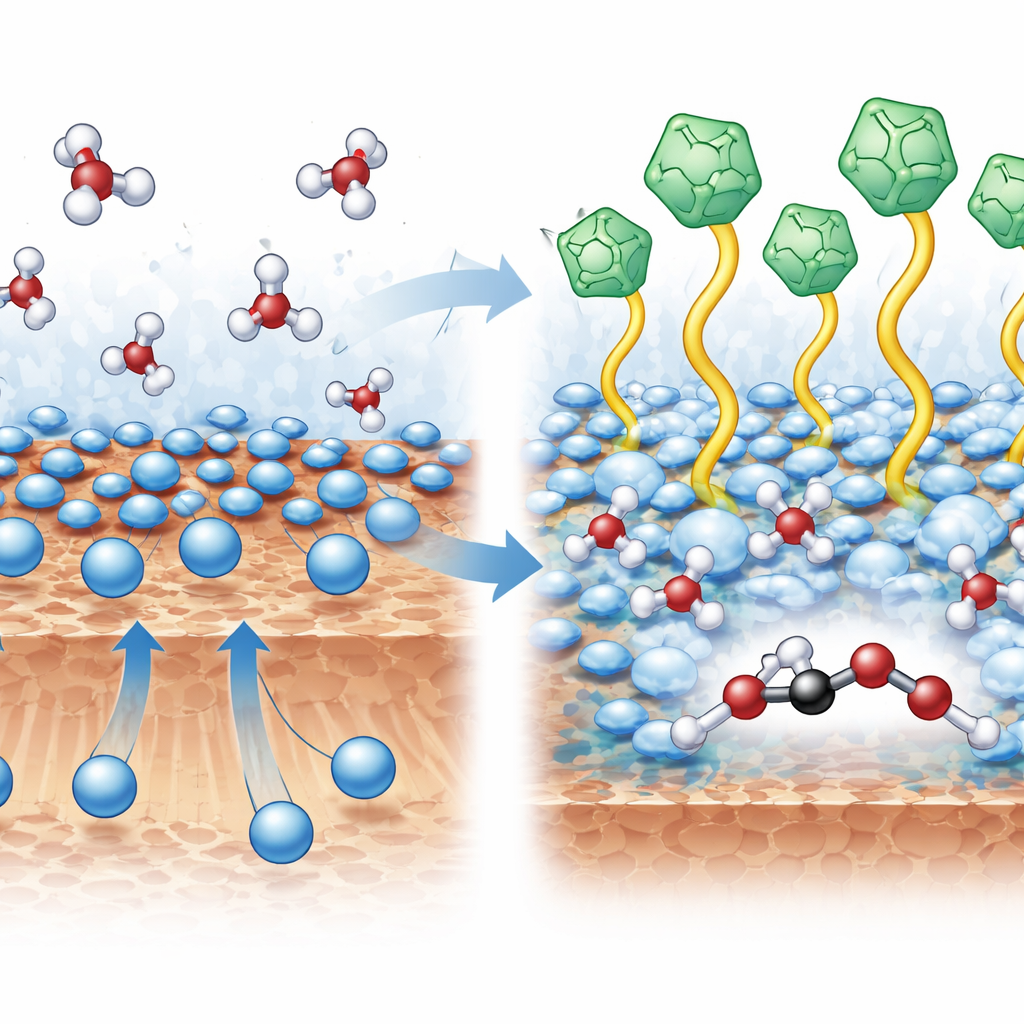
Réorganiser l’eau et les ions à la surface
Le cœur de l’avancée réside dans l’agencement microscopique des ions et de l’eau là où la réaction a lieu. Des mesures spectroscopiques et des simulations informatiques ont révélé que les cations du liquide ionique repoussent les ions potassium à proximité de la surface de cuivre. Cela crée de l’espace pour que les molécules d’eau s’approchent davantage et forment un réseau de liaisons hydrogène plus connecté autour d’intermédiaires clés à deux carbones. Avec le potassium maintenu à une distance optimale, les fragments contenant du carbone peuvent plus facilement se coupler entre eux plutôt que de se détacher sous forme de monoxyde de carbone. Parallèlement, le réseau d’eau environnant aide à préserver l’oxygène dans les molécules en croissance au lieu de permettre la rupture des liaisons et la libération d’éthylène gazeux. Des calculs en mécanique quantique ont montré que cet environnement réorganisé abaisse la barrière énergétique pour la formation de la liaison carbone–carbone et oriente la voie réactionnelle vers des liquides riches en oxygène comme l’éthanol.
Ingénierie de la couche invisible qui compte
En substance, l’étude démontre que contrôler le « microenvironnement » — l’agencement à l’échelle nanométrique des ions et de l’eau à une électrode — peut être tout aussi important que le choix du métal. En fixant des molécules de liquide ionique au cuivre, les auteurs augmentent simultanément le taux de conversion du CO2, favorisent des produits multi‑carbonés plus faciles à stocker et transporter, et maintiennent la stabilité de l’appareil en solutions acides plus pratiques pour une exploitation à long terme. Cette stratégie de redesign de la mince couche invisible où se déroulent les réactions pourrait orienter le développement de systèmes de nouvelle génération capables de transformer le CO2 résiduel en produits chimiques et carburants utiles à des échelles pertinentes pour atténuer le changement climatique.
Citation: Yin, Y., Ling, Z., Liu, S. et al. Ampere-level CO2 electroreduction to multi-carbon oxygenates in acidic electrolyte through surface microenvironment reconstruction. Nat Commun 17, 2353 (2026). https://doi.org/10.1038/s41467-026-68739-z
Mots-clés: réduction électrochimique du CO2, catalyseur cuivre, liquides ioniques, production d’éthanol, recyclage électrochimique du CO2