Clear Sky Science · fr
Contrôler l’écoulement de l’électrolyte augmente l’efficacité de l’électrosynthèse continue d’oxime au‑delà de 95 %
Verdir les précurseurs du plastique
Le nylon‑6 est omniprésent dans notre quotidien, des vêtements et moquettes aux pièces automobiles. Pourtant, l’un de ses ingrédients clés, l’oxime du cyclohexanone, est généralement produit par des procédés reposant sur des combustibles fossiles et générant des sous‑produits dangereux. Cette étude explore comment remplacer ces filières par un procédé électrochimique continu, consommant moins de matières et atteignant une très haute efficacité, ouvrant la voie à une production plus propre des plastiques de tous les jours.
Pourquoi les molécules de base du nylon posent problème
Pour fabriquer le nylon‑6, l’industrie produit d’abord l’oxime du cyclohexanone, qui est ensuite convertie en caprolactame, le précurseur direct du nylon. Les usines classiques obtiennent un intermédiaire crucial, l’hydroxylamine, en réduisant des oxydes d’azote avec du dioxyde de soufre et de l’hydrogène. Cette approche présente une importante empreinte carbone, un mauvais rendement atomique et des problèmes sérieux de sécurité et de pollution. Des voies alternatives fondées sur le peroxyde d’hydrogène évitent certains risques mais dépendent d’un oxydant coûteux et instable. Avec une capacité mondiale de production de nylon‑6 projetée à plusieurs millions de tonnes par an, trouver une voie plus sûre et à faible émission de carbone vers l’oxime du cyclohexanone est un défi urgent.
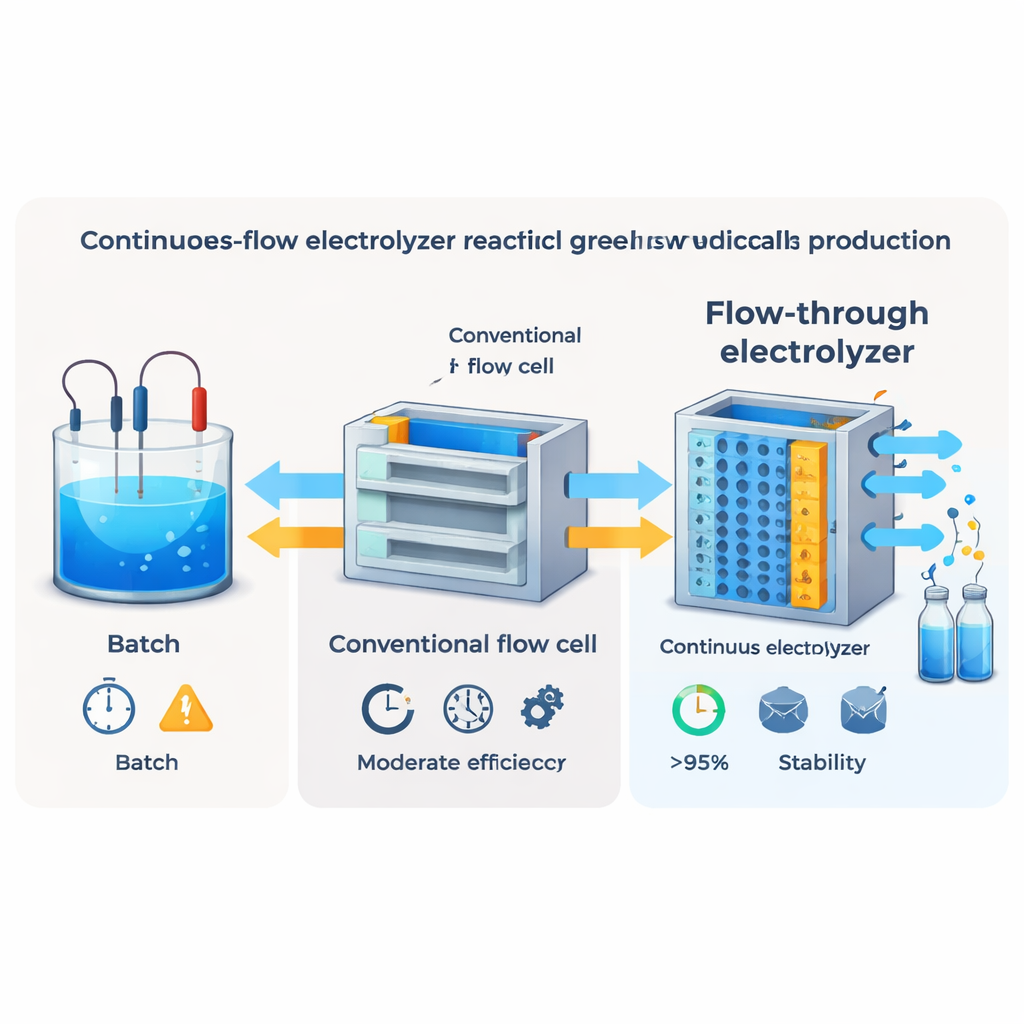
Utiliser l’électricité pour piloter une chimie plus propre
Les auteurs exploitent la disponibilité croissante d’électricité renouvelable pour repenser la fabrication de l’oxime du cyclohexanone. Plutôt que d’apporter de l’hydroxylamine, ils la génèrent directement à partir d’ions nitrite en solution sur une électrode, où des électrons fournis par une alimentation réduisent progressivement le nitrite en hydroxylamine. Cette hydroxylamine fraîchement formée réagit ensuite spontanément avec le cyclohexanone pour donner l’oxime souhaitée. Des démonstrations antérieures en laboratoire ont montré la faisabilité de cette voie, mais elles reposaient sur des cellules par lots de petite taille avec une évolutivité limitée et laissaient un décalage entre la vitesse de formation de l’hydroxylamine et celle de sa réaction, conduisant à une efficacité globale médiocre dans les dispositifs à flux continu.
Les catalyseurs à atome unique comme outils de précision
Pour améliorer les performances, l’équipe a d’abord recherché un catalyseur très sélectif. Ils ont créé une famille de matériaux « à atome unique », où des atomes métalliques isolés (cobalt, fer ou manganèse) sont ancrés sur un support en carbone dopé à l’azote. Des études détaillées par diffraction X et microscopie électronique ont confirmé que les métaux sont dispersés au niveau atomique, non agglomérés en particules. Testé dans une cellule électrochimique standard, l’échantillon au cobalt s’est distingué : il a produit l’oxime du cyclohexanone avec une efficacité faradique supérieure à 80 % et une sélectivité en carbone quasi parfaite, c’est‑à‑dire que presque chaque atome de carbone issu du cyclohexanone finissait dans le produit ciblé. Des spectroscopies avancées et des simulations informatiques ont expliqué pourquoi : le cobalt lie les intermédiaires azotés clés juste assez fortement pour orienter la réaction vers l’hydroxylamine, sans les réduire excessivement en ammoniaque ni gaspiller des électrons à la production d’hydrogène.
Repenser l’écoulement du liquide
Même un catalyseur excellent ne peut compenser une mauvaise distribution des réactifs. Dans les cellules à flux conventionnelles équipées d’une membrane, le liquide contourne l’électrode plutôt que de la traverser, si bien que les molécules doivent diffuser lentement vers les sites actifs. Les chercheurs ont utilisé des simulations de dynamique des fluides et des essais expérimentaux pour concevoir une cellule où l’électrolyte est forcé de traverser l’électrode elle‑même. Cette architecture « flow‑through » réduit considérablement les distances de diffusion et crée un fort écoulement convectif à travers le catalyseur. Par rapport aux configurations « flow‑by » standard, le nouveau design a augmenté la vitesse du liquide à l’intérieur de l’électrode de plusieurs ordres de grandeur et porté l’efficacité faradique pour l’oxime du cyclohexanone au‑delà de 95 %, y compris à des courants pertinents industriellement.
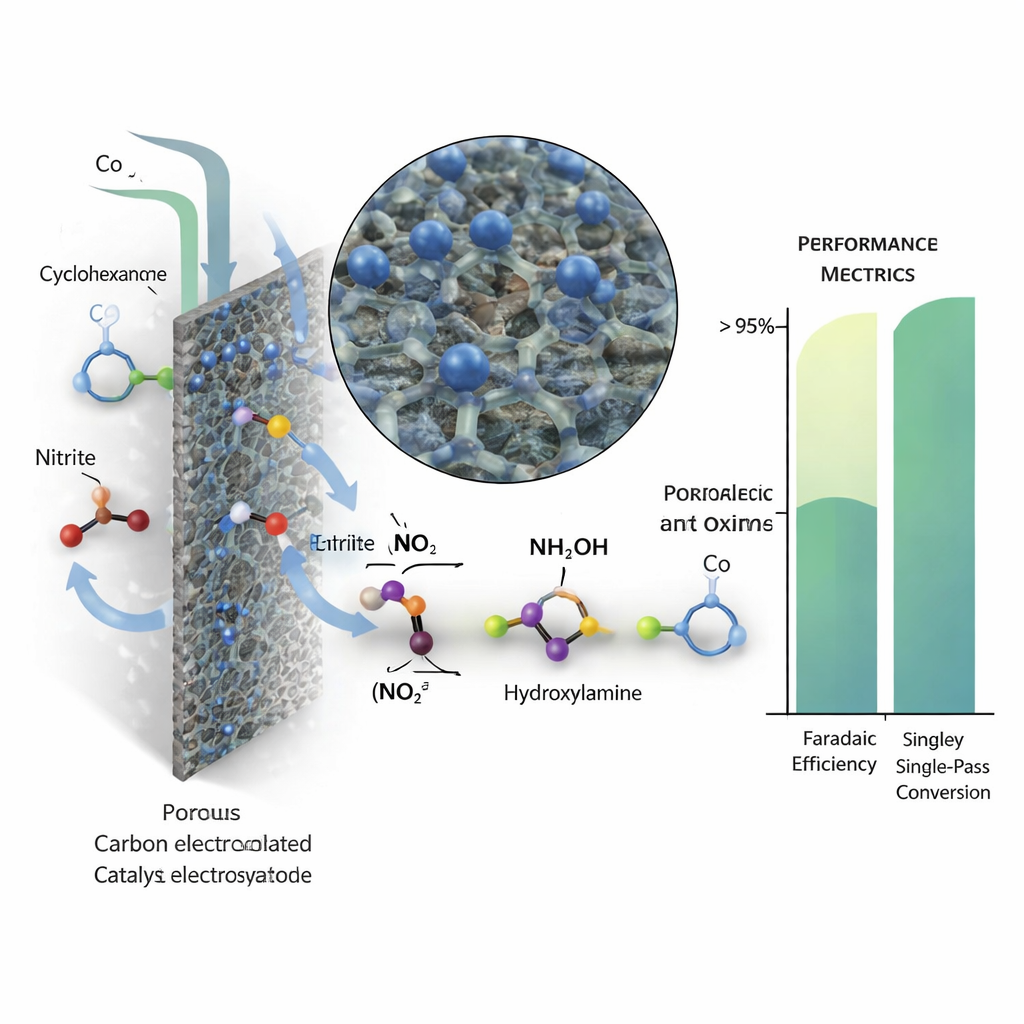
Rendre chaque passage efficace
Pour qu’un procédé continu soit rentable, un seul passage du liquide dans la cellule doit convertir la majeure partie du cyclohexanone, évitant des boucles de recyclage complexes. L’équipe a montré qu’en ajustant finement le débit et la concentration en nitrite, ils pouvaient équilibrer la vitesse de formation de l’hydroxylamine avec l’apport en cyclohexanone. Dans des conditions optimisées, la conversion en un seul passage a dépassé 95 % tout en maintenant une haute efficacité faradique. Le système a fonctionné de manière stable pendant 110 heures, produisant plus de 16 grammes d’oxime brut de haute pureté, et le catalyseur au cobalt a conservé sa structure atomique. Une analyse techno‑économique suggère qu’avec des gains supplémentaires en efficacité et en mise à l’échelle, ainsi qu’un accès à de l’électricité renouvelable peu coûteuse, le procédé pourrait produire l’oxime du cyclohexanone à un coût compatible avec la production de nylon à grand volume.
Ce que cela signifie pour les matériaux du quotidien
Pour les non‑spécialistes, le message central est simple : en maîtrisant la circulation du liquide dans un réacteur électrochimique et en utilisant un catalyseur à atome unique finement réglé, les auteurs transforment une étape polluante et fossile de la production du nylon en une étape efficace et pilotée par l’électricité. Leur conception à flux traversant extrait plus de produit de chaque électron et de chaque goutte de liquide, tandis que leur analyse trace une voie réaliste vers la viabilité économique. Au‑delà de cette molécule spécifique, la même stratégie — combiner des catalyseurs intelligents et des architectures d’écoulement optimisées — pourrait aider à électrifier et à assainir de nombreux autres procédés chimiques à grande échelle qui sous‑tendent la vie moderne.
Citation: Li, J., Wang, X., Yang, X. et al. Managing electrolyte flow boosts the efficiency of continuous oxime electrosynthesis to over 95%. Nat Commun 17, 1970 (2026). https://doi.org/10.1038/s41467-026-68738-0
Mots-clés: électrosynthèse, électrolyseur à flux traversant, catalyseur à atome unique, précurseur du nylon, chimie verte