Clear Sky Science · fr
Gémcitabine plus sélinexor dans des sarcomes avancés sélectionnés : un essai de phase I du groupe espagnol de recherche sur les sarcomes
Un nouvel espoir pour un cancer rare et difficile
Les sarcomes sont des cancers rares qui touchent souvent des adultes jeunes et peuvent être très difficiles à traiter une fois qu’ils se sont propagés. Pour de nombreux patients, les traitements actuels ne contrôlent la maladie que pendant une courte période. Cette étude évalue une nouvelle association médicamenteuse — une chimiothérapie bien connue, la gémcitabine, associée à une pilule ciblée plus récente, le sélinexor — pour déterminer si, en travaillant ensemble, ils peuvent mieux ralentir ou réduire les sarcomes avancés tout en maintenant des effets secondaires acceptables.
Pourquoi l’association de deux médicaments pourrait être plus efficace
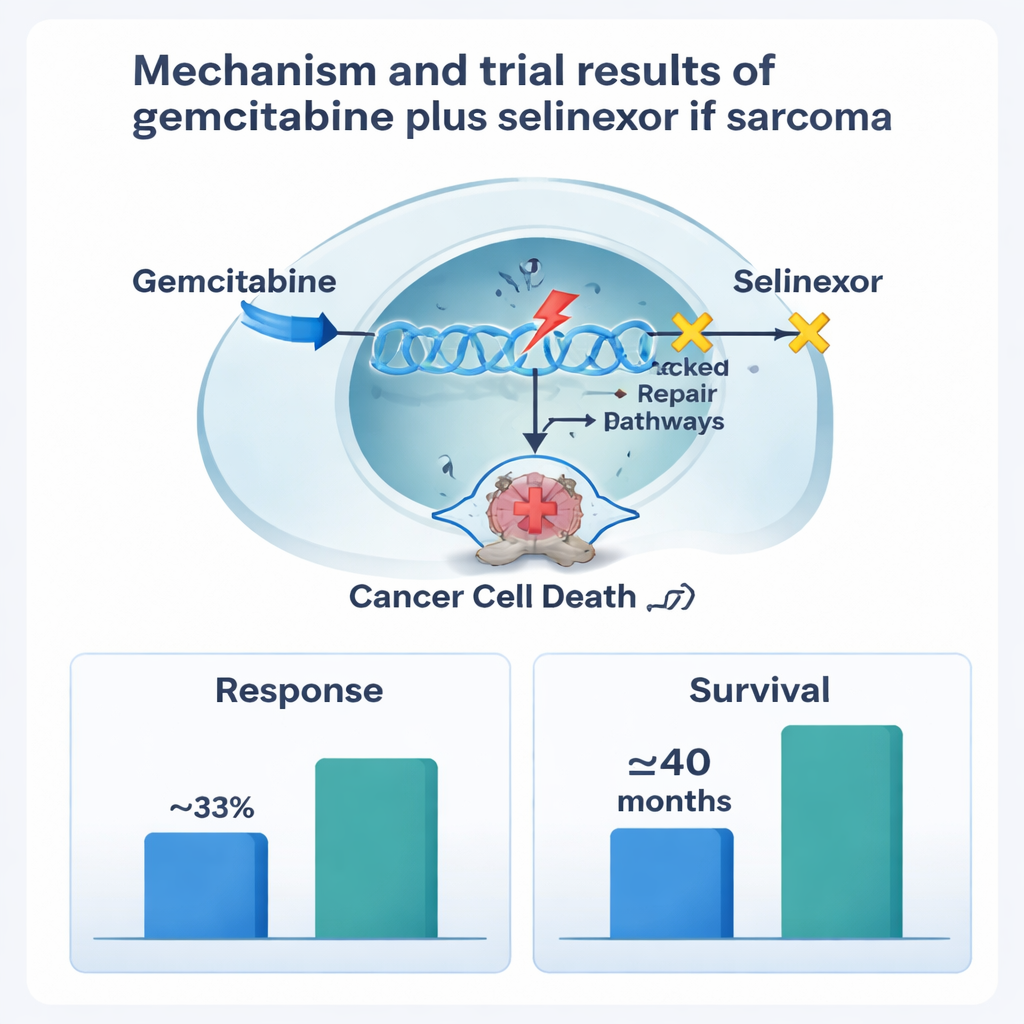
La gémcitabine est une chimiothérapie standard qui endommage l’ADN des cellules à division rapide, y compris les cellules cancéreuses. Le sélinexor agit d’une façon très différente : il bloque une protéine appelée exportine-1, qui aide normalement à déplacer des protéines de contrôle importantes hors du noyau de la cellule. Lorsque l’exportine-1 est hyperactive, comme c’est le cas dans de nombreuses tumeurs, les cellules cancéreuses peuvent échapper aux « signaux d’arrêt » internes et résister aux traitements. En retenant les protéines suppresseurs de tumeurs à l’intérieur du noyau, le sélinexor peut pousser les cellules cancéreuses vers l’autodestruction. Des travaux en laboratoire ont suggéré que donner d’abord la gémcitabine pour endommager l’ADN, puis le sélinexor pour bloquer les voies de réparation et de survie, pourrait être particulièrement puissant dans certains sarcomes.
Signaux prometteurs dans les expériences en laboratoire
Avant de traiter des patients, les chercheurs ont testé les deux médicaments ensemble sur des cellules cancéreuses cultivées en laboratoire, en se concentrant sur trois types de sarcomes : léiomyosarcome, ostéosarcome et tumeurs malignes des gaines nerveuses périphériques. Dans plusieurs lignées cellulaires de léiomyosarcome et de tumeurs des gaines nerveuses, la combinaison a tué davantage de cellules cancéreuses que chacun des médicaments pris isolément, montrant une véritable synergie. Ces cellules présentaient plus de dommages à l’ADN et des taux plus élevés d’apoptose quand les deux médicaments étaient utilisés ensemble. L’équipe a également étudié des protéines qui aident les cellules à survivre et à se diviser, comme la survivine. Lorsque le sélinexor faisait chuter fortement les niveaux de survivine et modifiait une autre protéine, IκBα, la combinaison était particulièrement efficace. En revanche, les cellules d’ostéosarcome montraient souvent l’effet inverse : les deux médicaments interféraient l’un avec l’autre, suggérant que cette approche pourrait ne bénéficier qu’à certains types de sarcomes sélectionnés.
Comment l’étude a été conduite chez les patients
L’essai clinique a recruté 17 adultes en Espagne présentant des sarcomes avancés ayant progressé malgré au moins un traitement standard. La plupart étaient atteints de léiomyosarcome, et un plus petit nombre présentait un ostéosarcome ou deux autres sarcomes rares. Les médecins ont utilisé un schéma progressif et prudent pour déterminer la dose maximale tolérée par les patients. Tous ont reçu la gémcitabine par voie intraveineuse les jours 1 et 8 d’un cycle de trois semaines, suivie d’un traitement oral hebdomadaire par sélinexor. L’équipe a surveillé de près les effets indésirables sévères durant les premiers cycles pour décider de la dose recommandée pour les études ultérieures.
Sécurité, effets secondaires et premiers bénéfices
Les principaux effets secondaires étaient des baisses des cellules sanguines — en particulier les globules blancs et les plaquettes — ce qui est courant avec la chimiothérapie. Ces complications étaient fréquentes mais généralement gérables grâce aux injections de facteurs de croissance, aux ajustements de dose et aux retards de traitement. Des nausées, vomissements et de la fatigue ont également été observés, mais pour la plupart légers à modérés, et aucun patient n’a dû interrompre l’étude en raison de la toxicité. La dose finale recommandée conservait la gémcitabine à un niveau relativement élevé tout en utilisant une dose hebdomadaire légèrement réduite de sélinexor pour améliorer la tolérance. Parmi 16 patients dont les tumeurs étaient mesurables, cinq ont présenté une réduction nette des tumeurs et cinq autres une maladie stable, aboutissant à un taux de réponse global d’environ 31 %. Pour l’ensemble du groupe, le cancer est resté contrôlé pendant une médiane d’environ 5 à 6 mois. Les patients atteints de léiomyosarcome se sont montrés particulièrement bien lotis, avec un contrôle de la maladie durant en moyenne près de 8 mois et une survie globale se rapprochant de trois ans et un quart, bien que le faible nombre de patients impose de rester prudent quant à l’interprétation de ces résultats.
Indices sur les patients susceptibles de bénéficier le plus
Comme tous les patients n’ont pas répondu, les chercheurs ont cherché des marqueurs dans les échantillons tumoraux qui pourraient prédire un bénéfice. Des niveaux élevés de survivine et une forte coloration nucléaire d’IκBα étaient tous deux associés à des délais plus courts avant la progression du cancer, en particulier dans le léiomyosarcome. Cela correspond à la constatation en laboratoire que la perte complète de survivine est liée à une synergie médicamenteuse plus marquée. Si ces résultats sont confirmés dans des études plus larges, ces protéines pourraient aider les médecins à identifier quels patients sont les plus susceptibles de répondre à la combinaison gémcitabine–sélinexor et qui pourrait nécessiter d’autres stratégies.
Que signifie cela pour les patients atteints de sarcome
Pour les personnes confrontées à des sarcomes avancés, les options thérapeutiques sont limitées et souvent d’efficacité brève. Cet essai de phase précoce montre que l’association gémcitabine–sélinexor est faisable, que ses effets secondaires peuvent être maîtrisés avec un accompagnement adapté, et qu’elle présente des signes encourageants d’efficacité, en particulier pour le léiomyosarcome. Ce travail commence aussi à dévoiler des marqueurs biologiques susceptibles d’orienter des prises en charge plus personnalisées. Des essais de phase II et III de plus grande ampleur sont maintenant en cours pour confirmer si cette combinaison améliore réellement la survie et la qualité de vie, mais pour les patients et les cliniciens, elle représente une voie nouvelle et réaliste dans la recherche de meilleurs traitements des sarcomes.
Citation: Martin-Broto, J., Casado, A., Marquina, G. et al. Gemcitabine plus selinexor in selective advanced sarcomas: a phase I of the Spanish group for research on sarcoma study. Nat Commun 17, 1873 (2026). https://doi.org/10.1038/s41467-026-68729-1
Mots-clés: traitement du sarcome, léiomyosarcome, gémcitabine, sélinexor, essai clinique contre le cancer