Clear Sky Science · fr
Sulfonations divergentes de carbonates propargyliques catalysées par le nickel
Pourquoi cette chimie compte au-delà du laboratoire
Les molécules contenant du soufre sont au cœur de nombreux médicaments modernes, agents de protection des cultures et matériaux avancés. Pourtant, les fabriquer de manière précise, efficace et flexible reste souvent difficile. Cet article décrit une méthode catalytique à base de nickel capable de transformer des matières premières simples en plusieurs familles distinctes de composés riches en soufre, toutes avec un contrôle strict de leur configuration tridimensionnelle. Un tel degré de maîtrise peut accélérer la découverte de médicaments et aider les chimistes à construire des molécules complexes de façon plus propre et plus durable.
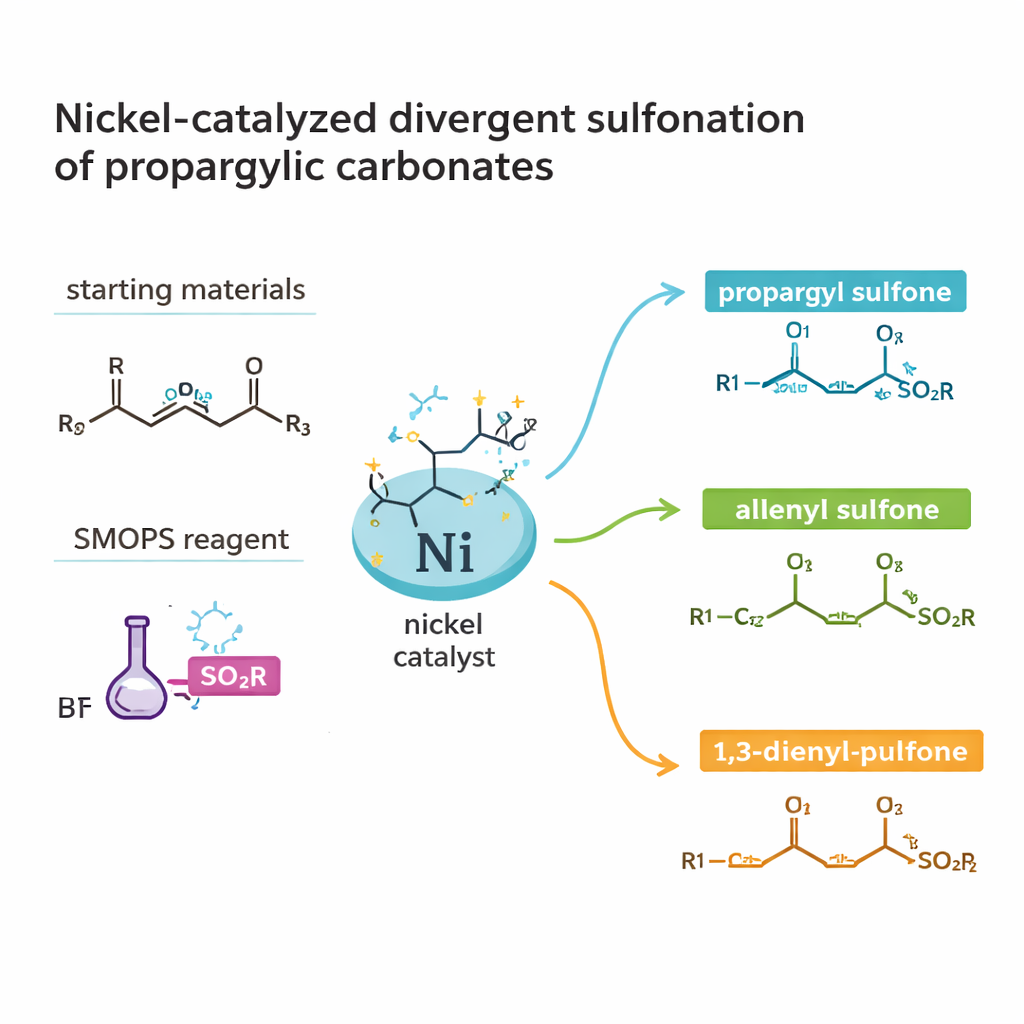
Construire des molécules utiles à partir de pièces simples
Le travail porte sur une classe de composés appelés sulfones et sulfinate, qui contiennent du soufre lié à l’oxygène et au carbone. Ces structures sont présentes dans de nombreux produits naturels bioactifs et médicaments, mais les voies traditionnelles pour les obtenir peuvent être longues et générer des déchets. Les auteurs se concentrent sur un sous-type particulièrement précieux : les sulfinate chiraux, dont les images miroirs peuvent se comporter très différemment dans l’organisme. Plutôt que de partir de blocs de construction déjà complexes, ils utilisent deux partenaires facilement disponibles : des carbonates propargyliques (une petite épine dorsale carbonée dotée d’un groupe partant) et une source de soufre commerciale connue sous le nom de SMOPS. En combinant ces éléments sous catalyse au nickel, ils cherchent à générer des produits sulfurés de grande valeur en une ou deux étapes seulement.
Un système catalytique, trois familles de produits
Un aspect frappant de l’étude est que les mêmes ingrédients de base peuvent être orientés vers la formation de trois types de produits distincts : sulfones propargyliques, sulfones allenyles et sulfones 1,3-dièniques. Chacun de ces cadres carbonés mène à une chimie et à une activité biologique en aval différentes. En choisissant avec soin le ligand lié au nickel, le solvant, la température et les additifs, l’équipe peut « diriger » la réaction vers un résultat ou un autre. Dans des conditions douces en acétonitrile et avec un ligand phosphine chiral, ils obtiennent des sulfones propargyliques en bon rendement et avec un excellent contrôle de l’énantioséléctivité. Le traitement de ces produits par de l’oxyde d’aluminium transforme délicatement la triple liaison carbone–carbone en allène, là encore sans perdre l’information chirale. Le passage à un ligand et à un solvant différents oriente en revanche le processus vers les sulfones 1,3-dièniques, étendant le squelette carboné.
Tester l’étendue et la flexibilité
Pour évaluer la généralité de cette approche, les chercheurs ont fait varier les deux partenaires de la réaction. Ils ont montré que de nombreux sulfinate de sodium différents, y compris des espèces alkyles simples, aryles et des systèmes cycliques plus complexes, réagissent proprement et donnent des produits chiraux avec un fort excès énantiomérique. De même, un large éventail de carbonates propargyliques portant différentes substitutions sur l’anneau aromatique ou la chaîne carbonée fonctionne bien, bien que certains substrats présentant des groupes très volumineux ou des alcynes terminaux se situent hors du périmètre actuel de la méthode. L’équipe démontre également que l’on peut augmenter les quantités sans sacrifier l’efficacité ni la sélectivité, une étape essentielle pour une utilisation pratique. Cette large portée permet aux chimistes d’assembler de nombreux fragments différents et d’accéder rapidement à une bibliothèque de molécules sulfurées apparentées.
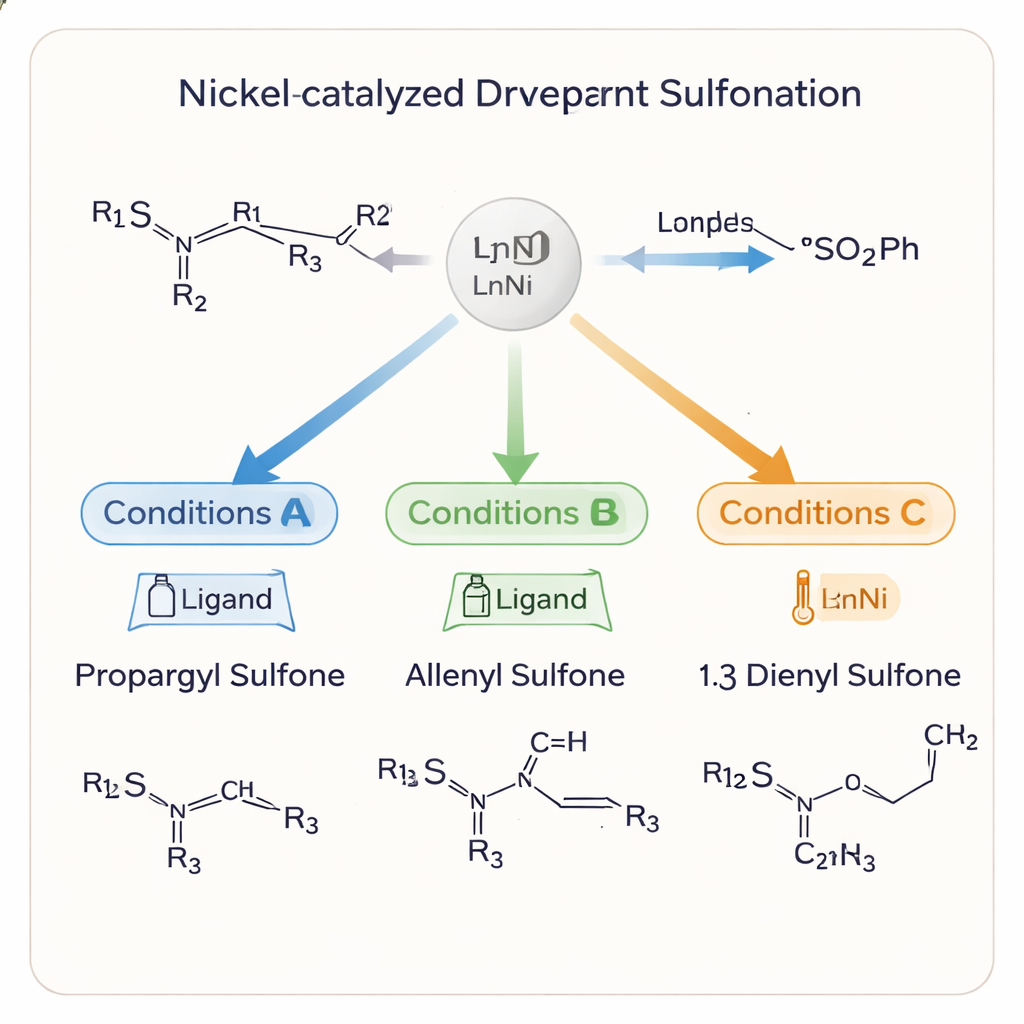
Transformer des blocs de construction en cibles complexes
Au‑delà de la simple préparation de ces sulfones, les auteurs montrent combien il est facile de les convertir en autres structures utiles. L’hydrogénation transforme la triple liaison en alcanes ou alcènes tout en préservant le centre chiral adjacent au soufre. Des réactions de suivi simples convertissent les unités sulfone en sulfinates, sulfonamides et fluorures sulfonyl — des motifs couramment rencontrés en chimie médicinale et dans des réactions d’assemblage de type « click ». En point d’orgue, ils utilisent leur méthode comme étape clé dans une synthèse concise d’un acide β‑sulfinylhydroxamique chiral, un type de molécule connu pour inhiber des enzymes bactériennes. Cette voie évite plusieurs étapes anciennes et plus lourdes et souligne la puissance synthétique de disposer de sulfinate chiraux sur demande.
Comment la réaction choisit sa voie
L’équipe examine également comment et pourquoi la réaction bifurque entre différents produits. Des expériences chronologiques montrent que le sulfone propargylique se forme généralement en premier, puis peut se réarranger en allène et, éventuellement, en 1,3‑diène sous certaines conditions. Le catalyseur au nickel, combiné au ligand et à l’additif choisis, contrôle quels intermédiaires sont favorisés et comment le groupe sulfure se déplace le long de la chaîne carbonée. L’oxyde d’aluminium, par exemple, permet la conversion alcyne→allène à très basse température tout en préservant la configuration 3D des atomes. Un mécanisme simplifié suggère que de subtils changements de conditions réorientent un intermédiaire nickel commun le long de voies différentes, expliquant comment un même système peut produire plusieurs produits distincts et précisément définis.
Ce que cela signifie pour les futurs médicaments et matériaux
Pour les non‑spécialistes, l’idée principale est que cette méthode catalysée par le nickel offre un « tableau de commande » chimique polyvalent : à partir des mêmes pièces de départ simples, les chimistes peuvent sélectionner l’ossature riche en soufre souhaitée et l’obtenir en une seule étape hautement sélective. Parce que ces produits sont d’excellents blocs de construction pour les médicaments et d’autres molécules fonctionnelles, l’approche pourrait raccourcir le chemin du concept au composé candidat. Elle illustre aussi comment une conception soignée du catalyseur et des conditions peut transformer une transformation autrefois difficile en un outil de routine, ouvrant la voie à une construction plus rapide et plus propre de molécules complexes et chirales contenant du soufre.
Citation: Gu, W., He, Z., Wang, H. et al. Nickel-catalyzed divergent sulfonations of propargylic carbonate. Nat Commun 17, 1882 (2026). https://doi.org/10.1038/s41467-026-68720-w
Mots-clés: catalyse au nickel, sulfones chiraux, synthèse asymétrique, conception de réactions organiques, blocs de construction de type médicament