Clear Sky Science · fr
Les caractéristiques intrinsèques de la tumeur façonnent la différenciation des lymphocytes T du stade précurseur au myélome multiple symptomatique
Pourquoi cette recherche est importante
Le myélome multiple est un cancer du sang qui se forme dans la moelle osseuse et est presque toujours précédé par des états précoces et plus silencieux qui peuvent ou non évoluer vers la maladie manifeste. Beaucoup de personnes vivent pendant des années avec ces stades précurseurs, sans savoir si ni quand la maladie progressera. Cette étude pose une question d’actualité : peut-on « lire » l’état d’esprit et l’historique du système immunitaire — en particulier des lymphocytes T — pour comprendre comment le myélome se développe, comment il répond aux traitements et qui court le plus grand risque d’évolution ?
Les éclaireurs anticancéreux de l’organisme
Les lymphocytes T sont des cellules immunitaires polyvalentes qui peuvent reconnaître et détruire des cellules anormales, y compris des cellules cancéreuses. Dans les tumeurs solides comme celles du poumon ou de la peau, une stimulation prolongée peut pousser les lymphocytes T vers un état d’épuisement où ils deviennent inefficaces, un changement que les immunothérapies modernes cherchent à inverser. Les auteurs ont constitué une immense carte unicellulaire de plus d’un million de cellules provenant de la moelle osseuse et du sang de personnes atteintes de myélome multiple, de ses stades précurseurs (MGUS et myélome indolent) et de témoins non cancéreux. En analysant à la fois l’activité génique et les séquences uniques des récepteurs qui définissent chaque clone de lymphocytes T, ils ont reconstitué l’organisation des lymphocytes T, leur « âge » ou leur niveau d’expérience, et à quel point ils suivent de près la tumeur sous-jacente.
Pas épuisés, mais prématurément vieillissants
Contrairement à ce qui est observé dans de nombreux cancers solides, l’équipe a constaté que les lymphocytes T dans le myélome sont rarement véritablement épuis. Les cellules portant des marqueurs classiques d’épuisement étaient en grande partie confinées à un seul patient inhabituel. Au lieu de cela, les lymphocytes T de la moelle osseuse dans le myélome indolent et symptomatique s’éloignaient des cellules naïves et de stade précoce vers des types « mémoire terminale » très expérimentés qui ressemblent aux lymphocytes T des personnes âgées. Ce schéma — appelé basculement des lymphocytes T — parallélisait le vieillissement naturel du système immunitaire mais semblait exagéré chez les patients, comme si leurs lymphocytes T avaient vieilli plus vite que le reste de l’organisme. Plus la maladie était avancée et plus la charge tumorale était élevée, plus ce basculement vers des cellules mémoire tardives était marqué, et des changements similaires pouvaient être observés dans le sang.
Indices tirés des empreintes des lymphocytes T
Chaque lymphocyte T porte un récepteur unique, et les cellules partageant la même séquence de récepteur appartiennent à un clone qui s’est développé en réponse à un déclencheur. En suivant ces récepteurs, les investigateurs ont montré que les moelles des patients atteints de myélome contenaient de nombreux clones de lymphocytes T expansés présentant des caractéristiques de cellules tueuses puissantes. Ces clones ne reconnaissaient pas principalement des virus courants. Ils portaient plutôt un profil génique distinct « non viral » lié à un fort appareil cytotoxique et étaient enrichis chez les personnes atteintes de myélome par rapport aux stades précurseurs. Les tumeurs qui présentaient mieux des fragments protéiques à leur surface — via une activité plus élevée des gènes de présentation d’antigènes — avaient tendance à être associées à ces lymphocytes T fortement différenciés et non viraux. Les patients dont les tumeurs montraient cette interaction immunologique plus marquée avaient généralement une survie meilleure, ce qui suggère que ces lymphocytes T sont, du moins en partie, réellement anti-tumoraux.
Traitement, rechute et signaux d’alerte précoces
L’étude a également suivi des patients ayant subi une greffe autologue de cellules souches, une thérapie intensive courante. Après la greffe, le répertoire des récepteurs des lymphocytes T est devenu plus dominé par quelques grands clones. Beaucoup de ces clones en expansion pouvaient être retracés jusqu’à des lymphocytes T CD8 terminalement différenciés présents avant le traitement et portant le même profil non viral associé au myélome. Les patients présentant des résidus tumoraux après la greffe avaient tendance à avoir des répertoires de lymphocytes T particulièrement clonaux et biaisés, ce qui suggère qu’une réponse lymphocytaire vigoureuse mais de type vieillissant peut ne pas suffire à éradiquer complètement la maladie. En examinant plus tôt l’histoire de la maladie, les auteurs ont constaté que les patients avec myélome indolent qui ont ensuite progressé vers un myélome actif avaient souvent une diminution des lymphocytes T CD4 régulateurs — des cellules qui aident normalement à maintenir l’équilibre des réponses immunitaires et de l’environnement médullaire. De faibles niveaux de ces cellules prédisaient une progression plus rapide, indépendamment des scores de risque cliniques existants.
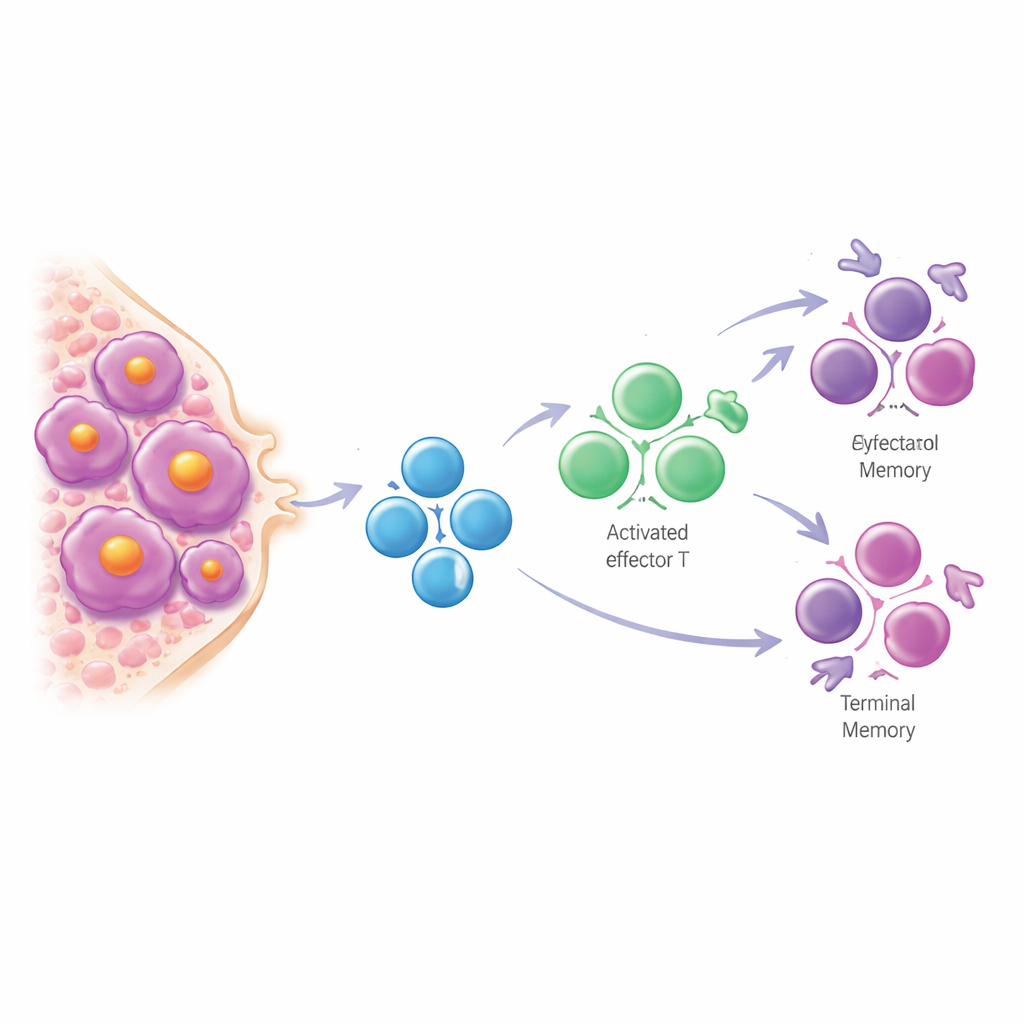
Ce que cela signifie pour les patients
Pour les personnes vivant avec le myélome et ses stades précurseurs, ce travail recontextualise la réponse immunitaire face à la tumeur. Plutôt que de simplement s’épuiser, les lymphocytes T dans le myélome semblent être poussés de façon chronique vers un état tardif et vieilli par des combats répétés contre les cellules tumorales. Ce paysage lymphocytaire cloné et biaisé reflète la charge tumorale, influence la réponse aux traitements comme la greffe et les médicaments mobilisant les lymphocytes T, et, dans le cas de la perte de lymphocytes T régulateurs, peut même signaler des individus à plus haut risque de progression du myélome indolent vers la maladie symptomatique. À long terme, ces connaissances pourraient orienter de nouvelles immunothérapies visant à rajeunir ou rediriger les lymphocytes T, et aider les cliniciens à utiliser des caractéristiques immunitaires en complément des marqueurs traditionnels pour calibrer plus précisément la surveillance et l’intervention précoce.
Citation: Foster, K.A., Rees, E., Ainley, L. et al. Tumour-intrinsic features shape T cell differentiation through precursor to symptomatic multiple myeloma. Nat Commun 17, 2400 (2026). https://doi.org/10.1038/s41467-026-68718-4
Mots-clés: myélome multiple, lymphocytes T, vieillissement immunitaire, séquençage unicellulaire, immunologie du cancer