Clear Sky Science · fr
Détermination par click de l’accumulation de molécules dans Escherichia coli
Pourquoi les petites molécules peinent à atteindre les bactéries dangereuses
La médecine moderne dépend des antibiotiques, pourtant certaines des bactéries les plus dangereuses sont aujourd’hui protégées par des parois externes résistantes qui empêchent l’entrée de nombreux médicaments. Les bactéries à Gram négatif comme Escherichia coli possèdent une membrane externe particulièrement efficace, ce qui rend la conception de médicaments capables de pénétrer et d’atteindre leurs cibles difficile. Cet article présente un nouveau test de laboratoire, appelé le test CHAMP, qui permet aux scientifiques de mesurer rapidement dans quelle mesure des milliers de petites molécules différentes franchissent ces défenses et s’accumulent à l’intérieur de cellules vivantes d’E. coli.
Une nouvelle façon d’observer l’entrée des médicaments dans les cellules bactériennes
La découverte d’antibiotiques traditionnelle s’appuyait sur des composés naturels et des tests simples de croissance pour savoir si les bactéries survivaient ou non. Ces tests ne révèlent pas la quantité de médicament réellement entrée dans la cellule, ni sa localisation une fois à l’intérieur. Les auteurs ont cherché à construire une méthode directe et largement utilisable pour suivre l’entrée des médicaments dans le cytosol bactérien — le milieu liquide intérieur où se trouvent de nombreuses cibles d’antibiotiques. Leur objectif était d’aller au‑delà de lectures grossières comme la concentration minimale inhibitrice, qui confondent l’absorption, la liaison à la cible et la biologie en aval, et d’obtenir une mesure claire de l’accumulation intracellulaire.
Transformer les bactéries en petits enregistreurs chimiques
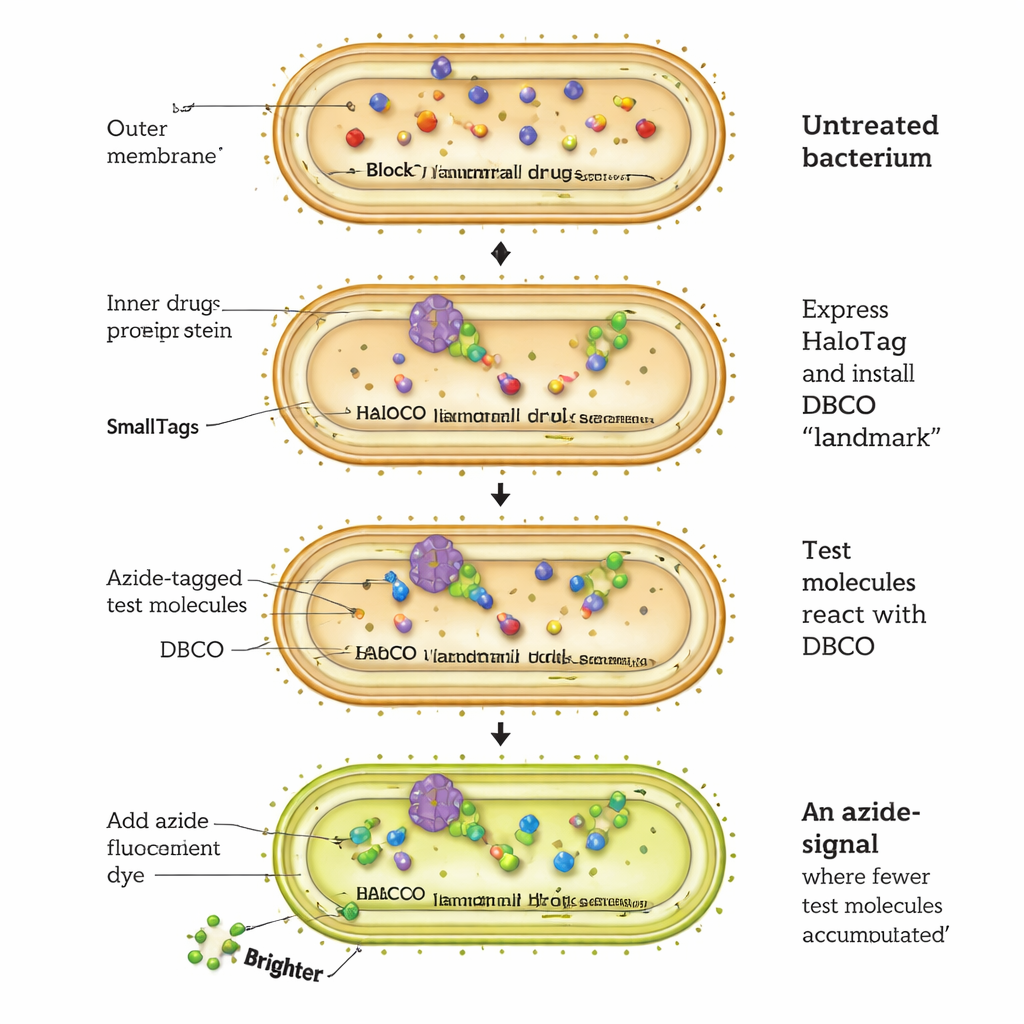
Le test CHAMP fonctionne en réaffectant une protéine bactérienne appelée HaloTag pour en faire une sorte de plate‑forme d’ancrage moléculaire. Les cellules d’E. coli sont génétiquement modifiées pour produire HaloTag dans leur cytosol. Les chercheurs attachent d’abord une poignée chimique spéciale, un alcyne « contraint » appelé DBCO, au HaloTag via un court lien chloroalcanes. Ensuite, ils exposent les bactéries à des molécules testées portant chacune un très petit tag azide. Seules les molécules testées qui traversent la membrane externe, franchissent la membrane interne et atteignent le cytosol peuvent réagir avec la poignée DBCO via une réaction de « click » hautement sélective, marquant de façon permanente le HaloTag. Enfin, les cellules sont traitées avec un colorant fluorescent azide‑marqué qui ne peut se lier qu’aux DBCO restants non occupés. Plus la fluorescence est intense, moins de molécules testées sont arrivées dans le cytosol ; des cellules plus faibles en intensité indiquent une meilleure accumulation.
Explorer comment la chimie et la biologie façonnent l’entrée des médicaments
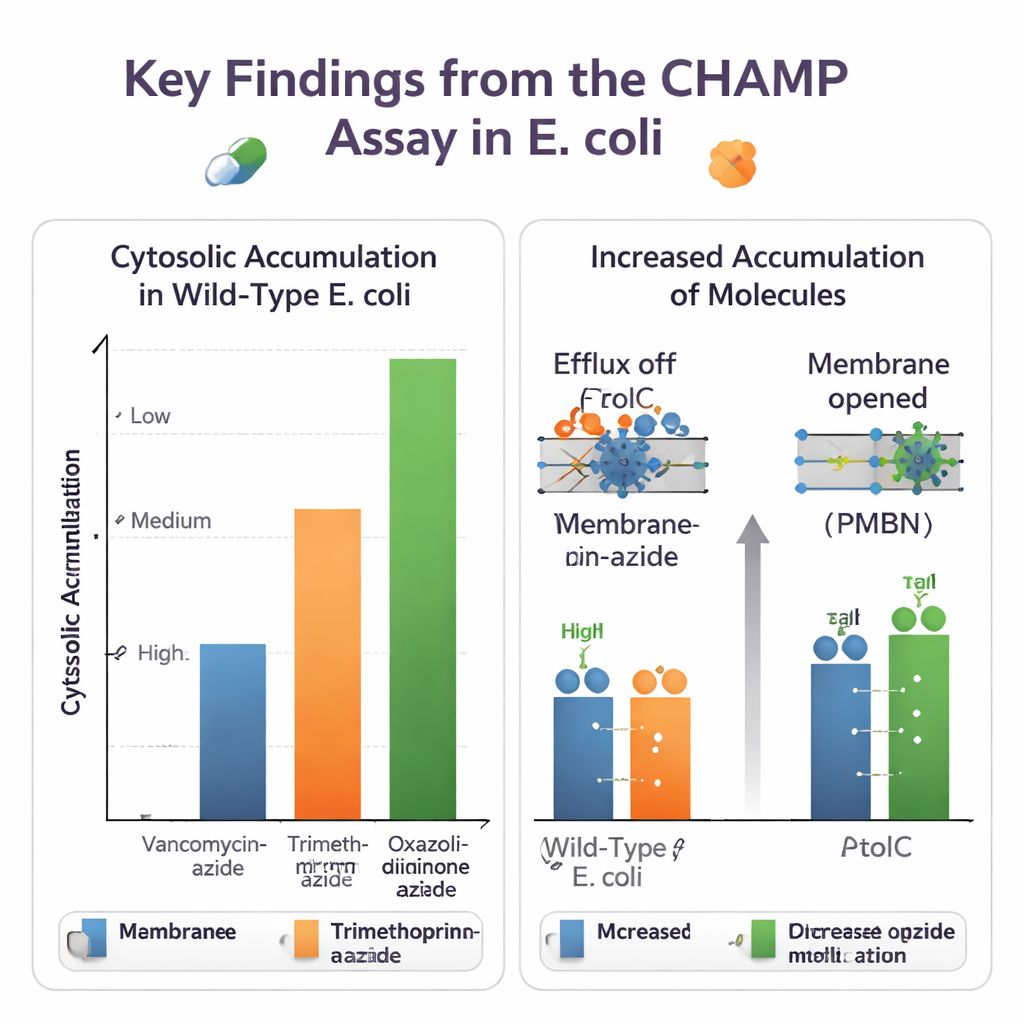
Avec CHAMP, l’équipe a d’abord ajusté l’expression de HaloTag, la quantité d’ancre DBCO et le choix des colorants fluorescents pour obtenir une fenêtre de signal large et fiable. Ils ont ensuite utilisé des séries de petites molécules étroitement liées pour observer comment des modifications chimiques influencent l’entrée. La conversion d’acides carboxyliques en amides, ou l’ajout/retrait de groupes amines basiques, pouvait modifier sensiblement les niveaux cytosoliques. Dans de nombreux cas, les amines primaires favorisaient l’accumulation, rappelant les « règles eNTRy » indépendantes proposées par d’autres équipes. Le test a également pris en charge des versions azide‑marquées d’antibiotiques réels, révélant de grandes différences : des médicaments volumineux comme la vancomycine atteignaient à peine le cytosol, tandis que des antibiotiques plus petits, tels que des dérivés du triméthoprime et certains oxazolidinones, y pénétraient beaucoup plus facilement.
Mettre à nu les défenses bactériennes qui expulsent les médicaments
Parce que la méthode s’exécute dans des bactéries vivantes génétiquement programmables, elle permet de démêler les rôles des différentes défenses cellulaires. Les auteurs ont comparé E. coli normales à des souches dépourvues de TolC, un composant clé d’une pompe d’efflux multi‑médicaments majeure, ou à des cellules traitées par un inhibiteur moléculaire de TolC. Pour la novobiocine et plusieurs autres antibiotiques azide‑marqués, CHAMP a montré une accumulation cytosolique nettement plus élevée lorsque TolC était désactivé, confirmant que ces composés sont des substrats d’efflux. Ils ont aussi testé des moyens d’assouplir la barrière de la membrane externe, soit chimiquement avec le peptide PMBN, soit génétiquement en surexprimant un porine très ouverte. De nombreuses molécules auparavant peu accumulées ont montré de grands gains lorsque la membrane était perméabilisée, soulignant comment l’entrée et l’efflux agissent ensemble pour déterminer les niveaux internes de médicament.
Passer à l’échelle des milliers de molécules pour dégager des tendances et des règles
Pour démontrer un véritable haut débit, les chercheurs ont criblé un lot commercial de 404 composés azide‑marqués et une bibliothèque personnalisée de 1 152 molécules portant un groupe azide. Ils ont mesuré l’accumulation dans plusieurs contextes bactériens, notamment des cellules non traitées, des cellules traitées au PMBN, des cellules hyperporinées, et des cellules hyperporinées dépourvues de TolC. En comparant la même molécule à travers ces conditions, ils ont pu distinguer les changements dus à la biologie cellulaire plutôt qu’à des particularités de la vitesse de réaction click. En combinant les données CHAMP avec des analyses computationnelles, ils ont relié certaines caractéristiques physico‑chimiques — telles que la surface polaire, la capacité de liaisons hydrogène et des squelettes de cycles spécifiques — à une reconnaissance plus forte par l’efflux dépendant de TolC. Ce type de profilage à grande échelle commence à définir des règles de conception pour des molécules qui évitent les pompes ou exploitent plus efficacement les porines.
Ce que cela signifie pour les antibiotiques du futur
En termes simples, ce travail transforme E. coli en un capteur à haut débit qui indique précisément quelle quantité d’un composé testé atteint la partie de la cellule où se trouvent nombre de cibles médicamenteuses. CHAMP ne remplace pas les tests d’activité bactéricide, mais il comble une lacune cruciale en séparant le « fait d’entrer » du « fait de nuire ». Avec la capacité de mesurer plus d’un millier de molécules dans différentes souches mutantes ou chimiquement modifiées en l’espace de quelques jours, les chercheurs peuvent désormais apprendre de façon systématique quelles caractéristiques chimiques favorisent l’entrée, réduisent l’efflux ou bénéficient d’adjuvants perturbant la membrane. Ces connaissances devraient accélérer la conception de nouveaux antibiotiques et de médicaments d’appoint capables de percer les redoutables défenses des pathogènes à Gram négatif avant que la résistance n’érode davantage l’arsenal antibiotique.
Citation: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Mots-clés: résistance aux antibiotiques, Escherichia coli, perméabilité des médicaments, pompes d’efflux, chimie click