Clear Sky Science · fr
Le niveau d’expression de TREM2 est crucial pour l’état microglial, la capacité métabolique et l’efficacité de l’agonisme de TREM2
Pourquoi les cellules de nettoyage du cerveau comptent dans la maladie d’Alzheimer
La maladie d’Alzheimer est surtout connue pour les amas de protéines collantes dans le cerveau, mais une histoire tout aussi importante est la façon dont les cellules immunitaires du cerveau réagissent à ces lésions. Ces cellules, appelées microglies, jouent le rôle de nettoyeurs et de secouristes : elles éliminent les débris, régulent l’inflammation et aident les neurones à survivre. Cette étude pose une question apparemment simple aux implications majeures pour les traitements futurs : quelle quantité d’un récepteur microglial clé, TREM2, est « juste suffisante » pour protéger le cerveau — et quand des médicaments qui stimulent TREM2 peuvent-ils aider ou nuire ?
Un variateur, pas un interrupteur
Des travaux génétiques antérieurs ont montré que les personnes portant certaines variantes entraînant une perte de fonction du gène TREM2 présentent un risque accru de maladie d’Alzheimer à début tardif. Pourtant, TREM2 avait souvent été traité comme un interrupteur marche/arrêt : présent ou absent. Les auteurs ont au contraire conçu une souris « rapporteuse » spéciale dans laquelle les microglies brillent en proportion de la quantité de TREM2 qu’elles produisent. Cela leur a permis de trier les microglies en groupes à faible, moyen et fort niveau de TREM2 et d’examiner ce que faisait chaque groupe. Ils ont étudié ces cellules aussi bien chez des souris saines que chez des souris développant des plaques amyloïdes, une caractéristique de la pathologie de type Alzheimer. 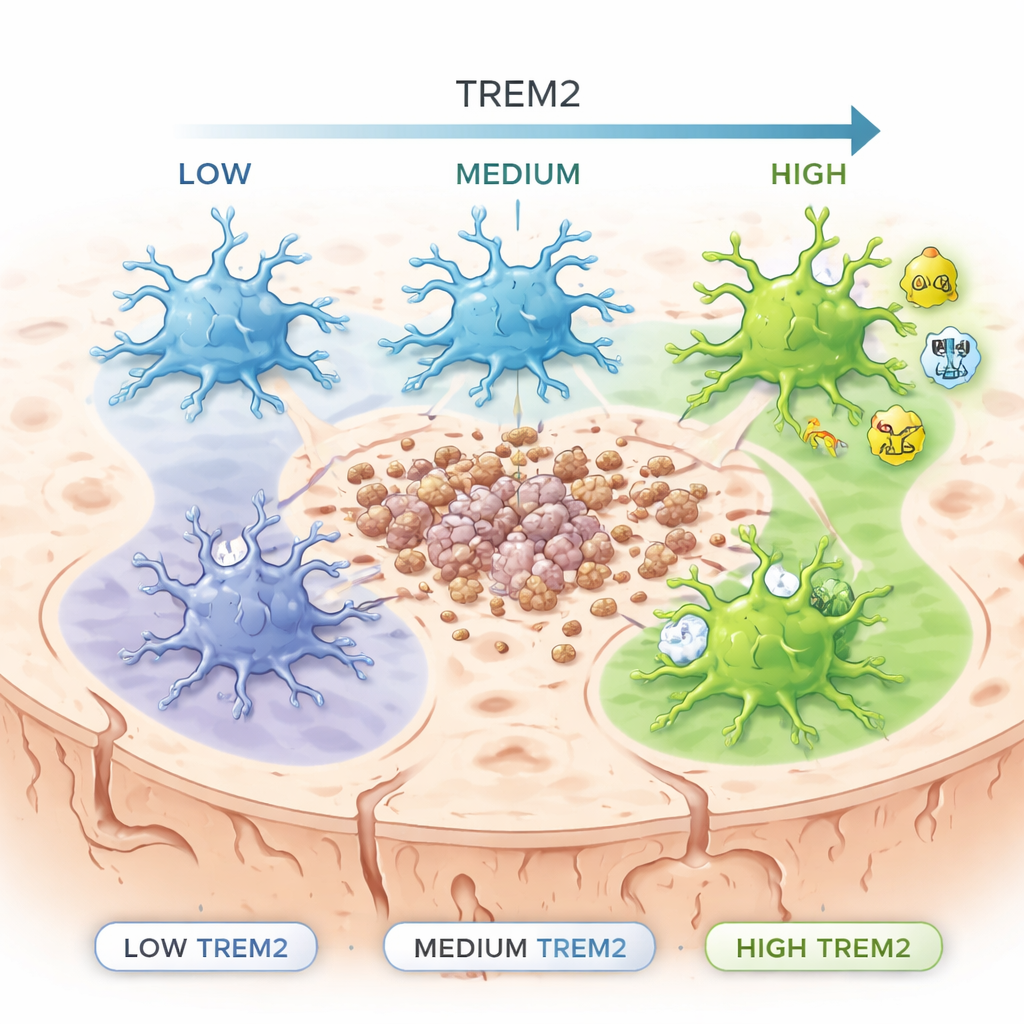
L’utilisation d’énergie et le traitement du cholestérol évoluent selon le niveau de TREM2
Une fois ces sous-groupes microgliaux séparés, les chercheurs ont analysé quels gènes étaient activés, quels métabolites étaient présents et à quel point les cellules consommaient de l’énergie. Les microglies exprimant davantage de TREM2 montraient une activité renforcée dans les voies liées à la phosphorylation oxydative (le principal système de production d’énergie de la cellule) ainsi qu’au métabolisme du cholestérol et des lipides. Des mesures de captation de glucose marqué ont confirmé que les cellules à TREM2 élevé absorbaient plus de sucre, surtout dans les cerveaux malades. Des profils détaillés de métabolites et de lipides ont révélé que les microglies à TREM2 élevé possédaient davantage de blocs de construction pour l’énergie cellulaire et la défense antioxydante, et moins de cholestérol libre et de certains acides gras, ce qui suggère une utilisation du carburant plus efficiente et une meilleure élimination du cholestérol.
Du métabolisme à la capacité de nettoyage
Ces signatures moléculaires se sont traduites par de réelles différences fonctionnelles. Dans des tests en laboratoire contrôlés, l’équipe a exposé les microglies à des fragments de myéline marqués par fluorescence — un substitut des types de débris que les microglies doivent éliminer dans le tissu cérébral malade. Les microglies à faible TREM2 ont ingéré le moins de débris ; celles à niveau moyen ont fait mieux ; et les cellules à TREM2 élevé ont été les plus voraces. Le même schéma est apparu dans deux modèles murins différents de type Alzheimer, ce qui renforce l’idée que le niveau de TREM2 est étroitement lié à la « capacité de nettoyage » de la cellule. Parallèlement, des analyses de réseaux géniques ont montré qu’un TREM2 plus élevé s’associe non seulement à un métabolisme amélioré mais aussi à certains programmes de réponse immunitaire, y compris des signaux liés aux interférons qui peuvent être bénéfiques dans certains contextes et nocifs dans d’autres. 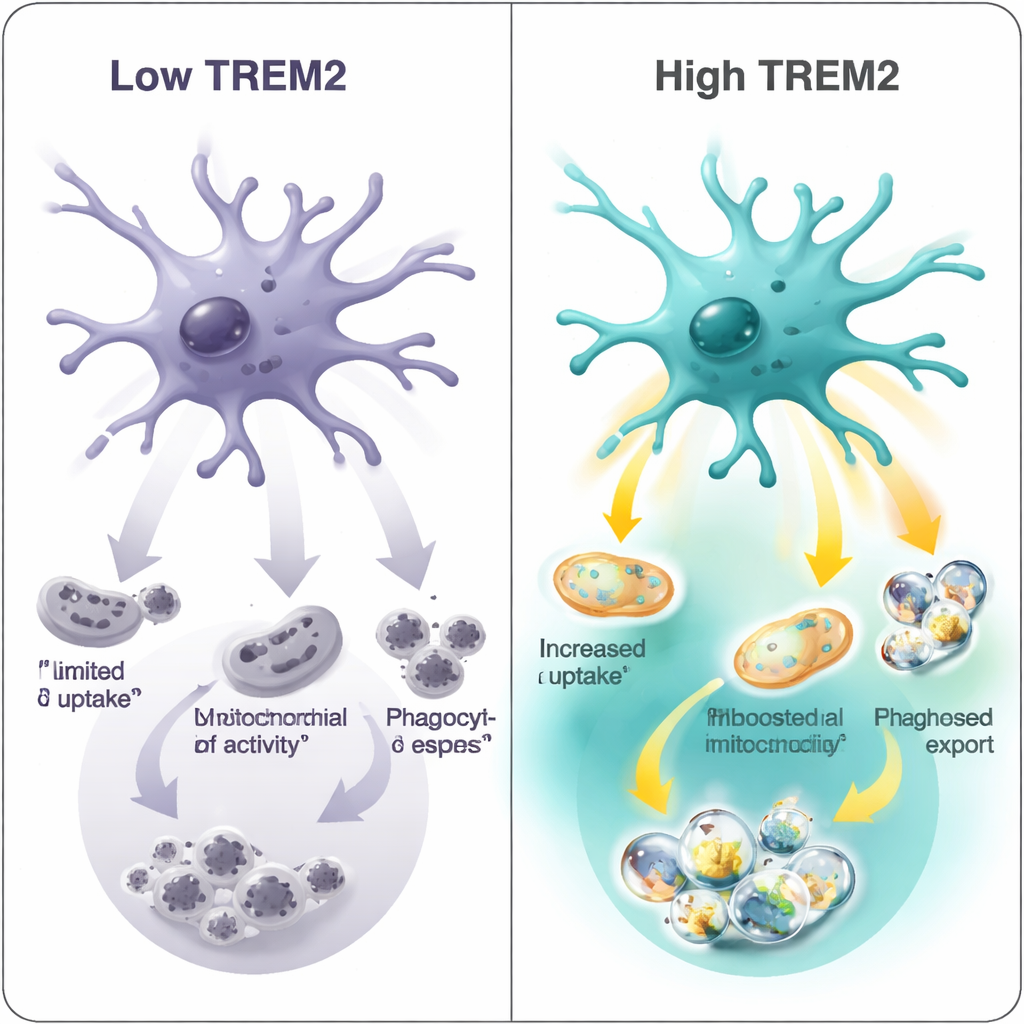
Quand stimuler TREM2 aide — et quand cela peut aller trop loin
Comme des entreprises pharmaceutiques testent des anticorps activant TREM2, les auteurs se sont demandé comment un tel médicament affecte des microglies aux niveaux de TREM2 différents. Ils ont traité des souris rapporteuses porteuses de pathologie amyloïde avec un anticorps activateur de TREM2 capable de traverser la barrière hémato‑encéphalique, puis ont de nouveau trié les microglies selon l’expression de TREM2. De manière frappante, ce sont les cellules à TREM2 moyen qui ont le plus fortement répondu : leurs marqueurs métaboliques ont montré une glycolyse accrue, une meilleure activité lysosomale et péroxysomale, et des niveaux plus élevés de certains lipides membranaires protecteurs. Les microglies à faible TREM2 ont peu changé, probablement parce qu’elles ne fournissaient pas suffisamment de cible pour le médicament. En revanche, chez les microglies à TREM2 élevé, le même traitement a semblé ramener le métabolisme vers un état plus modéré, suggérant un « effet plafond » où une activation excessive est atténuée plutôt qu’amplifiée.
Ce que cela signifie pour les traitements futurs de l’Alzheimer
Pour le lecteur non spécialiste, la conclusion principale est que les microglies ayant la bonne quantité de TREM2 sont mieux alimentées, gèrent mieux le cholestérol et éliminent plus efficacement le matériel nocif autour des plaques amyloïdes. Mais l’équilibre est délicat. Les médicaments qui stimulent TREM2 fonctionneront probablement mieux dans une fenêtre spécifique de niveaux de récepteur — trop peu de TREM2 et il n’y a pas assez de cible à activer ; trop de TREM2 et le système peut déjà être proche ou au‑delà de son point optimal. Cela aide à expliquer pourquoi un essai clinique initial d’un anticorps stimulant TREM2 a échoué et suggère que les futurs essais pourraient devoir mesurer l’activité de TREM2 et l’état microglial au fil du temps, peut‑être par imagerie cérébrale, pour sélectionner les bons patients et le bon moment de traitement. En bref, ce travail reconfigure TREM2 comme un « variateur » finement réglable du métabolisme et du nettoyage microglial, plutôt que comme un simple interrupteur, et offre une feuille de route pour des immunothérapies de l’Alzheimer plus intelligentes et mieux ciblées.
Citation: Feiten, A.F., Dahm, K., Schlepckow, K. et al. TREM2 expression level is critical for microglial state, metabolic capacity and efficacy of TREM2 agonism. Nat Commun 17, 2002 (2026). https://doi.org/10.1038/s41467-026-68706-8
Mots-clés: microglie, TREM2, maladie d’Alzheimer, métabolisme cérébral, immunothérapie