Clear Sky Science · fr
Microscopie à illumination structurée aveugle haute vitesse via déroulage algorithmique non supervisé
Des films plus nets de la vie à l'intérieur des cellules
La biologie moderne repose souvent sur l'observation de cellules vivantes en action, mais de nombreuses structures clés sont tout simplement trop petites et trop rapides pour être saisies nettement par des microscopes ordinaires. Cet article présente une nouvelle méthode pour transformer des images floues acquises rapidement en films nets et ultra détaillés en temps réel, sans nécessiter de matériel parfaitement réglé. La méthode, appelée microscopie à illumination structurée aveugle déroulée (UBSIM), promet de rendre l'imagerie cellulaire avancée et à haute vitesse plus accessible aux laboratoires de biologie courants.
Pourquoi les microscopes classiques sont insuffisants
Les microscopes optiques traditionnels sont limités par la diffraction, une propriété fondamentale de la lumière qui brouille les détails fins plus petits que quelques centaines de nanomètres. La microscopie à illumination structurée (SIM) contourne cela en projetant une lumière structurée sur l'échantillon et en utilisant l'interférence résultante pour extraire du détail supplémentaire, doublant approximativement la résolution. Cependant, la SIM classique exige des motifs d'illumination précisément connus et une calibration soigneuse, ce qui peut être coûteux et fragile. Une variante plus récente, la blind‑SIM, assouplit ces contraintes matérielles en permettant des motifs aléatoires et en résolvant simultanément l'échantillon et l'illumination à partir des données elles‑mêmes. L'inconvénient est que ce processus de résolution est lent et itératif, prenant des secondes à des minutes par image—beaucoup trop lent pour des films en temps réel de cellules vivantes.
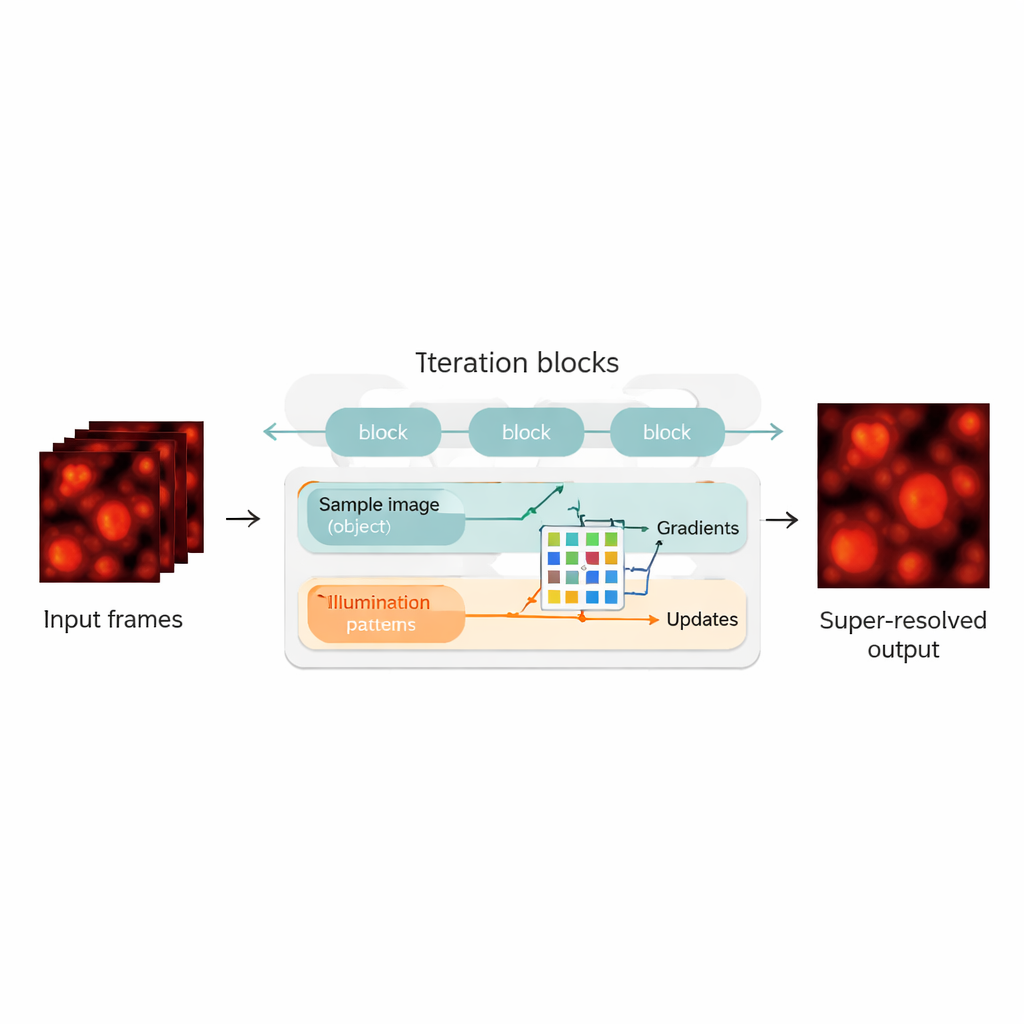
Allier la physique aux réseaux neuronaux
Les auteurs comblent ce fossé en reconfigurant la reconstruction blind‑SIM comme un hybride entre un modèle fondé sur la physique et un réseau neuronal. Ils « déroulent » l'algorithme itératif original—chaque itération devient une couche d'un réseau neuronal, formant une chaîne de blocs de mise à jour. Dans chaque bloc, la méthode évalue dans quelle mesure l'estimation actuelle de l'échantillon et de l'illumination explique les images mesurées, calcule des gradients (directions d'amélioration), puis les transmet à un réseau neuronal convolutionnel compact. Ce réseau apprend à effectuer des corrections plus intelligentes, jouant un rôle semblable à un accélérateur automatiquement optimisé de l'algorithme initial. Fait crucial, UBSIM est entraîné de manière non supervisée : au lieu d'avoir besoin d'images parfaites comme vérité terrain, il n'exige que le modèle physique de la propagation de la lumière dans le microscope. Cela réduit le risque que le réseau « hallucine » des structures plausibles mais incorrectes.
Rapide, précis et moins sujet aux conjectures
Pour évaluer UBSIM, l'équipe a d'abord utilisé des images de microscopie simulées où les structures sous‑jacentes sont connues. Ils ont montré qu'UBSIM restitue une résolution environ deux fois supérieure à celle des images en champ clair ordinaires, comparable à la blind‑SIM standard, mais s'exécute deux à trois ordres de grandeur plus rapidement—une image 256×256 peut être reconstruite en environ 10 millisecondes au lieu de plusieurs secondes. Les scores de qualité d'image, incluant l'erreur, la similarité et le rapport signal‑sur‑bruit, se sont tous nettement améliorés par rapport aux images conventionnelles. UBSIM s'est également avéré plus fiable que les réseaux de super‑résolution profonds populaires lorsqu'on le confronte à des données inhabituelles. Là où des réseaux standard entraînés sur un type de structure avaient tendance à imposer ce motif à de nouveaux échantillons différents—introduisant des artefacts subtils mais trompeurs—UBSIM a conservé une fidélité cohérente, car il est ancré dans la physique de l'imagerie plutôt que seulement dans des exemples visuels.
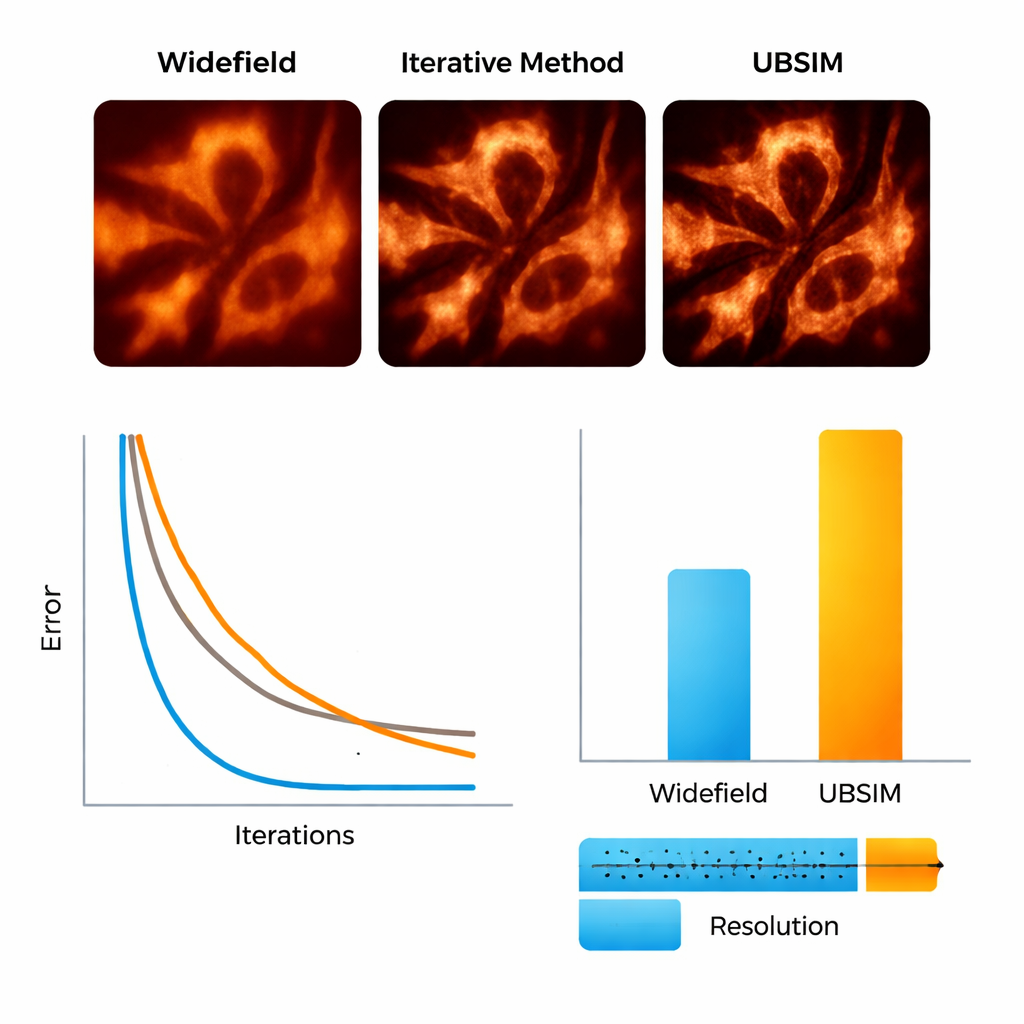
Voir les squelettes et les membranes cellulaires en mouvement
Les chercheurs sont ensuite passés à des échantillons biologiques réels. En utilisant une configuration flexible qui projette des motifs de speckle aléatoires sur des cellules vivantes, ils ont imagé des filaments d'actine—l'« échafaudage » protéique à l'intérieur des cellules—et le réticulum endoplasmique (RE), un réseau membranaire ramifié impliqué dans la production de protéines et les réponses au stress. Avec UBSIM, des fibres d'actine qui apparaissaient comme des bandes floues dans les images ordinaires sont devenues des brins nettement séparés, la résolution passant d'environ 300 nanomètres à environ 150 nanomètres. Plus frappant encore, UBSIM a permis une super‑résolution à cadence vidéo : en capturant des données brutes jusqu'à 100 images par seconde et en reconstruisant jusqu'à 50 images super‑résolues par seconde, l'équipe a pu observer les tubules du RE croître, s'effondrer et se réorganiser en temps réel. Ces dynamiques, se déroulant en fractions de seconde à quelques secondes, sont habituellement difficiles à visualiser avec suffisamment de détails.
Ce que cela signifie pour l'imagerie cellulaire future
Pour les non‑spécialistes, l'essentiel est que UBSIM rend beaucoup plus pratique l'observation en temps réel de petites structures cellulaires en mouvement, avec une clarté au‑delà des limites normales des microscopes optiques—le tout sans exiger une calibration matérielle parfaite ni des jeux de données d'entraînement massifs. En combinant la fiabilité des modèles fondés sur la physique avec la rapidité des réseaux neuronaux modernes, cette approche transforme des piles d'images bruitées et structurées en films ultra‑nets et dignes de confiance, assez rapides pour des expériences de routine. À mesure que la méthode sera affinée et associée à de meilleures stratégies d'illumination, elle pourrait aider les chercheurs à explorer comment des organites comme le RE répondent au stress, comment le cytosquelette se réorganise lors du mouvement ou de la division cellulaire, et comment les maladies altèrent l'architecture cellulaire à l'échelle nanométrique.
Citation: Burns, Z., Zhao, J., Sahan, A.Z. et al. High-speed blind structured illumination microscopy via unsupervised algorithm unrolling. Nat Commun 17, 1967 (2026). https://doi.org/10.1038/s41467-026-68693-w
Mots-clés: microscopie à super‑résolution, illumination structurée, apprentissage profond, imagerie de cellules vivantes, dynamique du réticulum endoplasmique