Clear Sky Science · fr
Dispersion géographique de la résistance aux antimicrobiens après distribution massive d’azithromycine
Pourquoi cela compte pour la santé des enfants
L’azithromycine, un antibiotique courant, a été utilisée dans des campagnes de distribution de masse pour sauver la vie des jeunes enfants dans certaines régions d’Afrique subsaharienne, notamment au Niger. Ces campagnes ont réduit la mortalité infantile mais ont soulevé une inquiétude majeure : pourraient-elles aussi favoriser la propagation de bactéries résistantes depuis les villages traités vers des communautés voisines qui ne reçoivent jamais le médicament ? Cette étude interroge si un tel « spillover » de la résistance a lieu entre villages, une question clé pour les pays qui évaluent les avantages et les risques d’élargir ces programmes.
Campagnes salvatrices et risque caché
De grands essais antérieurs ont montré que l’administration d’azithromycine deux fois par an à tous les jeunes enfants dans des zones à forte mortalité réduit les décès d’environ 14 à 18 %. Ce succès a incité l’Organisation mondiale de la Santé et des gouvernements comme celui du Niger à envisager une utilisation plus large de cette stratégie. Pourtant, les antibiotiques ne tuent pas seulement les bactéries nuisibles ; ils favorisent aussi la survie de souches capables de leur résister. Dans des travaux précédents, la même équipe de recherche a observé des signes nets de bactéries résistantes à l’azithromycine chez les enfants traités. Ce qui n’était pas établi, c’est si ces microbes résistants restent confinés aux villages traités ou s’ils se déplacent vers l’extérieur, compromettant l’efficacité des antibiotiques pour d’autres.
Suivre la résistance à travers un paysage rural
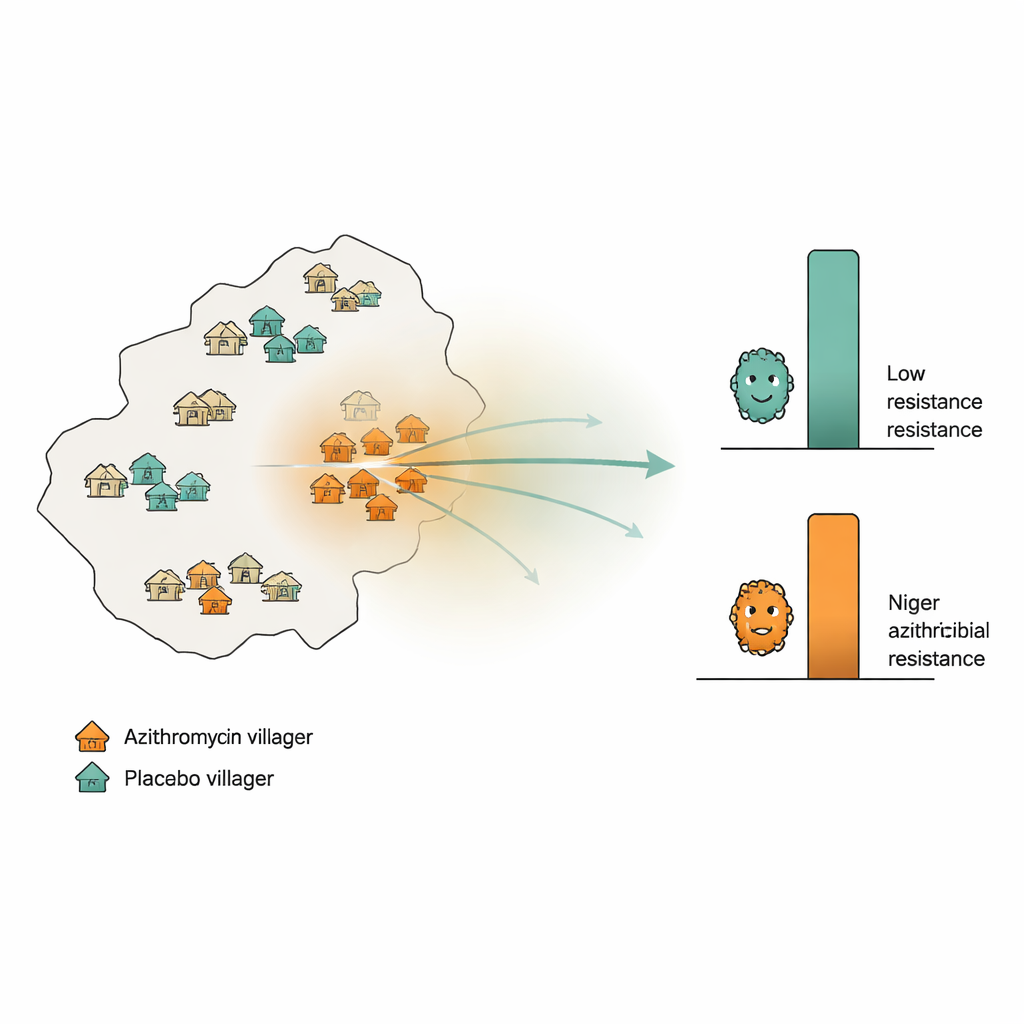
Les chercheurs ont tiré parti d’un grand essai sur la survie infantile dans la région de Dosso au Niger, où 594 villages avaient été assignés de façon aléatoire pour recevoir de l’azithromycine ou un placebo inactif deux fois par an pendant deux ans. De plus, 30 villages « de surveillance » distincts ont été choisis au hasard : la moitié a reçu de l’azithromycine, l’autre moitié le placebo. À partir de ces villages de surveillance, l’équipe a collecté des écouvillons rectaux chez 10 enfants par village au début de l’essai puis à nouveau après 24 mois. Grâce à un séquençage profond de l’ADN, ils ont mesuré le nombre moyen de gènes associés à la résistance aux antibiotiques macrolides (la classe incluant l’azithromycine) présents dans chaque village. Ils ont aussi calculé, pour chaque village de surveillance, l’intensité d’utilisation de l’azithromycine dans la zone environnante : en comptant toutes les doses administrées dans les villages voisins et en pondérant davantage les villages les plus proches.
Rechercher des signes de propagation entre villages
Si la résistance se propageait géographiquement, les chercheurs s’attendaient à observer des niveaux plus élevés de gènes de résistance dans les villages traités par placebo qui se trouvaient entourés de voisins fortement traités, comparés aux villages placebo situés dans des zones où l’utilisation d’azithromycine était faible. Ils ont testé cette idée de plusieurs manières : en examinant de simples corrélations de rang entre l’intensité du traitement local et la résistance ; en répétant l’analyse sur différentes bandes de distance (dans un rayon de 10, 20 ou 30 kilomètres) ; et en utilisant une stratégie rigoureuse de permutation qui remélangeait les étiquettes de traitement dans l’essai plus large pour voir si des motifs apparents pouvaient surgir par hasard. Ils ont également effectué une analyse de « contrôle négatif » répétant les mêmes calculs en utilisant les doses de placebo au lieu des doses d’azithromycine ; un motif similaire dans ce cas suggérerait une confusion plutôt qu’un véritable spillover.
Ce que les données ont révélé sur la résistance
À travers toutes ces vérifications, les villages placebo ont présenté de faibles niveaux de gènes de résistance aux macrolides qui sont restés proches de leurs niveaux de référence, quelle que soit l’intensité d’utilisation d’azithromycine autour d’eux. Les tests statistiques n’ont montré aucun lien significatif entre l’utilisation de médicaments environnante et la résistance dans ces communautés non traitées. En revanche, les villages dont les propres enfants ont reçu de l’azithromycine ont montré une augmentation marquée des gènes de résistance sur la période de deux ans, cohérente avec une sélection directe liée au traitement — mais cette augmentation ne s’est pas systématiquement renforcée dans les zones à plus forte intensité de traitement environnante. Lorsque les chercheurs ont examiné des bactéries pneumococciques vivantes prélevées dans le nez des enfants, ils n’ont de nouveau trouvé aucune relation entre l’intensité géographique du traitement et la résistance. Des analyses utilisant différents modèles mathématiques et des définitions alternatives de l’intensité du traitement ont abouti à la même conclusion générale.
Limites, réserves et perspective générale
L’étude ne peut pas complètement exclure de faibles effets de spillover, d’autant qu’un seul échantillon de 30 villages de surveillance a été testé de manière intensive, et elle n’a pas examiné la propagation à très petite échelle au sein des ménages ou d’un même village. Elle suppose également que la distance et le nombre de doses sont les principaux moteurs d’une éventuelle propagation, et elle se concentre sur une fenêtre de deux ans ; des effets à plus long terme ou des conceptions de programmes différentes, comme des traitements communautaires complets pour des maladies oculaires, pourraient montrer d’autres schémas. Malgré tout, les preuves suggèrent que dans ce contexte, l’essentiel de la pression de sélection pour la résistance induite par les campagnes massives d’azithromycine reste confiné aux communautés qui reçoivent effectivement le médicament, plutôt que de se répandre silencieusement sur le paysage.
Ce que cela signifie pour les campagnes antibiotiques à venir
Pour les responsables de la santé de pays comme le Niger, ces résultats apportent une assurance prudente. Si les traitements massifs à l’azithromycine augmentent bien la résistance aux antibiotiques au sein des villages traités, cette étude n’a pas trouvé de signes forts que cette résistance se propage vers les villages voisins non traités sur 24 mois. Cela signifie que les estimations antérieures du risque de résistance issues de ces essais de survie infantile sont peu susceptibles d’être fortement déformées par un spillover géographique non reconnu. Les décideurs doivent toujours mettre en balance les bénéfices qui sauvent des vies de ces campagnes et l’augmentation locale de la résistance, mais ils peuvent le faire avec plus de confiance qu’au moins à moyen terme et à l’échelle villageoise, le problème ne se diffuse pas rapidement vers l’extérieur.
Citation: Srivathsan, A., Arzika, A.M., Maliki, R. et al. Geographic spillover of antimicrobial resistance from mass distribution of azithromycin. Nat Commun 17, 2152 (2026). https://doi.org/10.1038/s41467-026-68691-y
Mots-clés: résistance aux antimicrobiens, azithromycine, administration de masse de médicaments, mortalité infantile, Niger