Clear Sky Science · fr
Perspectives fonctionnelles et structurelles des interactions entre β-arrestine 1 et Gαs ou Gαi1
Pourquoi cela importe pour la santé et la médecine
Beaucoup de médicaments actuels, des antihistaminiques aux traitements cardiaques et psychiatriques, agissent en ciblant une vaste famille de protéines membranaires appelées récepteurs couplés aux protéines G (RCGP ou GPCR). Ces récepteurs transmettent des messages à l’intérieur de la cellule en s’appuyant sur deux aides principales : les protéines G et des protéines appelées beta-arrestines. Cette étude examine la façon dont une beta-arrestine (beta-arrestine 1) communique directement avec deux types de protéines G à l’intérieur de la cellule. Comprendre cette conversation cachée pourrait aider les scientifiques à concevoir des médicaments plus ciblés et mieux tolérés en ajustant finement la circulation des signaux au sein de nos cellules.
Deux messagers majeurs à l’intérieur de nos cellules
Quand une hormone ou un médicament se lie à un GPCR à la surface cellulaire, il déclenche deux grandes voies de communication. Une voie utilise les protéines G, qui s’activent et se désactivent comme des minuteries moléculaires en échangeant un petit nucléotide (GDP) contre un autre (GTP). L’autre voie utilise les beta-arrestines, qui peuvent à la fois arrêter la signalisation via les protéines G et initier leurs propres voies de signalisation. Pendant longtemps, les chercheurs ont surtout étudié séparément la façon dont les récepteurs s’adressent aux protéines G ou aux beta-arrestines. Des travaux plus récents ont suggéré que protéines G et beta-arrestines pourraient aussi interagir entre elles ou même former de grands « mégacomplexes » avec le récepteur. Mais les détails de ces connexions et leurs conséquences pour la signalisation restaient flous.
Mesurer qui se lie à qui
Dans cette étude, les auteurs se sont focalisés sur la beta-arrestine 1 et sur deux sous-unités alpha des protéines G : Gαs, qui stimule généralement l’activité cellulaire, et Gαi1, qui la réduit habituellement. En utilisant une technique de liaison sensible, ils ont testé l’affinité des liaisons entre la beta-arrestine 1 purifiée et chaque protéine G dans différentes conditions. Ils ont constaté que le facteur clé n’est pas l’état « on » ou « off » de la protéine G, mais l’état de la beta-arrestine 1, plus active et flexible. Une version de la beta-arrestine 1 dépourvue de sa queue — qui se comporte comme un ensemble lâche et actif de conformations — se lie fortement à la fois à Gαs et à Gαi1. En revanche, la forme au repos de la beta-arrestine 1, ou une forme verrouillée par un peptide imitant la queue d’un récepteur, se lie faiblement voire pas du tout. Cela suggère que les protéines G reconnaissent préférentiellement la beta-arrestine 1 lorsqu’elle adopte des conformations proches de l’état actif qui peuvent exister après l’activation du récepteur. 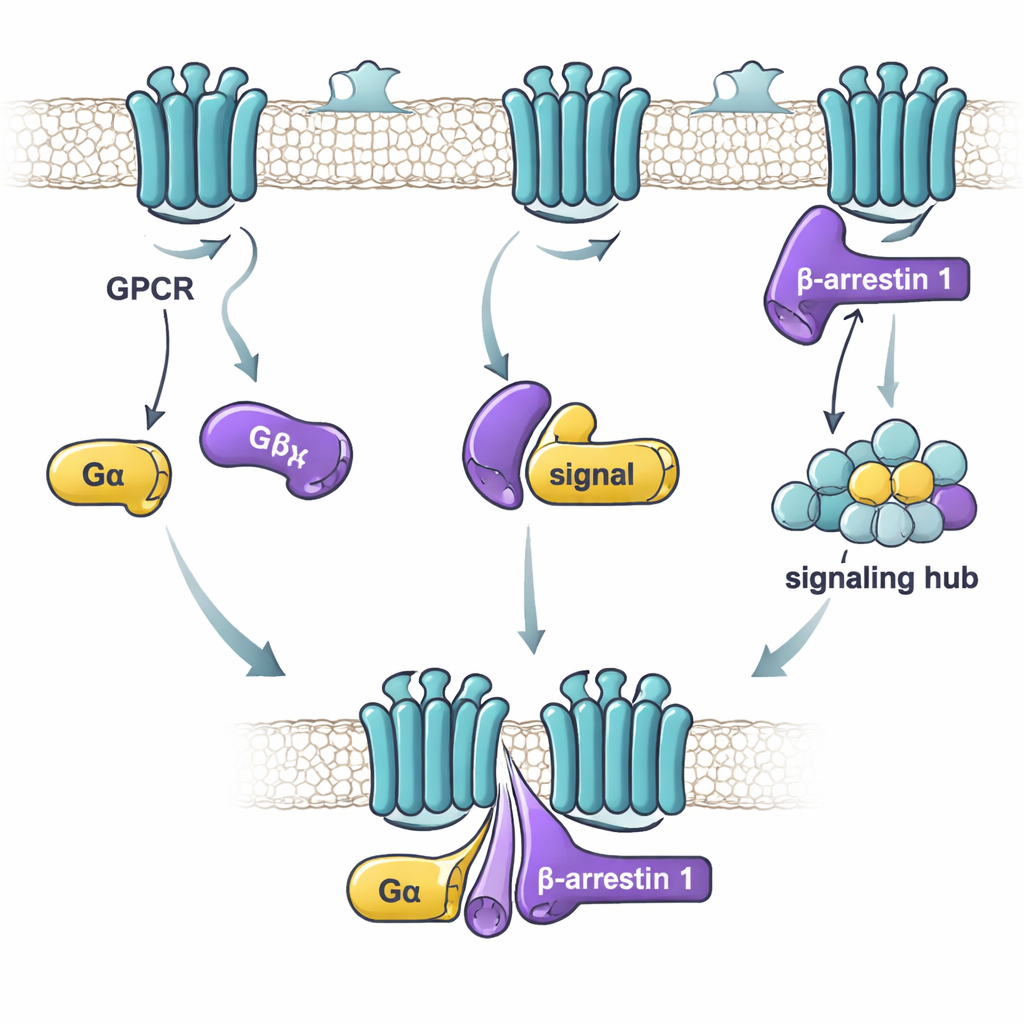
Observer de subtiles modifications de conformation
Pour voir comment la liaison affecte la conformation des protéines, l’équipe a utilisé une méthode suivant la vitesse d’échange des hydrogènes du squelette protéique avec l’hydrogène lourd du solvant. Un échange plus lent signifie généralement qu’une région est devenue plus protégée ou rigide ; un échange plus rapide indique qu’elle est devenue plus flexible ou exposée. Lorsque le fragment de beta-arrestine 1 de type actif s’est lié à Gαs ou Gαi1, les deux protéines G ont présenté des changements de motif clairs dans plusieurs régions, indiquant qu’elles se remodelaient autour du complexe. En revanche, la beta-arrestine 1 elle-même n’a été que légèrement modifiée, principalement au niveau de boucles flexibles. En travaillant avec des domaines isolés des protéines G, les chercheurs ont également montré que la portion catalytique principale de type Ras et la partie hélicoïdale alpha environnante contribuent à la liaison. Pour Gαs, la région hélicoïdale joue un rôle particulièrement important ; pour Gαi1, les deux régions comptent à peu près pour autant.
Fonction sans basculer l’interrupteur principal
La question suivante était de savoir si ce contact direct modifie l’activation des protéines G. L’équipe a utilisé une sonde fluorescente mimant le GTP qui s’éclaire quand une protéine G passe du GDP au GTP, un indicateur standard d’activation. De manière surprenante, l’ajout de beta-arrestine 1 n’a pas modifié la vitesse ni l’étendue de cet échange de nucléotide pour Gαs ou Gαi1. En d’autres termes, la beta-arrestine 1 n’agit pas comme une enzyme classique de mise « sur on » des protéines G. Son influence se manifeste plutôt sur sa propre structure. En employant une beta-arrestine 1 ingénieusement conçue dont le mouvement de la queue C-terminale pouvait être suivi par fluorescence, ils ont observé que Gαs actif, mais pas Gαi1, favorise le relâchement de la queue C-terminale de la beta-arrestine en présence d’un peptide dérivé du récepteur. Dans des cellules vivantes, des images complémentaires et des capteurs de transfert d’énergie ont confirmé que Gαs et la beta-arrestine 1 se rapprochent lors de la stimulation hormonale et que Gαs aide à pousser la beta-arrestine 1 vers une conformation plus active. 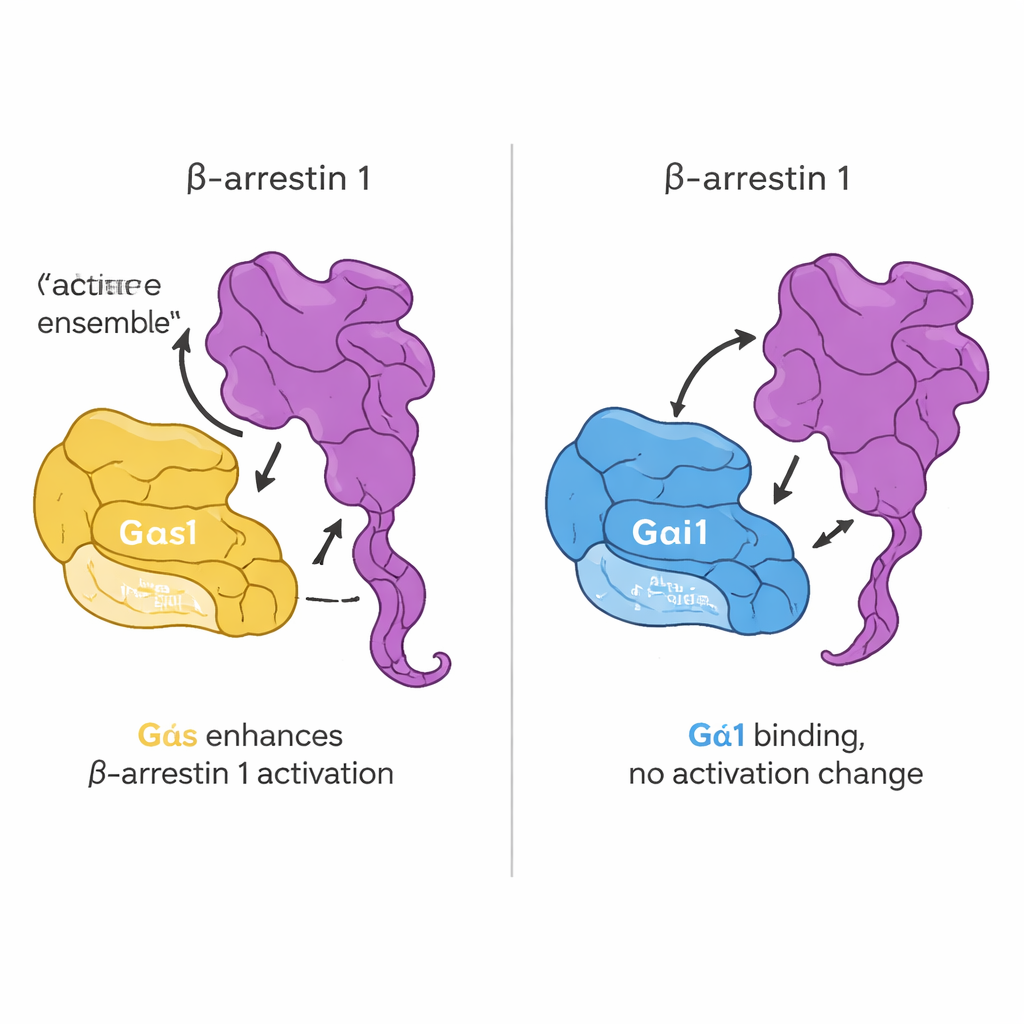
Une nouvelle couche de régulation dans la signalisation cellulaire
En rassemblant ces résultats, l’étude propose que Gαs et Gαi1 se lient directement à la beta-arrestine 1, mais de manières légèrement différentes et avec des conséquences distinctes. Aucune des deux protéines G ne voit son comportement principal d’activation/désactivation modifié par ce contact. À la place, en particulier pour Gαs, l’interaction agit plutôt comme un bouton de réglage fin sur la beta-arrestine 1, la poussant ou la stabilisant dans une forme plus active avec la queue libérée. Cela ajoute une couche jusque-là sous-estimée à la signalisation des GPCR : non seulement les récepteurs peuvent coordonner protéines G et beta-arrestines, mais protéines G et beta-arrestines peuvent aussi se moduler directement entre elles. À long terme, cartographier ces interactions subtiles pourrait aider les concepteurs de médicaments à orienter la signalisation vers des voies bénéfiques — en renforçant les voies utiles tout en évitant celles qui provoquent des effets indésirables.
Citation: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Mots-clés: Récepteurs couplés aux protéines G, beta-arrestine, signalisation des protéines G, mécanismes de signalisation cellulaire, biologie structurale