Clear Sky Science · fr
Analyse épigénomique à l’échelle du génome identifie des méthylations de l’ADN médiatrices du risque cardiométabolique lié au traitement chez les survivants du cancer de l’enfance
Pourquoi les séquelles du cancer persistent dans l’organisme
Grâce à des traitements améliorés, la plupart des enfants atteints de cancer survivent aujourd’hui à l’âge adulte. Mais nombre de ces survivants font face des décennies plus tard à de nouveaux problèmes de santé, notamment l’obésité, l’hypertension et des troubles semblables au diabète. Cette étude pose une question cruciale : comment les traitements administrés pendant l’enfance laissent-ils de telles répercussions durables sur le cœur et le métabolisme ? En examinant les marques chimiques portées par l’ADN dans les cellules sanguines, les chercheurs mettent au jour des indices montrant que la chimiothérapie et la radiothérapie passées peuvent « reprogrammer » l’organisme d’une manière qui augmente le risque cardiométabolique à long terme.
Suivre les risques cachés chez les survivants adultes
L’équipe a étudié près de 3 000 adultes survivants d’un cancer de l’enfance suivis dans la cohorte de longue durée St. Jude Lifetime Cohort. Ces survivants avaient reçu durant l’enfance diverses chimiothérapies et des radiations dirigées vers le cerveau ou le tronc (thorax, abdomen, pelvis), puis sont revenus des années plus tard pour des bilans de santé détaillés et des analyses sanguines. Les scientifiques se sont concentrés sur cinq problèmes cardiométaboliques clés connus pour augmenter le risque de maladie cardiaque et de mortalité précoce : obésité, glycémie anormale, hypertriglycéridémie, hypercholestérolémie et hypertension. En comparant les survivants avec et sans ces affections, ils ont recherché, à travers des millions de positions du génome, des différences de méthylation de l’ADN — de minuscules interrupteurs chimiques qui contribuent à contrôler l’activation ou la répression des gènes.
Les marques chimiques sur l’ADN comme mémoire du traitement
À l’échelle du génome, les chercheurs ont identifié près de 1 900 sites d’ADN dont les niveaux de méthylation étaient associés à au moins une des cinq affections cardiométaboliques. La plupart de ces sites étaient liés à un seul problème, mais un petit groupe semblait faire office de « nœuds » connectés à plusieurs affections. Cinq sites clés, situés à proximité de deux gènes nommés CPT1A et LMNA, étaient associés simultanément aux cinq risques cardiométaboliques. Ces gènes influencent la gestion des lipides et la structure cellulaire, ce qui suggère que le traitement peut perturber des voies métaboliques et cardiovasculaires communes. De nombreuses modifications de méthylation recoupaient des signaux déjà observés chez la population générale, notamment ceux liés à l’inflammation, tandis que d’autres semblaient spécifiques aux survivants du cancer — suggérant que le traitement laisse une empreinte biologique propre.
Relier thérapie, modifications de l’ADN et maladie
La démarche suivante consistait à tester si ces modifications de méthylation contribuent réellement à expliquer comment le traitement conduit à une maladie ultérieure, plutôt que d’être de simples marqueurs associés. Les chercheurs se sont concentrés sur des problèmes cardiométaboliques nouveaux ou aggravés qui sont apparus seulement après la prise de l’échantillon sanguin, préservant ainsi la chronologie : traitement → modification de l’ADN → maladie. À l’aide d’analyses de médiation statistiques, ils ont identifié 24 sites de méthylation qui, ensemble, expliquaient jusqu’à environ un quart du lien entre des traitements spécifiques et des problèmes cardiométaboliques ultérieurs. La radiothérapie du cerveau et du tronc montrait des schémas particulièrement marqués : des groupes de sites de méthylation expliquaient globalement environ 10–20 % de l’impact de ces radiothérapies sur les anomalies de la glycémie. Un site notable, près d’un gène nommé ANTXR2, semblait médiatiser environ 20 % de l’effet de la radiothérapie du tronc sur les troubles glycémique ultérieurs.
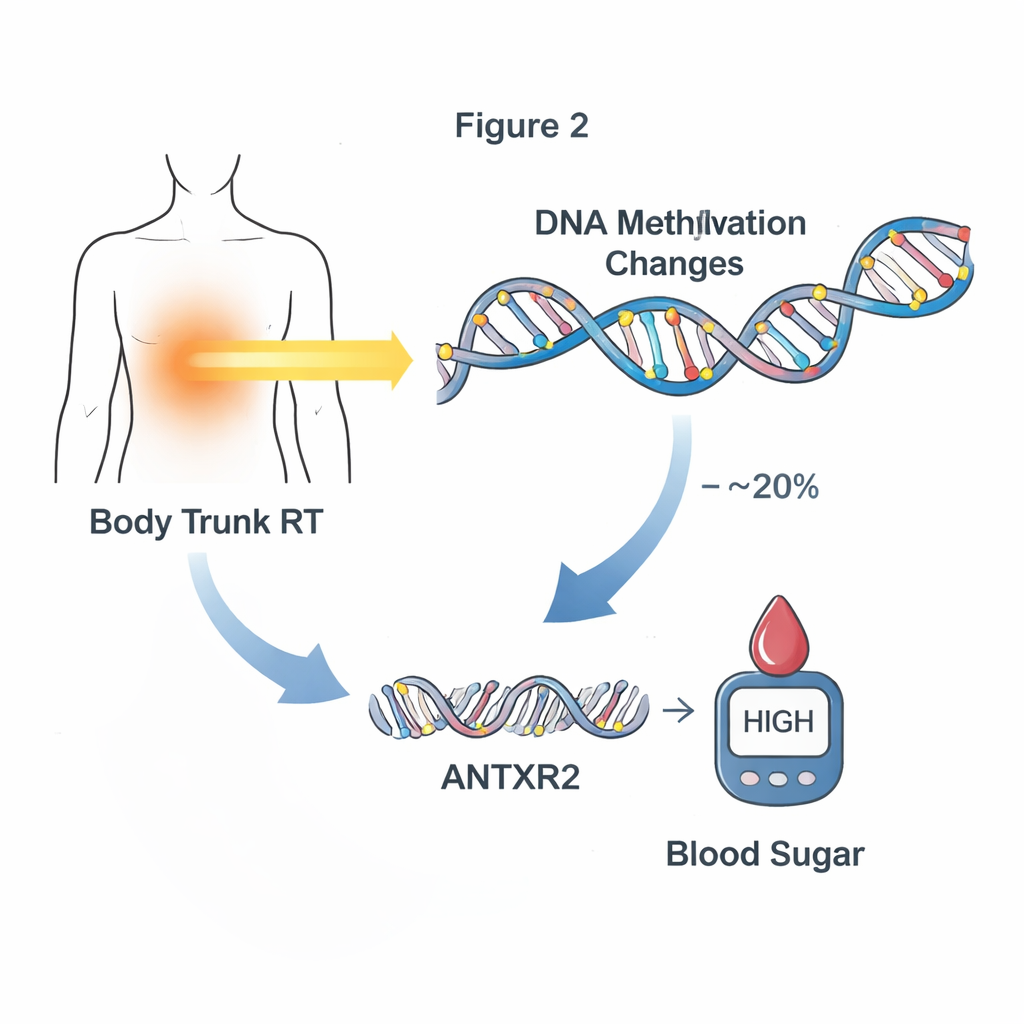
Des marques d’ADN à l’activité des gènes
Pour comprendre comment ces marques de méthylation pouvaient modifier la biologie, l’équipe a examiné l’activité génique dans un sous‑groupe de survivants disposant à la fois de données ADN et ARN issues de leur sang. Ils ont trouvé des dizaines de sites de méthylation où des niveaux plus élevés ou plus faibles étaient liés à des modifications de l’expression génique voisine. Parmi eux se trouvait le site médiateur clé près de ANTXR2, dont les niveaux de méthylation étaient fortement corrélés à l’expression de ce gène, en particulier chez les survivants ayant reçu une radiothérapie du tronc. ANTXR2 participe à la régulation des vaisseaux sanguins et de la matrice tissulaire environnante — des systèmes qui influencent le flux de glucose et d’insuline dans l’organisme. Ce schéma suggère une chaîne d’événements dans laquelle la radiation modifie la méthylation, ce qui change l’activité génique, susceptible à son tour de favoriser des anomalies de la glycémie.
Conséquences pour les survivants et les soins futurs
Pour le grand public, le message essentiel est que les traitements du cancer de l’enfance n’endommagent pas seulement les tissus sur le moment ; ils peuvent aussi laisser des « notes » durables sur l’ADN qui façonnent la santé pendant des décennies. Dans cette étude, certaines de ces notes — modifications de la méthylation de l’ADN — contribuent à expliquer pourquoi certains survivants sont plus susceptibles de développer de l’obésité, des anomalies lipidiques ou des troubles de la glycémie liés au diabète et aux maladies cardiaques. Bien que ces marques chimiques ne racontent qu’une partie de l’histoire, elles pourraient à terme servir de biomarqueurs sanguins pour identifier les survivants les plus à risque et pour évaluer si des changements de mode de vie ou de nouvelles thérapies peuvent, en toute sécurité, modifier une partie de cet historique épigénétique. Ce travail rapproche la prise en charge des survivants d’une médecine de précision : utiliser les empreintes moléculaires des traitements passés pour guider une prévention plus précoce et mieux ciblée des maladies cardiaques et métaboliques.
Citation: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Mots-clés: survivants du cancer de l’enfance, méthylation de l’ADN, risque cardiométabolique, radiothérapie, épigénétique