Clear Sky Science · fr
Détermination co-traductionnelle des structures quaternaires dans les usines à chaperons
Comment les « lignes d’assemblage » cellulaires maintiennent les grosses machines en état
À l’intérieur de chacune de nos cellules, des milliers de pièces protéiques doivent s’emboîter pour former des machines moléculaires complexes, des moteurs qui copient l’ADN aux usines qui fabriquent d’autres ARN. Cette étude pose une question apparemment simple mais aux grandes implications : comment les cellules décident-elles, en temps réel, quels protéines aides vont accompagner chaque nouvelle pièce pendant sa synthèse, et comment organisent-elles ce processus dans le milieu fluide et chaotique de la cellule ?
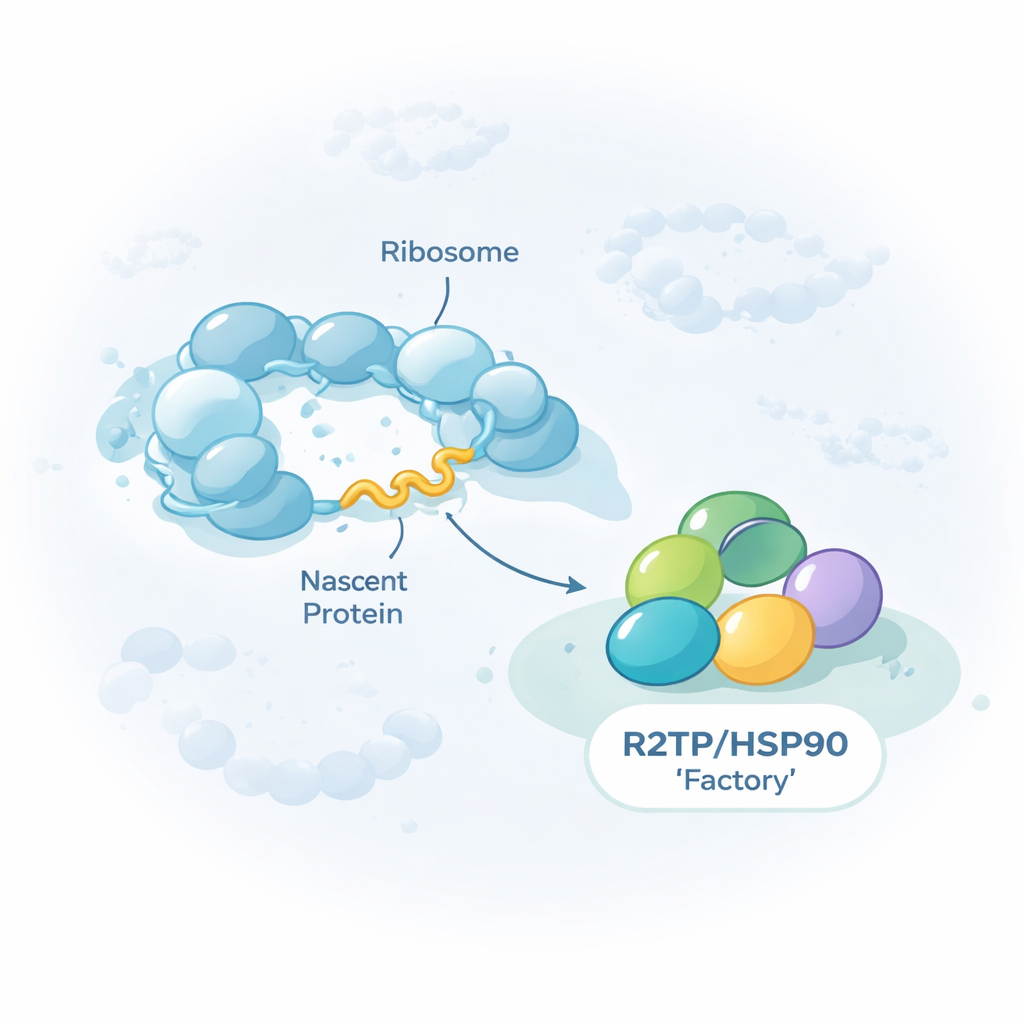
Un aide‑généraliste pour les méga‑machines cellulaires
Le travail se concentre sur un groupe de protéines d’aide, ou chaperons, connus sous le nom HSP90/R2TP. Plutôt que de replier des protéines individuelles, ce chaperon se spécialise dans l’assemblage de complexes géants multi‑composants, y compris les trois ARN polymérases nucléaires qui transcrivent l’ADN en ARN, certains RNP (particules ARN–protéine) et de grandes machines de remodelage qui réorganisent le conditionnement de l’ADN. Les auteurs montrent que R2TP ne rencontre pas simplement ces protéines clientes une fois terminées. Au contraire, il s’y attache souvent alors que chaque cliente est encore en cours de fabrication sur les ribosomes, les machines de synthèse protéique de la cellule. En isolant R2TP à partir de cellules humaines et en séquençant les ARN qui l’accompagnaient, ils ont trouvé environ 150 ARN messagers dont les protéines codées sont en contact avec R2TP pendant leur propre traduction.
Des aides qui accompagnent les chaînes protéiques en croissance
Pour vérifier si cette liaison a lieu réellement pendant la synthèse protéique, l’équipe a utilisé des médicaments qui gèlent ou perturbent la traduction. Lorsqu’ils ont utilisé des composés qui arrachent les chaînes protéiques naissantes des ribosomes, la plupart des ARNm ont disparu de l’empreinte de R2TP. Mais lorsqu’ils ont utilisé un médicament qui met simplement les ribosomes en pause tout en laissant les chaînes naissantes attachées, la liaison de R2TP a augmenté. Des ARNm rapporteurs ingénierisés ont confirmé cela : si la traduction était arrêtée artificiellement tôt, le chaperon ne se liait plus au message. Ensemble, ces résultats indiquent une règle d’engagement claire : R2TP reconnaît ses clientes principalement via la chaîne protéique émergente qui sort du ribosome, plutôt que par la séquence d’ARN elle‑même.
Des « usines » construites par des chaperons qui concentrent des messages spécifiques
En utilisant une imagerie monocouche moléculaire avancée, les auteurs ont ensuite fait une découverte surprenante. Au lieu d’observer de nombreux messages clients différents dispersés au hasard, ils ont vu que certains messages-clés — en particulier ceux codant les grandes sous‑unités de l’ARN polymérase II et un important facteur d’épissage appelé PRPF8 — se regroupaient souvent en foyers lumineux dans le cytoplasme. Ces foyers étaient enrichis en R2TP et son partenaire HSP90, ainsi qu’en composants ribosomiques et les protéines en cours de synthèse, montrant qu’il s’agissait de sites de traduction actifs. Quand la traduction ou l’activité ATPase énergivore de R2TP ou HSP90 était bloquée, ces foyers se dissolvaient. Les auteurs appellent ces structures « usines R2TP » : des condensats spécialisés où certains ARNm et chaperons sont concentrés pour favoriser des contacts rapides et protecteurs entre les chaînes protéiques émergentes et leurs aides d’assemblage.
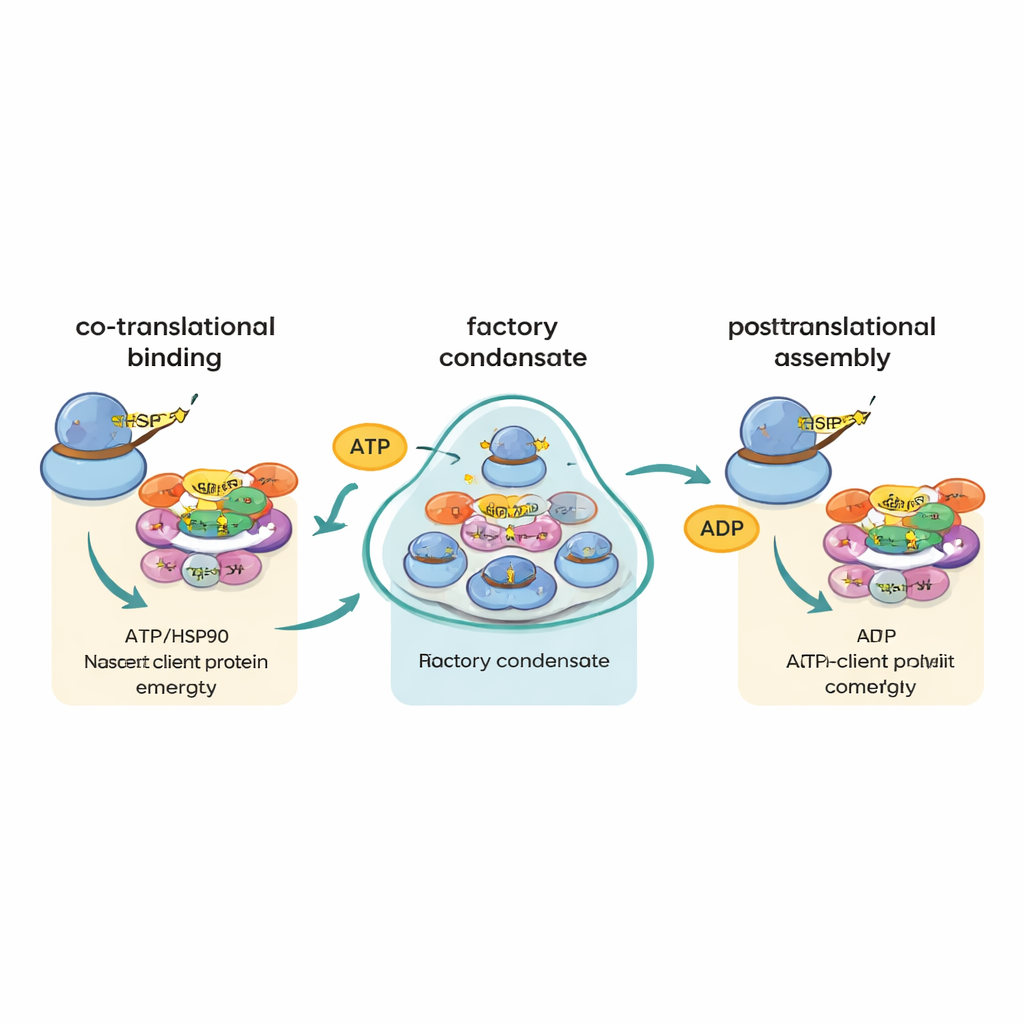
Diriger les pièces sans rapprocher leurs plans
Une idée antérieure était que les messages codant différentes parties d’un même complexe pourraient se retrouver et être traduits côte à côte, permettant à leurs produits protéiques de s’assembler immédiatement. Le nouveau travail écarte en grande partie ce modèle de « plans co‑localisés ». Même pour des paires de protéines connues pour se joindre dans la même machine, leurs ARNm apparaissaient rarement ensemble. À la place, les données soutiennent une stratégie différente que les auteurs appellent « canalisation chaperonne co‑traductionnelle », ou « cha‑cha ». Dans ce schéma, dès qu’une grande protéine ou une protéine sujette à l’assemblage commence à émerger du ribosome, R2TP et HSP90 s’y fixent et déterminent son sort, la guidant à travers les étapes ultérieures d’assemblage. Les usines elles‑mêmes ne rapprochent pas principalement des messages correspondants ; elles augmentent plutôt la probabilité que des protéines nouvelles et vulnérables rencontrent rapidement le chaperon approprié.
Pourquoi cette organisation cachée compte pour la santé et la maladie
En révélant que R2TP et HSP90 non seulement protègent des pièces protéiques fragiles mais aussi façonnent où et comment elles sont traduites, cette étude dévoile un niveau inattendu d’organisation intracellulaire. Le mécanisme cha‑cha aide à expliquer comment les cellules construisent de façon fiable d’énormes complexes moléculaires alors que les messages de leurs composants partagent rarement la même adresse. Il suggère aussi pourquoi des défauts dans les chaperons ou leurs cycles énergétiques peuvent déstabiliser des machines vitales comme l’ARN polymérase et les facteurs d’épissage, avec des conséquences allant de troubles du développement au cancer. En somme, ce travail montre que les cellules s’appuient sur des « usines » chaperonnes dynamiques pour diriger les pièces fraîchement produites vers les bons assemblages, maintenant leur machinerie interne à la fois efficace et ordonnée.
Citation: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Mots-clés: chaperons protéiques, assemblage co-traductionnel, machines moléculaires, ARN polymérase, contrôle qualité cellulaire