Clear Sky Science · fr
Découverte itérative d’antibiotiques polymériques puissants via un apprentissage multi‑étapes et multi‑tâches contre la résistance antimicrobienne
Pourquoi de nouveaux antibiotiques comptent pour tout le monde
Les infections résistantes aux médicaments augmentent dans le monde, rendant des maladies familières plus difficiles, et parfois impossibles, à soigner. Cette étude décrit une nouvelle façon de découvrir rapidement un type différent d’antibiotique : de petits polymères synthétiques capables à la fois de tuer des bactéries résistantes et de réactiver d’anciens médicaments, comme la pénicilline. Les travaux combinent une intelligence artificielle avancée, la chimie et des tests animaux pour explorer un espace chimique immense qui serait impossible à sonder par essais‑erreurs seuls.
À la recherche de nouveaux défenseurs dans un univers chimique encombré
Les antibiotiques traditionnels ciblent généralement des protéines bactériennes spécifiques, que les bactéries peuvent finir par contourner. En revanche, les polymères de cette étude imitent les peptides de défense naturels de notre organisme, qui endommagent physiquement les membranes bactériennes et sont moins sujets à l’apparition de résistances. Le défi tient au fait qu’il existe des dizaines de milliers de structures polymériques possibles, et que leur comportement dépend d’un équilibre délicat entre charge positive, parties hydrophiles et lipophiles. Tester manuellement suffisamment de candidats pour trouver des composés sûrs et puissants prendrait des années. Les auteurs ont construit une bibliothèque combinatoire d’environ 100 000 polymères apparentés appelés poly(β‑amino esters), chacun conçu pour s’autoassembler en particules de taille nanométrique capables d’interagir fortement avec la surface des cellules bactériennes.
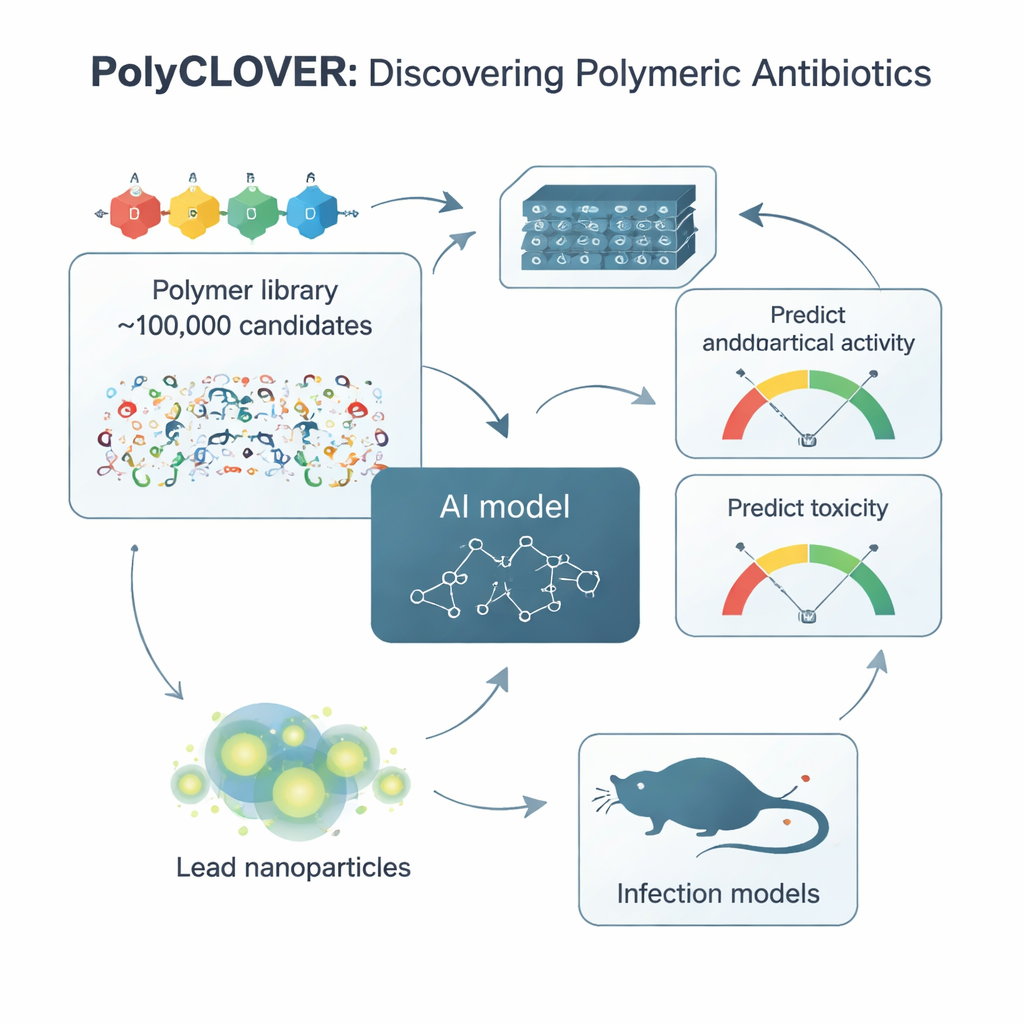
Apprendre à une IA à lire le « langage corporel » des polymères
Pour parcourir cette bibliothèque, l’équipe a créé un cadre qu’elle appelle PolyCLOVER. Au cœur se trouve un réseau neuronal basé sur des graphes qui traite chaque polymère comme un réseau d’atomes connectés, permettant au modèle de percevoir des différences structurelles subtiles. Comme il y avait très peu d’exemples étiquetés indiquant quels polymères étaient de bons ou de mauvais antibiotiques, les chercheurs ont utilisé une stratégie d’apprentissage auto‑supervisé en plusieurs étapes. D’abord, le modèle a été entraîné sur environ un million de structures polymériques non étiquetées pour capter des motifs chimiques généraux. Puis il a été affiné sur la bibliothèque non étiquetée de 100 000 membres, et enfin ajusté sur un petit ensemble de 220 polymères synthétisés et testés pour leur puissance antibactérienne et leur cytotoxicité sur les globules rouges. Cet apprentissage par étapes a nettement amélioré la capacité du modèle à prédire quels nouveaux polymères seraient à la fois puissants et sûrs.
Laisser les expériences et les algorithmes apprendre l’un de l’autre
PolyCLOVER ne s’arrête pas à une seule série de prédictions. Il fonctionne en boucle : l’IA propose les candidats les plus prometteurs et les plus instructifs, les chimistes les synthétisent et les testent en format haut débit, et les nouveaux résultats sont réinjectés pour affiner le modèle. L’étape de sélection utilise une approche dite de « borne supérieure de confiance » qui équilibre l’exploitation (favoriser les polymères prédits performants) et l’exploration (sonder des régions incertaines où le modèle peut le plus apprendre). Sur environ quatre cycles itératifs, les polymères suggérés se sont améliorés de manière continue : ils sont devenus plus puissants contre le Staphylococcus aureus résistant à la méthicilline (SARM) tout en conservant une toxicité acceptable vis‑à‑vis des globules rouges. En seulement 20 jours d’expérimentation, le système a convergé vers un petit ensemble de candidats vedettes.
De minuscules particules autoassemblées qui perforent les bactéries
Les trois polymères leaders finaux, nommés H1, H2 et H3, se sont autoassemblés spontanément en nanoparticules chargées positivement d’environ 100 nanomètres. En laboratoire, ils ont tué le SARM aussi efficacement qu’un antibiotique standard, la streptomycine, et beaucoup plus rapidement : ils ont réduit le nombre de bactéries de plusieurs ordres de grandeur en quelques minutes à heures, même dans du sérum riche en protéines. La microscopie électronique et des sondes fluorescentes ont montré que ces particules s’attachent rapidement à la surface bactérienne et perturbent l’intégrité et le potentiel électrique de la membrane, provoquant la fuite du contenu cellulaire. Fait important, lorsque le SARM a été exposé à ces polymères pendant près d’un mois, les bactéries ont développé très peu de résistance, en net contraste avec la streptomycine, dont la dose efficace a fortement augmenté sur la même période.
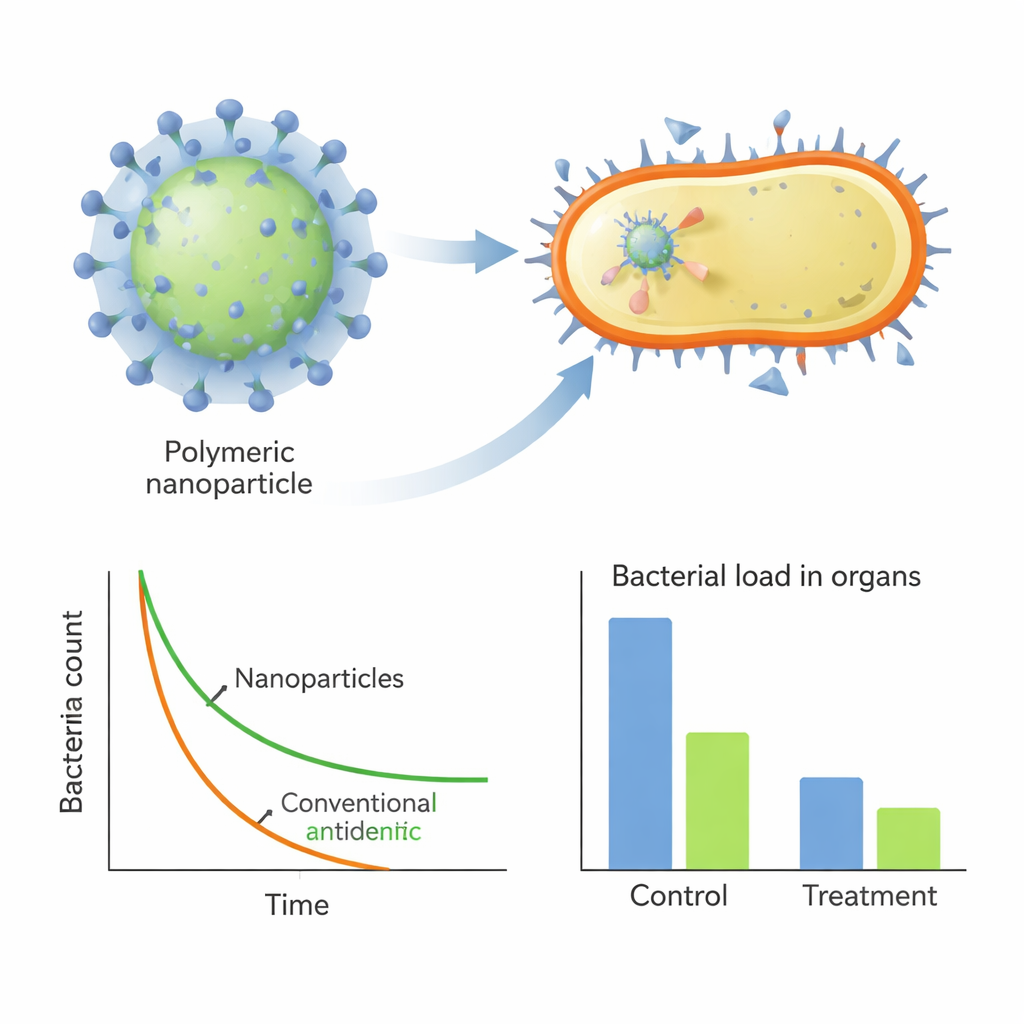
Réactiver de vieux antibiotiques dans des infections animales
Outre leur activité propre, les nanoparticules ont aussi joué le rôle d’adjuvants puissants pour les médicaments traditionnels. Associé à la pénicilline G, à laquelle le SARM est normalement très résistant, le meilleur polymère (H2) a formé des nanocomposites qui emprisonnaient l’antibiotique à l’intérieur de la particule. Ces composites ont montré une forte synergie en laboratoire, réduisant fortement la dose de pénicilline nécessaire pour supprimer le SARM. Dans des modèles murins d’infection pulmonaire et d’une infection abdominale sévère, le traitement par les polymères leaders — seuls ou en combinaison avec la pénicilline — a considérablement réduit la charge bactérienne dans les organes, diminué les signaux inflammatoires dans le sang et limité les lésions tissulaires, le tout sans toxicité évidente.
Un nouveau mode d’emploi pour une découverte d’antibiotiques plus intelligente
Pour le grand public, l’essentiel est que PolyCLOVER montre comment l’IA et les expériences automatisées peuvent s’associer pour découvrir des types entièrement nouveaux d’antibiotiques beaucoup plus rapidement qu’auparavant. Plutôt que de s’en remettre uniquement au hasard et aux criblages lents, cette approche apprend de chaque série de résultats pour se concentrer sur des polymères qui attaquent les bactéries résistantes et transportent les antibiotiques conventionnels plus efficacement. Bien que des travaux supplémentaires soient nécessaires avant que l’un de ces matériaux n’atteigne la clinique, l’étude offre une voie prometteuse pour reconstituer notre arsenal déclinant contre les infections résistantes et suggère une stratégie générale pour concevoir de nombreux autres biomatériaux intelligents.
Citation: Wu, Y., Wang, C., Shen, X. et al. Iterative discovery of potent polymeric antibiotics via multi-stage and multi-task learning against antimicrobial resistance. Nat Commun 17, 1878 (2026). https://doi.org/10.1038/s41467-026-68682-z
Mots-clés: résistance aux antimicrobiens, antibiotiques polymériques, nanoparticules, apprentissage automatique, bactéries résistantes aux médicaments