Clear Sky Science · fr
Perturbation différentielle des lipides membranaires par des antibiotiques lipopeptidiques, la colistine et les turnercyclamycines
Pourquoi cela compte pour les antibiotiques du futur
On estime que les infections résistantes aux médicaments pourraient tuer des dizaines de millions de personnes chaque année d'ici le milieu du siècle, et certains des agents les plus meurtriers sont des bactéries à Gram négatif qui résistent déjà à de nombreux antibiotiques. La colistine est l'un des rares médicaments restants capables de traiter ces infections, mais elle est agressive pour les patients et les bactéries apprennent de plus en plus à y échapper. Cette étude dissèque le mode d'action de la colistine comparé à une nouvelle famille d'antibiotiques naturels appelés turnercyclamycines, révélant que de petits ajustements chimiques peuvent engendrer des façons très différentes de tuer les bactéries — et potentiellement des médicaments plus sûrs.
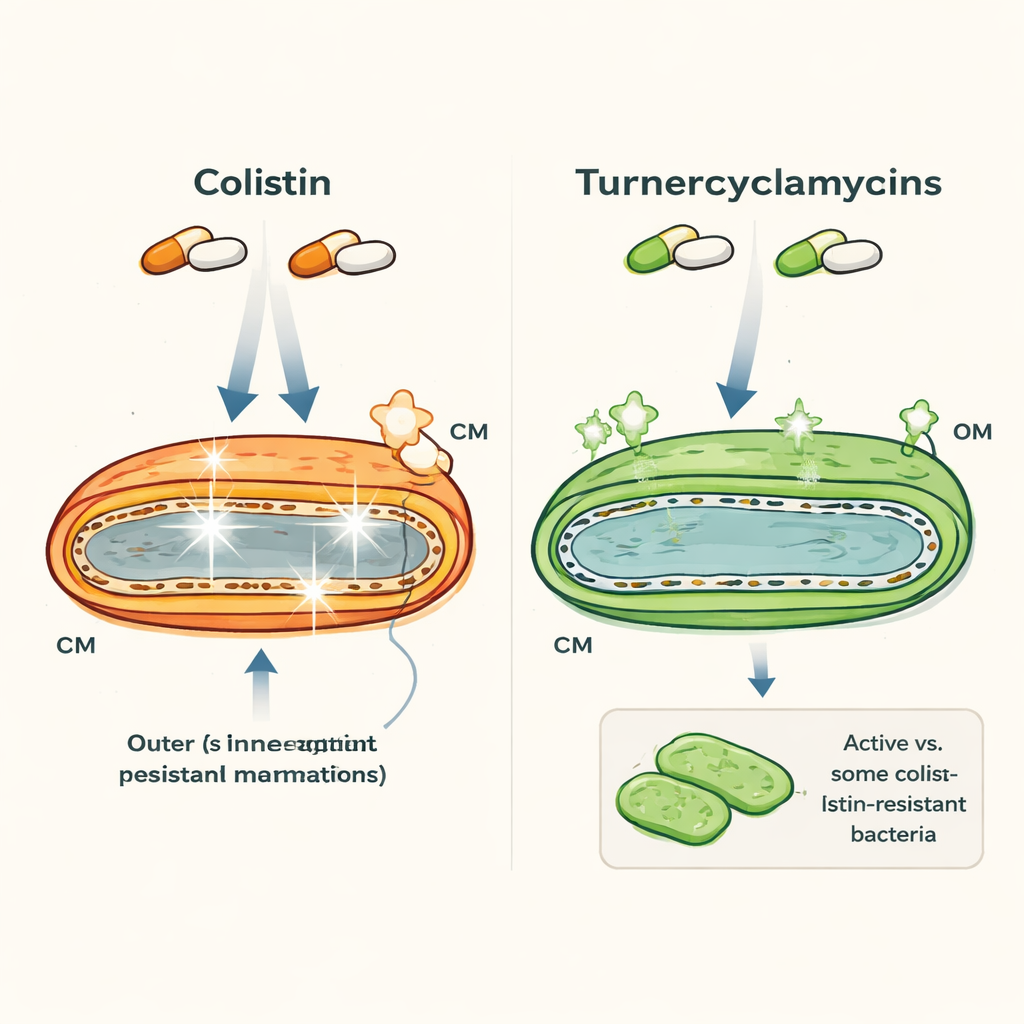
Deux médicaments d'apparence similaire mais de comportements très différents
La colistine et les turnercyclamycines sont tous deux des lipopeptides — des molécules qui combinent une queue lipidique et un anneau peptidique — et ciblent les bactéries à Gram négatif telles que Escherichia coli et Acinetobacter. À première vue elles se ressemblent, mais leurs propriétés divergent fortement. La colistine est un médicament de dernier recours qui agit rapidement mais peut endommager les reins et les nerfs humains, et les bactéries portent de plus en plus des gènes de résistance comme mcr-1. Les turnercyclamycines, découvertes chez des bactéries associées aux shipworms, peuvent tuer nombre des mêmes agents pathogènes, y compris certaines souches résistantes à la colistine, mais montrent beaucoup moins de toxicité dans des tests en laboratoire. Fait intriguant, deux variantes ne différant que par une petite extension de la queue lipidique présentent déjà des profils de résistance différents, ce qui suggère que des caractéristiques structurales très subtiles ont de l'importance.
Comment la colistine perce des trous et les turnercyclamycines prennent leur temps
Les auteurs ont utilisé des colorants fluorescents, des expériences de cinétique de tuerie et la microscopie électronique pour observer comment ces médicaments affectent les membranes bactériennes au fil du temps. La colistine rend rapidement poreuses à la fois la membrane externe et la membrane cytoplasmique interne, entraînant une mort cellulaire rapide en quelques heures. Les turnercyclamycines, en revanche, tuent plus lentement — prenant 6 à 10 heures pour épurer complètement des cultures — et perturbent principalement la membrane externe. Les colorants qui s'allument lorsque la membrane interne est compromise ont montré des signaux forts pour la colistine mais seulement des signaux modestes et retardés pour les turnercyclamycines, et des images en haute résolution ont confirmé peu de dommages visibles à la membrane interne même lorsque les cellules mouraient. Cela indique que les turnercyclamycines ne tuent pas par la voie classique de « formation de pores » utilisée par de nombreux antibiotiques ciblant la membrane.
Les blocs de construction lipidiques comme commandes cachées
Les deux familles de médicaments dépendent en fin de compte d'un composant bactérien appelé lipopolysaccharide (LPS), qui est synthétisé dans la membrane interne puis généralement exporté vers la surface externe. Lorsque les chercheurs ont désactivé les premières étapes de la biosynthèse du LPS, la colistine et les turnercyclamycines perdaient leur activité ; mais lorsqu'ils ont bloqué la machinerie de transport qui déplace le LPS vers l'extérieur, les médicaments fonctionnaient encore. Cela signifie que l'existence des précurseurs du LPS est essentielle, mais pas leur destination finale. Une différence clé est apparue lors de mesures d'interaction directe : la colistine adhère au LPS purifié avec une affinité micromolaire, tandis que les turnercyclamycines n'ont montré aucune liaison mesurable. À la place, les turnercyclamycines étaient fortement influencées par d'autres lipides membranaires. Certains phospholipides, en particulier la phosphatidylglycérol, pouvaient atténuer ou moduler leur activité, et les médicaments étaient facilement capturés par des vésicules de membrane externe — de minuscules bulles lipidiques relâchées par les bactéries.
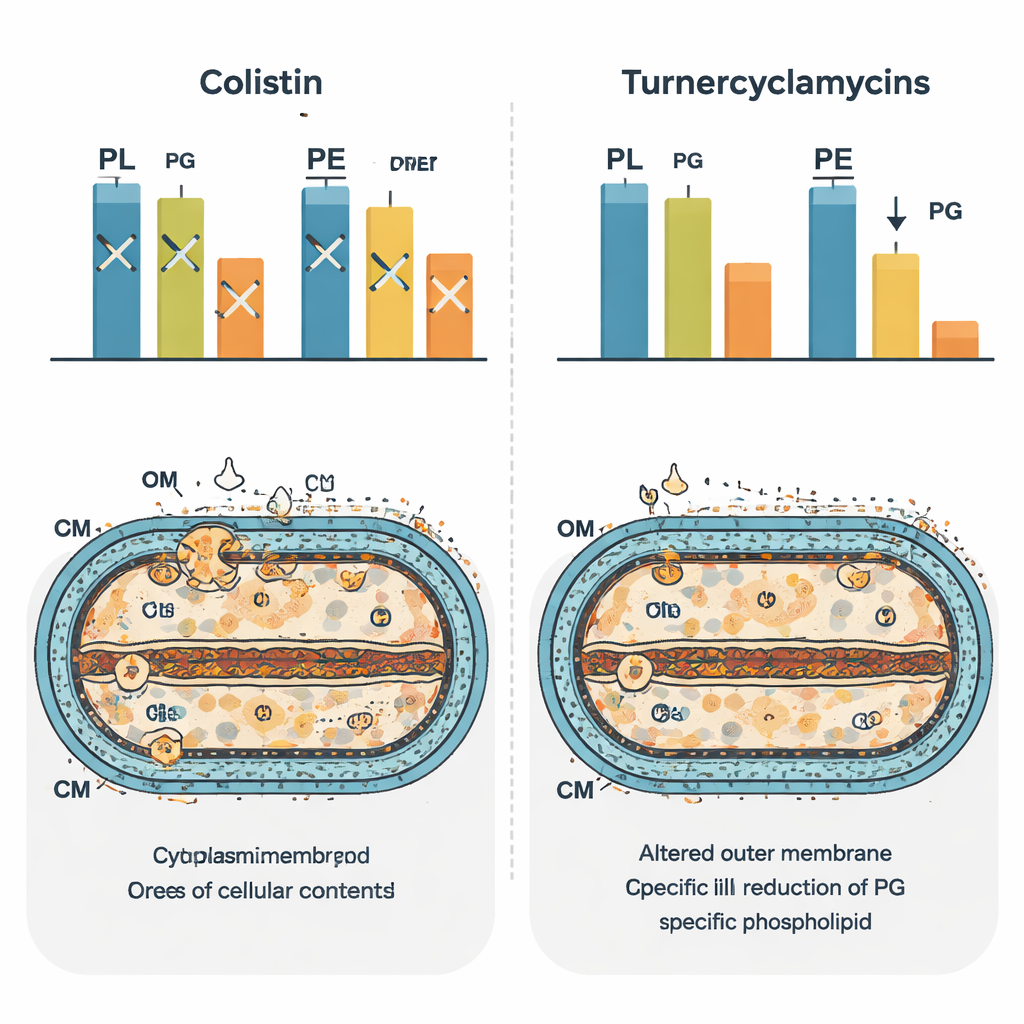
Reconfigurer le paysage lipidique bactérien
Pour voir l'impact plus large sur la cellule, l'équipe a utilisé une « phospholipidomique » par spectrométrie de masse pour inventorier des centaines d'espèces lipidiques après traitement. La colistine a produit un motif distinct de changements, reflétant sa perturbation large de l'homéostasie membranaire. Les turnercyclamycines ont généré une signature différente qui ressemblait étroitement à celle des bactéries dépourvues d'une protéine de transport lipidique appelée MlaA. Dans ces cellules, certains lipides diacylés étaient appauvris tandis que des formes monoacylées augmentaient, suggérant que le cycle et le remodelage normaux des phospholipides entre les membranes étaient déréglés. Notamment, les niveaux de phosphatidylglycérol diminuaient dans les cellules traitées par turnercyclamycines, renforçant l'idée que ce lipide est directement lié à leur puissance. Les auteurs proposent que les turnercyclamycines puissent agir comme des leurres moléculaires qui grippent les voies reliant la synthèse ou le transport des acides gras, du LPS et de la phosphatidylglycérol.
Ce que cela signifie pour concevoir de meilleurs médicaments
En termes clairs, l'étude montre que la colistine tue en déchirant rapidement les deux couches protectrices d'une bactérie à Gram négatif, aidée par une forte liaison au LPS, tandis que les turnercyclamycines agissent davantage comme des saboteurs de la chaîne d'approvisionnement lipidique de la cellule. Elles s'insinuent dans la membrane externe, perturbent progressivement la fabrication et le recyclage de lipides spécifiques, et finissent par provoquer l'effondrement de l'enveloppe cellulaire — sans attaquer violemment la membrane interne. Parce que ce mécanisme plus doux et plus ciblé est lié à une moindre toxicité et à un profil de résistance différent, le comprendre offre une feuille de route pour concevoir des lipopeptides de nouvelle génération. En ajustant des caractéristiques telles que la longueur et la saturation de la queue lipidique, les chimistes pourraient être capables de créer des médicaments qui épargnent les tissus humains, conservent leur activité contre des souches résistantes à la colistine, et gardent une longueur d'avance dans la course aux armements contre les bactéries résistantes aux antibiotiques.
Citation: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
Mots-clés: résistance aux antibiotiques, bactéries à Gram négatif, colistine, antibiotiques lipopeptidiques, lipides membranaires