Clear Sky Science · fr
Base structurelle des conformations dynamiques d’AP-4 et de son association à ARF1
Comment les cellules trient et expédient leurs cargaisons
Chaque cellule est un entrepôt animé, triant et expédiant en permanence des milliers de « colis » protéiques vers leurs destinations. Lorsque ce système de livraison dysfonctionne dans les neurones, les conséquences peuvent être des troubles graves du cerveau et du mouvement. Cette étude révèle comment une machine d’expédition clé, nommée AP-4, change de conformation et s’associe à une protéine régulatrice, ARF1, pour charger des cargos dans de petites vésicules de transport, et pourquoi sa flexibilité est si importante pour la santé neuronale.
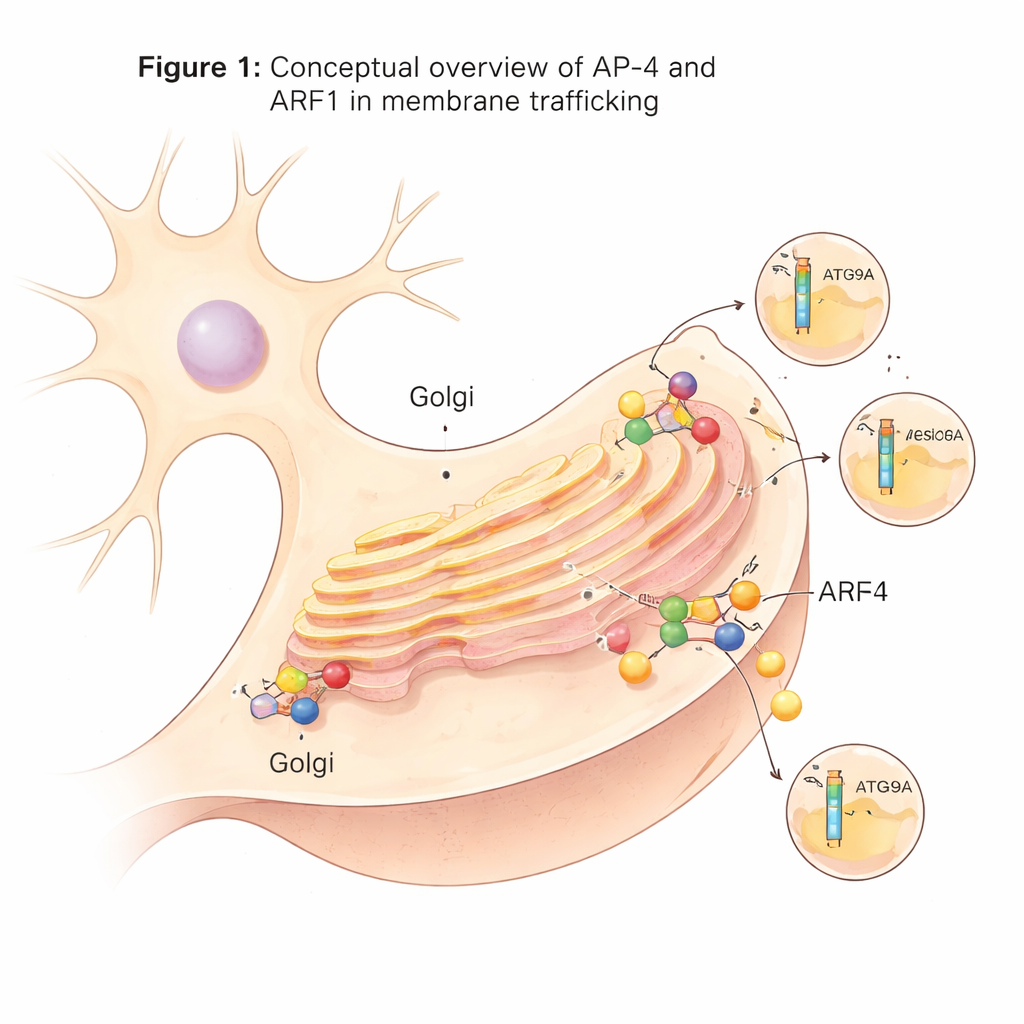
Une machine d’expédition spécialisée dans les neurones
À l’intérieur des cellules, de nombreuses vésicules de transport bourgeonnent d’une plaque de tri centrale connue sous le nom de réseau trans-Golgi. Ces vésicules dépendent de complexes d’adaptateurs protéiques, ou complexes AP, qui jouent un rôle de quais de chargement : ils reconnaissent les protéines cargos et aident à former des vésicules recouvertes autour d’elles. AP-4 est l’un de ces adaptateurs et se distingue parce que, contrairement à beaucoup d’autres, il n’utilise pas la protéine échafaudage courante clathrine. Bien que l’AP-4 soit exprimé dans de nombreux tissus, il joue un rôle particulièrement important dans les neurones. Lorsque l’AP-4 est absent ou défectueux chez l’homme, des cargos cruciaux tels que la protéine liée à l’autophagie ATG9A et certains récepteurs du glutamate ne sont pas correctement transportés, conduisant à une affection neurodéveloppementale sévère connue sous le nom de syndrome de déficience en AP-4.
Un complexe changeant de forme au repos
Les auteurs ont utilisé la cryo‑microscopie électronique, une méthode d’imagerie puissante capable de visualiser de grands assemblages protéiques, pour déterminer la structure tridimensionnelle du « cœur » du complexe AP-4 en solution. AP-4 est constitué de quatre sous‑unités qui forment collectivement une structure en forme de coupe. Ils ont découvert qu’AP-4 n’adopte pas une seule conformation rigide. Au contraire, il bascule naturellement entre une forme « fermée », dans laquelle une sous‑unité (le domaine C‑terminal de la sous‑unité moyenne) est repliée au centre de la coupe, et une forme « ouverte », dans laquelle cette portion se projette vers l’extérieur et devient très flexible. Des expériences complémentaires de fluorescence monocentrique ont montré que cette sous‑unité explore en réalité au moins trois positions — fermée, partiellement ouverte et complètement ouverte — révélant qu’AP-4 est intrinsèquement dynamique même avant sa liaison aux membranes.
Le rôle d’ARF1 : recruteur, pas interrupteur principal
Beaucoup de complexes adaptateurs apparentés sont activés en passant d’une forme inactive à une forme active par la liaison à de petites protéines régulatrices appelées ARF. Pour comprendre ce mécanisme pour AP-4, les chercheurs ont résolu les structures d’AP-4 lié à ARF1, une petite protéine liant le GTP qui s’ancre aux membranes. Ils ont constaté qu’ARF1 s’attache principalement à l’une des grandes sous‑unités d’AP-4 près de son extrémité N‑terminale, de façon similaire à d’autres complexes AP. De manière surprenante, la liaison d’ARF1 ne déclenche pas une réorganisation structurelle spectaculaire d’AP-4. Les formes fermée et ouverte coexistent toujours, et l’architecture globale du complexe reste largement inchangée. Des essais biochimiques ont confirmé que des points de contact spécifiques entre ARF1 et AP-4 sont essentiels pour le recrutement membranaire, mais qu’ARF1 seul n’enferme pas AP-4 dans un unique état actif.
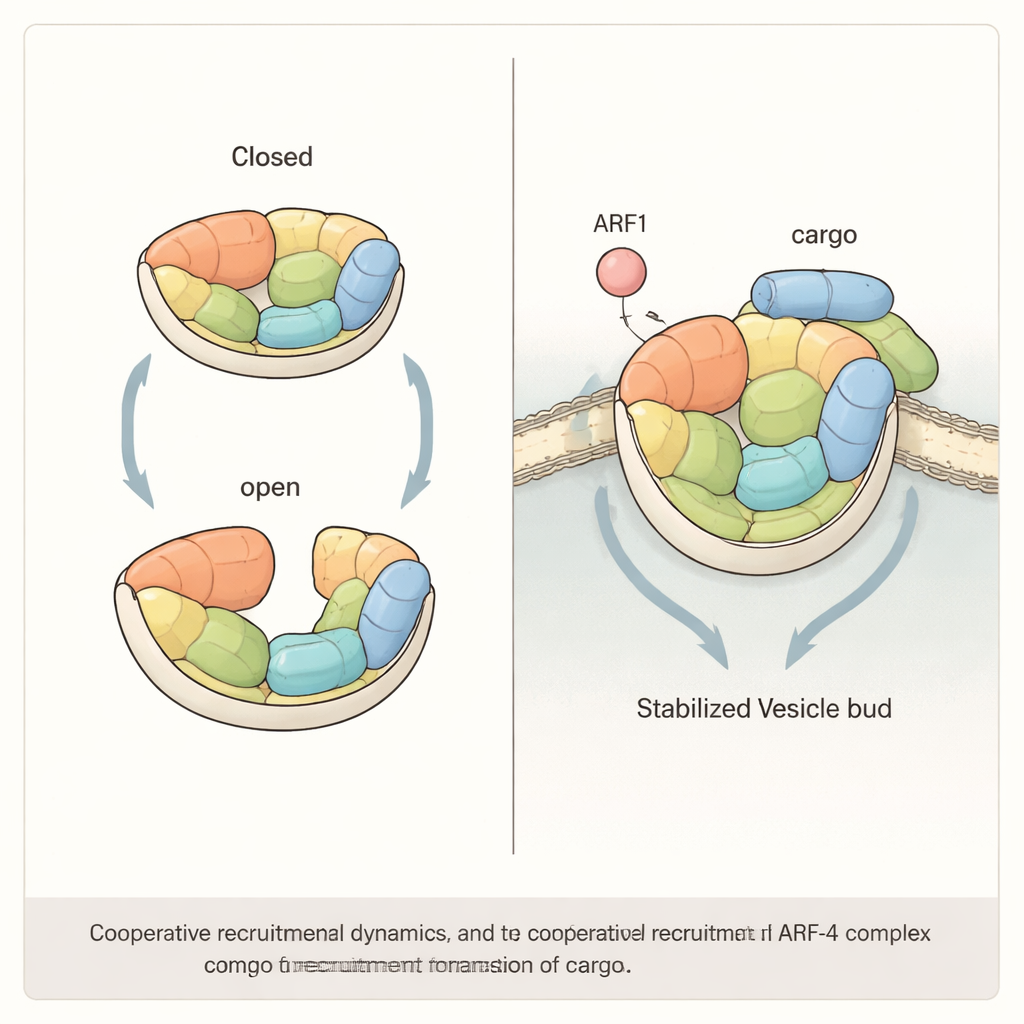
Collaboration entre régulateur et cargo
L’étude montre ensuite que le recrutement efficace d’AP-4 vers les membranes nécessite vraisemblablement une coopération entre ARF1 et les protéines cargos elles‑mêmes. En reconstituant le système sur des billes artificielles et des liposomes, les auteurs ont observé que soit ARF1, soit une courte queue du cargo ATG9A peut attirer AP-4, mais que lorsque les deux sont présents ensemble, ils recrutent beaucoup plus d’AP-4 que la simple addition de leurs effets individuels. Lorsque les chercheurs ont conçu des mutations qui rigidifiaient la structure d’AP-4 — réduisant sa capacité à basculer entre états ouvert et fermé — cet effet synergique disparaissait. Dans des cellules humaines dépourvues d’une sous‑unité clé d’AP-4, le simple rétablissement de versions « rigides » mutantes du complexe n’a pas permis de restaurer le transport normal d’ATG9A depuis le Golgi, soulignant que la flexibilité d’AP-4 n’est pas une curiosité mais une exigence fonctionnelle.
Pourquoi la flexibilité compte pour la santé cérébrale
Dans l’ensemble, ce travail présente AP-4 comme un adaptateur changeant de forme qui explore plusieurs conformations en solution et sur les membranes. Plutôt que d’agir comme un interrupteur marche/arrêt, ARF1 sert de recruteur membranaire qui agit de concert avec les protéines cargos pour stabiliser AP-4 dans des configurations productives pour la formation de vésicules. Perturber cet équilibre — en affaiblissant la liaison à ARF1 ou au cargo, ou en figant AP-4 dans une seule conformation — compromet l’export des cargos depuis le Golgi et peut contribuer à des maladies neurodéveloppementales. En révélant la base structurelle du comportement dynamique d’AP-4, cette étude fournit un cadre pour comprendre les troubles liés à AP-4 et suggère des pistes pour restaurer un trafic correct dans les neurones affectés.
Citation: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Mots-clés: tri membranaire, complexe adaptateur AP-4, ARF1, formation de vésicules, trouble du développement neurologique