Clear Sky Science · fr
Les cellules NK ZNF683+ déterminent la sensibilité à la chimiothérapie dans les CPCSH avancés en remodelant le microenvironnement immunitaire
Pourquoi certains traitements chimiques fonctionnent mieux pour certains cancers de la gorge
Les personnes atteintes d’un carcinome épidermoïde de l’hypopharynx avancé — une tumeur cachée au fond de la gorge — subissent souvent une chimiothérapie lourde aux résultats incertains. Certaines tumeurs régressent fortement, tandis que d’autres bougent à peine. Cette étude pose une question simple mais cruciale : qu’y a‑t‑il de différent à l’intérieur des tumeurs qui répondent bien ? En examinant les cellules immunitaires une par une, les chercheurs mettent au jour un type particulier de « cellule sentinelle » capable de faire pencher la balance entre succès et échec de la chimiothérapie standard.
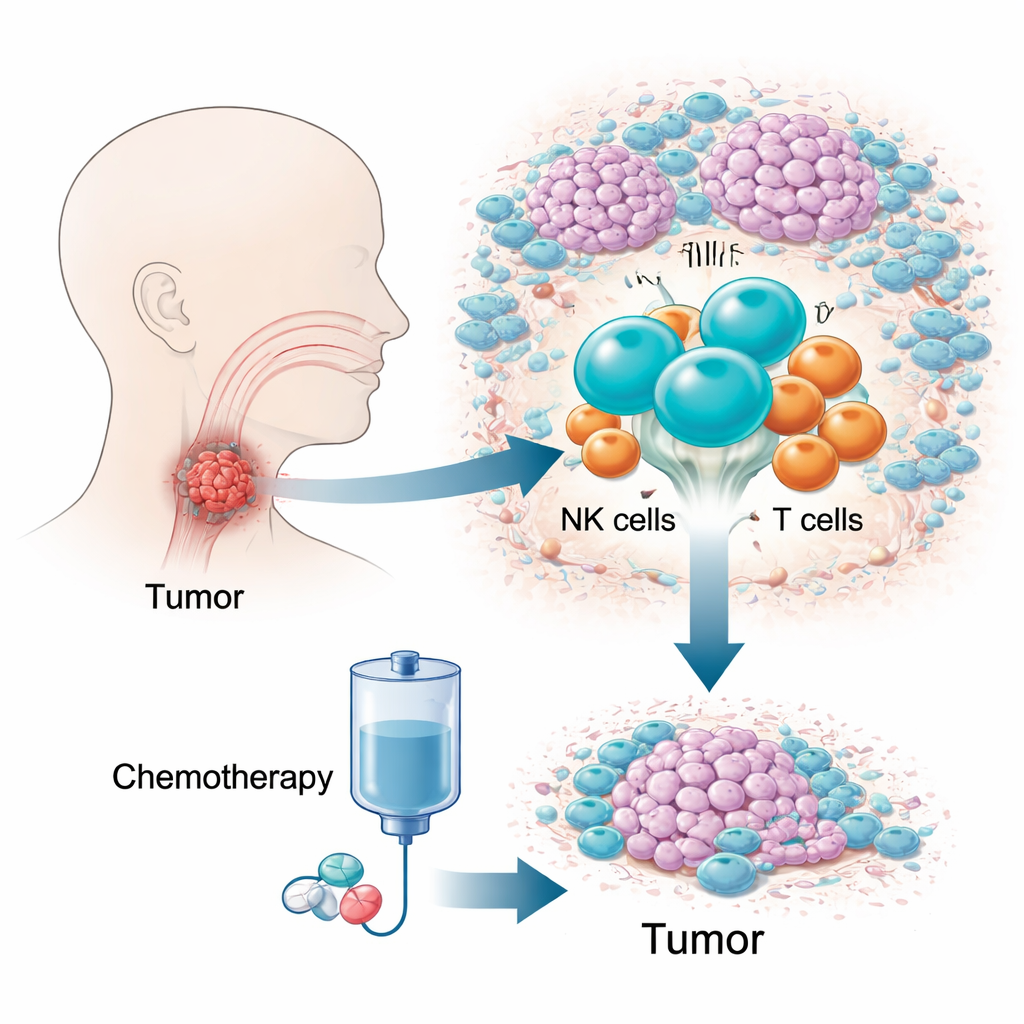
Le défi d’un cancer caché et difficile à traiter
Le carcinome épidermoïde de l’hypopharynx est l’un des cancers de la tête et du cou les plus mortels, en partie parce qu’il se développe dans une région étroite difficile à examiner et cause peu de symptômes au stade précoce. Beaucoup de patients sont diagnostiqués tard, lorsque les options sont limitées et que la survie à cinq ans est faible. Une combinaison médicamenteuse connue sous le nom de chimiothérapie TPF est largement utilisée car elle peut contrôler la maladie tout en préservant la boîte vocale. Pourtant, 10 à 20 % des patients présentent peu ou pas de réponse, perdant un temps précieux. Les tests génétiques classiques, qui moyennent des signaux sur des millions de cellules, ont eu du mal à expliquer cette différence, poussant les auteurs à se concentrer plutôt sur l’écosystème vivant des cellules immunitaires de la tumeur.
Lire le paysage immunitaire tumoral cellule par cellule
Les chercheurs ont suivi 12 patients au fil du temps, prélevant des échantillons tumoraux avant et après deux cycles de chimiothérapie TPF et profilant plus de 150 000 cellules immunitaires à résolution unicellulaire. Ils ont également examiné 41 patients supplémentaires pour confirmer les résultats clés par imagerie et cytométrie en flux. En cartographiant l’activité génique et le type de chaque cellule, ils ont construit un atlas détaillé du microenvironnement tumoral : cellules T, cellules B, macrophages, cellules dendritiques, mastocytes, neutrophiles et cellules NK (natural killer). Parmi tous ces acteurs, un schéma s’est démarqué. Avant le traitement, les tumeurs qui ont ensuite diminué contenaient beaucoup plus de cellules NK que celles qui résistaient à la thérapie, et plus la fraction de cellules NK était élevée, plus la réduction tumorale finale était importante.
Un sous‑ensemble particulier de NK prépare les cellules T au succès
En approfondissant l’analyse, l’équipe a subdivisé les cellules NK en trois groupes selon leurs caractéristiques moléculaires. Un seul de ces groupes, marqué par le facteur de transcription ZNF683 et principalement localisé dans le tissu entourant les nids tumoraux, corrélait fortement avec une bonne réponse à la chimiothérapie. Les patients dont les tumeurs contenaient davantage de ces cellules NK ZNF683+ au départ étaient beaucoup plus susceptibles de bénéficier du TPF. Dans des expériences chez la souris, l’élimination des cellules NK supprimait presque complètement l’effet bénéfique de la chimiothérapie, confirmant que l’activité des NK n’est pas seulement un marqueur mais une condition nécessaire à l’efficacité du traitement. Fait intéressant, ces cellules NK n’agissaient pas simplement comme des tueuses directes du cancer ; leurs programmes géniques étaient enrichis en fonctions d’orientation et d’activation des cellules T.
Comment les NK autorisent des cellules T hautement cytotoxiques
Pour comprendre quelles cellules T importaient le plus, les scientifiques ont suivi des clones de récepteurs de cellules T avant et après traitement. Ils ont découvert que, chez les répondants, un groupe spécifique de cellules T CD8 « mémoire effectrices », enrichi pour la molécule GZMK, s’est fortement développé après la chimiothérapie. Ces cellules T produisaient de fortes quantités des cytokines toxiques TNF et interféron‑gamma sans présenter de signes marqués d’épuisement, en faisant des tueuses puissantes et durables. L’imagerie spatiale a révélé qu’après le traitement, ces cellules T CD8 GZMK+ se regroupaient fortement dans les tumeurs des patients répondants mais pas chez les non‑répondants. Dans des tests de co‑culture in vitro avec des cellules humaines, le contact direct avec les NK ZNF683+ a stimulé l’expansion de ce sous‑ensemble de CD8 GZMK+, un effet qui disparaissait lorsque les cellules étaient séparées par une barrière.
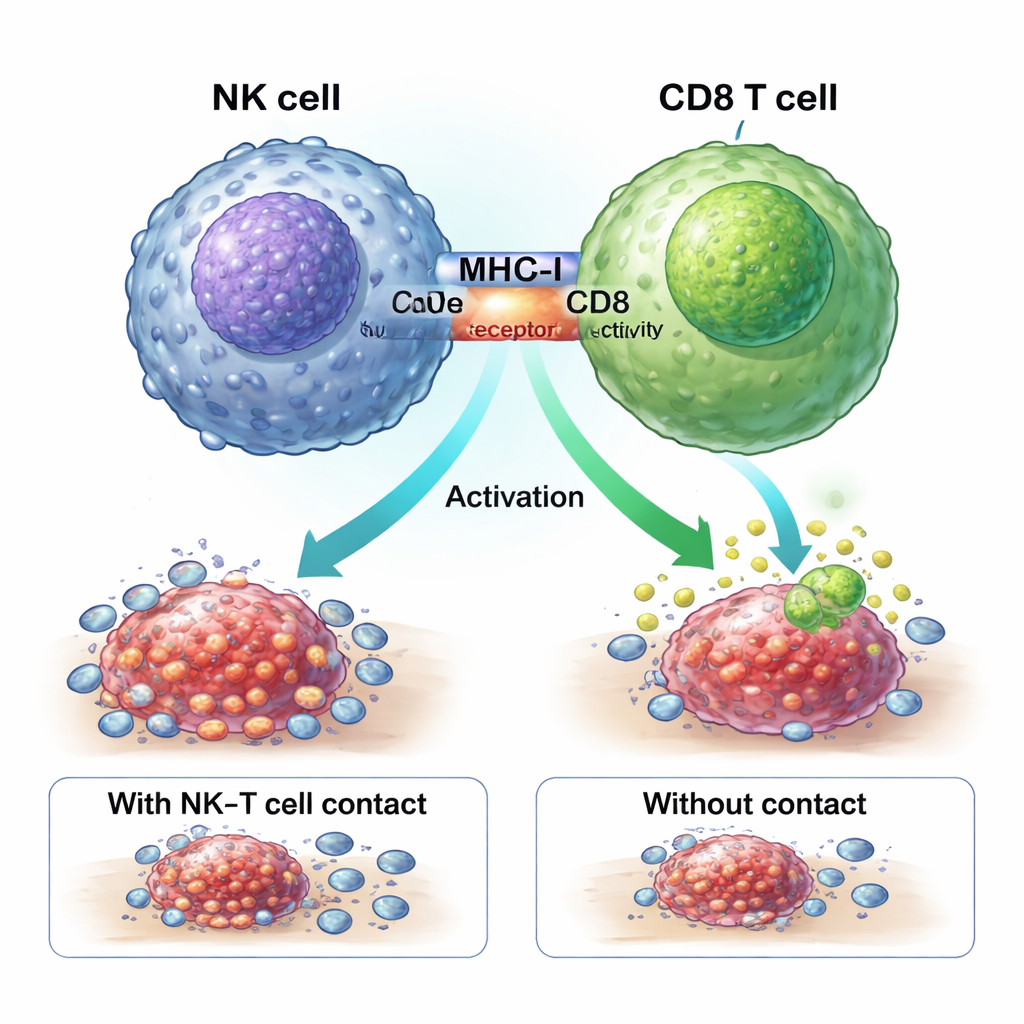
Une poignée de main physique qui active les combattants anti‑tumeur
L’étude montre que les NK ZNF683+ améliorent la réponse à la chimiothérapie via une « poignée de main » physique avec les cellules T CD8. Des molécules appelées CMH‑I (MHC‑I) à la surface des NK s’engagent avec les récepteurs CD8 des cellules T dans une zone de contact étroit, ou synapse immunitaire. Le blocage du CMH‑I empêchait les NK de générer les cellules T CD8 GZMK+ puissantes. Chez des souris génétiquement modifiées dépourvues de ZNF683 uniquement dans les NK, ces NK exprimaient moins de CMH‑I et étaient beaucoup moins efficaces pour activer les CD8, renforçant l’idée que ZNF683 programme les NK pour devenir des coachs efficaces des cellules T plutôt que de simples exécutrices.
Ce que cela signifie pour les patients
Pour un public non spécialiste, le message principal est que toutes les cellules immunitaires d’une tumeur ne se valent pas. Ce travail identifie un sous‑ensemble particulier de NK comme éclaireur avancé qui prépare le champ de bataille avant même le début de la chimiothérapie. Les tumeurs riches en ces cellules sont prêtes à libérer des vagues de cellules T CD8 puissantes une fois les médicaments administrés, entraînant une réduction tumorale nettement meilleure. Mesurer l’abondance de cet axe NK–T avant le traitement pourrait aider les médecins à prédire qui bénéficiera du TPF et qui pourrait nécessiter des thérapies alternatives ou complémentaires. À l’avenir, des traitements qui augmentent ou imitent ces NK ZNF683+ pourraient transformer des cancers de l’hypopharynx résistants en cancers beaucoup plus sensibles à la chimiothérapie standard.
Citation: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
Mots-clés: cancer de l’hypopharynx, résistance à la chimiothérapie, cellules tueuses naturelles, microenvironnement immunitaire tumoral, cellules T CD8