Clear Sky Science · fr
Construction sélective de liaisons N–N induite par la lumière via la libération et le transfert de nitrène
Éclairer une nouvelle façon d’unir des atomes d’azote
Les atomes d’azote sont au cœur de nombreux médicaments, agents de protection des cultures et matériaux avancés. Les chimistes savent très bien lier l’azote au carbone, mais connecter directement deux atomes d’azote est beaucoup plus difficile. Cette étude présente une méthode sans métal, alimentée par la lumière, pour assembler des atomes d’azote de façon contrôlée, ouvrant une voie plus simple vers une large gamme de molécules utiles.
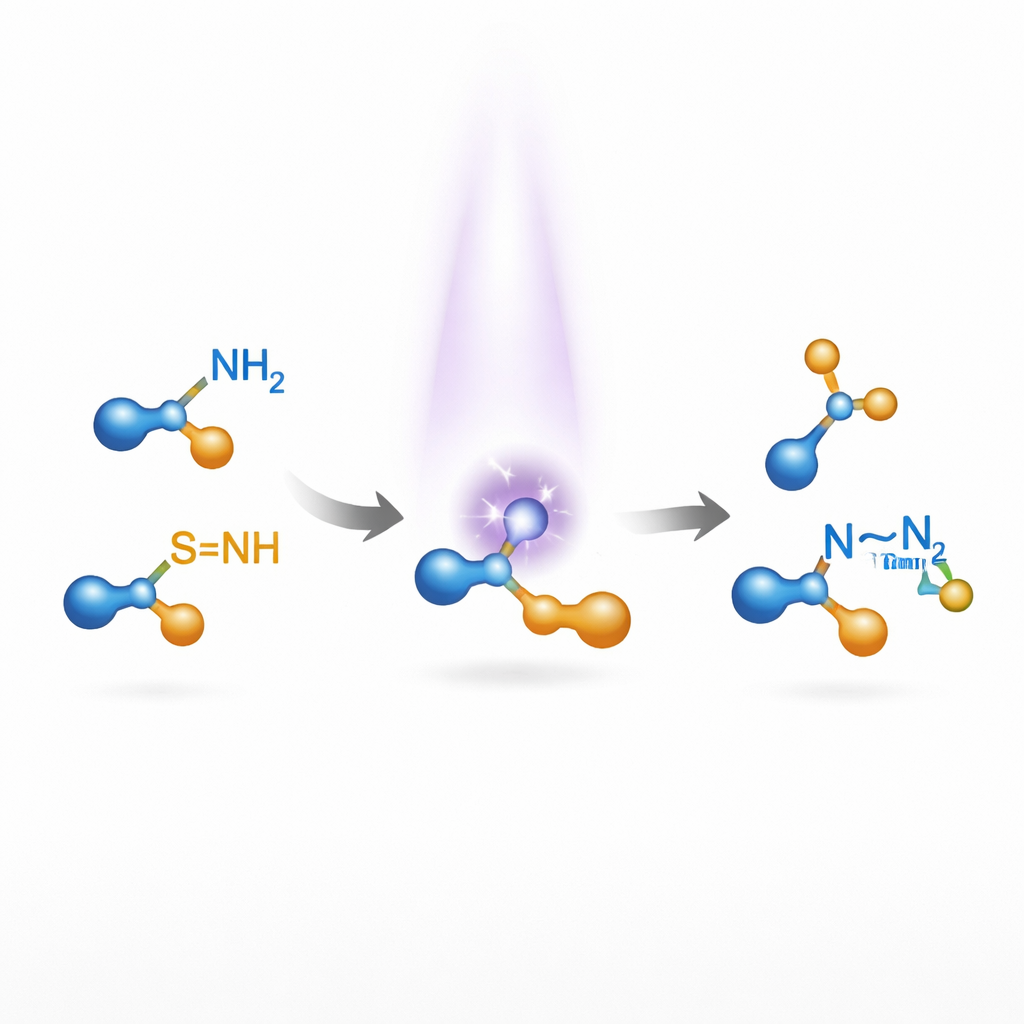
Pourquoi relier l’azote à l’azote est difficile
De nombreux produits naturels et médicaments contiennent des paires d’atomes d’azote liés entre eux, une disposition qui peut moduler le comportement d’une molécule dans l’organisme ou dans les matériaux. Les méthodes existantes pour construire ces unités N–N partent généralement de fragments azote–azote préformés, tels que les hydrazines ou les composés diazo, puis les modifient étape par étape. Forger directement la liaison N–N à partir d’amines simples est séduisant mais complexe : l’azote est assez électronégatif, de sorte que deux atomes d’azote ne forment pas naturellement une liaison non polaire stable. Les succès passés ont beaucoup reposé sur des catalyseurs à base de métaux de transition et fonctionnent souvent seulement pour des familles de molécules restreintes, limitant leur utilité en chimie de découverte.
Utiliser la lumière pour maîtriser un intermédiaire réactif
Les auteurs se sont tournés vers les nitrènes — des espèces d’azote hautement réactives et de vie brève qui peuvent, en principe, s’insérer dans d’autres liaisons. La chimie traditionnelle des nitrènes nécessite typiquement des catalyseurs métalliques et peut souffrir de réactions secondaires car les nitrènes sont très énergétiques. L’équipe s’est demandé si elle pouvait générer des nitrènes par la lumière de manière plus douce et plus contrôlée, sans métaux, puis les utiliser pour relier des amines simples en produits contenant N–N. Leur idée clé a été d’utiliser des sulfilimines, une famille de molécules faciles à modifier et qui absorbent dans l’ultraviolet et le proche visible. Lorsqu’elles sont illuminées, ces sulfilimines peuvent se scinder en libérant un fragment nitrène tout en produisant un sous-produit soufré inoffensif.
Une recette large et sans métal pour obtenir des paires d’azote
Après des tests systématiques, les chercheurs ont identifié une sulfilimine particulière qui, sous lumière de 365 nanomètres en chloroforme, réagit efficacement avec de nombreuses amines pour donner des hydrazides — des molécules présentant une liaison N–N nouvellement formée adjacente à un groupe carbonyle. Ils ont optimisé des paramètres tels que la structure de la sulfilimine, le solvant et l’intensité lumineuse pour favoriser le produit désiré plutôt que des sous-produits courants comme les urées. Dans ces conditions douces, une grande variété d’amines, y compris aromatiques, aliphatique et des variantes cycliques, se sont couplées avec succès. Ils ont aussi montré que de nombreuses sulfilimines différentes, portant des groupes acyles aromatiques ou aliphatiques et des groupes sulfonyl, participent bien, donnant des dizaines de produits distincts contenant N–N. Fait important, la méthode peut être appliquée en fin de synthèse pour modifier des molécules complexes et biologiquement actives, telles que des anti-inflammatoires courants et des blocs de construction chiraux, démontrant sa praticité pour la chimie médicinale et des matériaux.
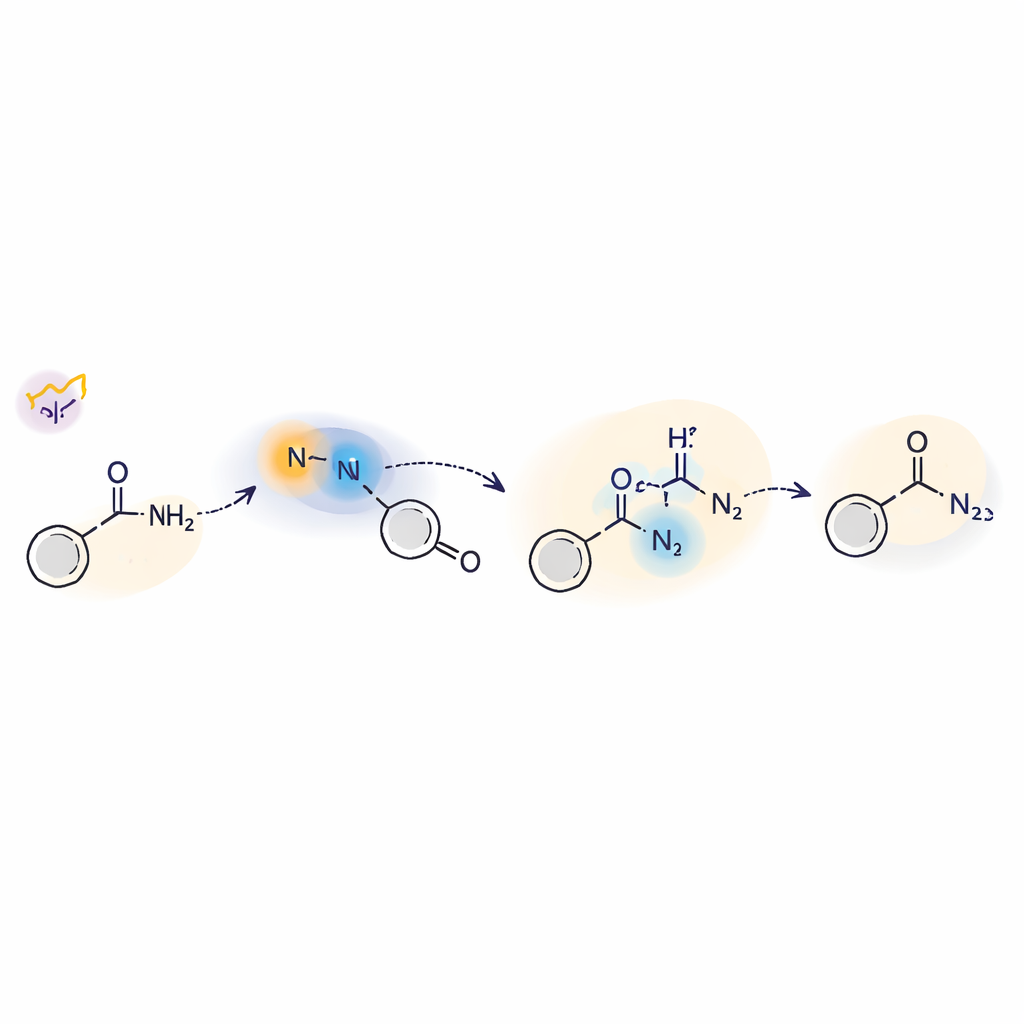
Regarder sous le capot de l’étape Photo‑induite
Pour comprendre comment fonctionne cette chimie déclenchée par la lumière, l’équipe a combiné expériences et théorie. Ils ont utilisé des pièges à radicaux, le marquage isotopique et la résonance paramagnétique électronique pour montrer que des intermédiaires nitrènes libres et des radicaux centrés sur l’azote apparaissent pendant la réaction. La spectroscopie laser résolue dans le temps a révélé deux formes clés du nitrène : un état triplet de courte durée de vie et un état singulet de vie plus longue. La forme singulet réagit directement avec les amines par une sorte d’attaque nucléophile, tandis que le triplet peut participer à des étapes de transfert d’atomes d’hydrogène. Des calculs informatiques soutiennent un mécanisme où la lumière excite la sulfilimine, la liaison soufre–azote se rompt, et le nitrène résultant engage ensuite l’amine via des voies singulet et triplet avant de se stabiliser dans la structure finale de l’hydrazide.
Ce que cela signifie pour les molécules de demain
Ce travail montre que des sulfilimines soigneusement conçues peuvent agir comme des « réservoirs de nitrène » qui libèrent des unités d’azote réactives à la demande sous lumière, sans l’aide de métaux. En exploitant à la fois les personnalités singulet et triplet des nitrènes tout en maintenant leur concentration basse, la méthode permet une formation sélective de liaisons N–N sur une large gamme de blocs de construction. Pour le non-spécialiste, l’essentiel est que les chimistes disposent désormais d’un moyen plus simple, plus propre et plus souple pour assembler des atomes d’azote, ce qui pourrait accélérer la création de nouveaux médicaments, agrochimiques et matériaux riches en azote.
Citation: Yu, M., Feng, J., Wang, X. et al. Photo-induced selective N-N bond construction via harnessing nitrene release and transfer. Nat Commun 17, 2084 (2026). https://doi.org/10.1038/s41467-026-68674-z
Mots-clés: chimie des nitrènes, réactions photo-induites, formation de liaisons N–N, sulfilimines, hydrazides