Clear Sky Science · fr
Exploiter le PV‑oxirène pour la synthèse modulaire des α‑oxy carbonylés
Pourquoi de petits liaisons chimiques comptent
Beaucoup de médicaments modernes, de produits phytosanitaires et de matériaux avancés s’appuient sur de petits « connecteurs » moléculaires qui maintiennent des éléments plus grands ensemble et modulents subtilement leur comportement. Une famille de ces connecteurs, les carbonylés α‑oxy, peut modifier la stabilité d’un médicament, la conformation d’un peptide ou les propriétés d’un plastique. Pourtant, ces liaisons prometteuses ont été étonnamment difficiles à préparer de façon flexible et combinatoire. Cet article décrit une nouvelle méthode douce permettant aux chimistes de construire rapidement de nombreux carbonylés α‑oxy à partir de matériaux de départ simples, ouvrant de nouvelles possibilités en conception de médicaments, biologie chimique et science des matériaux.
Construire une meilleure boîte à outils chimique
Les carbonylés α‑oxy se rencontrent à la fois dans la nature et dans la technologie — des agents anticancéreux et antibiotiques aux polymères biodégradables et aux herbicides. Un groupe étroitement lié, les acides α‑hydroxy, peut même être inséré dans des chaînes de type protéique pour ajuster la façon dont ces chaînes se replient et interagissent, ce qui influence leur reconnaissance des cibles biologiques. Les méthodes existantes pour accéder à ces liaisons reposent sur des séquences en plusieurs étapes, des réactifs agressifs ou des jeux de blocs de construction restreints. Ces limites compliquent l’exploration rapide de nouvelles structures ou la modification de molécules médicamenteuses complexes en fin de synthèse.
Une nouvelle chaîne d’assemblage en trois pièces
Les chercheurs présentent une réaction à base de cuivre qui assemble en une seule opération trois ingrédients simples : un réactif « ylide » spécialement conçu, un acide carboxylique ordinaire (un groupe présent dans d’innombrables produits naturels et médicaments) et un troisième partenaire apportant de l’azote, de l’oxygène, du soufre, du sélénium ou de l’eau. Dans des conditions douces et sans métaux précieux, ces trois éléments se combinent pour donner des produits carbonylés α‑oxy tels que des esters, des amides, des thioesters et des structures apparentées. La réaction tolère de nombreux autres groupes sensibles — doubles liaisons, nitriles, sulfures et systèmes cycliques complexes — montrant qu’elle peut s’appliquer directement à des molécules complexes de type médicament.
Exploiter un cycle fugitif pour contrôler la réaction
Cette nouvelle méthode repose sur un cycle inhabituel et fortement tendu appelé oxirène, longtemps considéré comme une curiosité éphémère plutôt qu’un outil pratique. En incorporant dans le cycle un groupe contenant du phosphore et en le générant brièvement avec l’aide du cuivre, l’équipe transforme cette structure réactive en une étape de transition contrôlable. L’acide carboxylique devient d’abord un partenaire chargé qui attaque l’oxirène à une position préférentielle, orientant la réaction de sorte qu’un produit principal unique se forme au lieu d’un mélange confus. L’intermédiaire obtenu transmet ensuite son fragment acyle au troisième nucléophile, livrant le carbonylé α‑oxy final dans une étape qui ressemble à une course de relais soigneusement chorégraphiée.
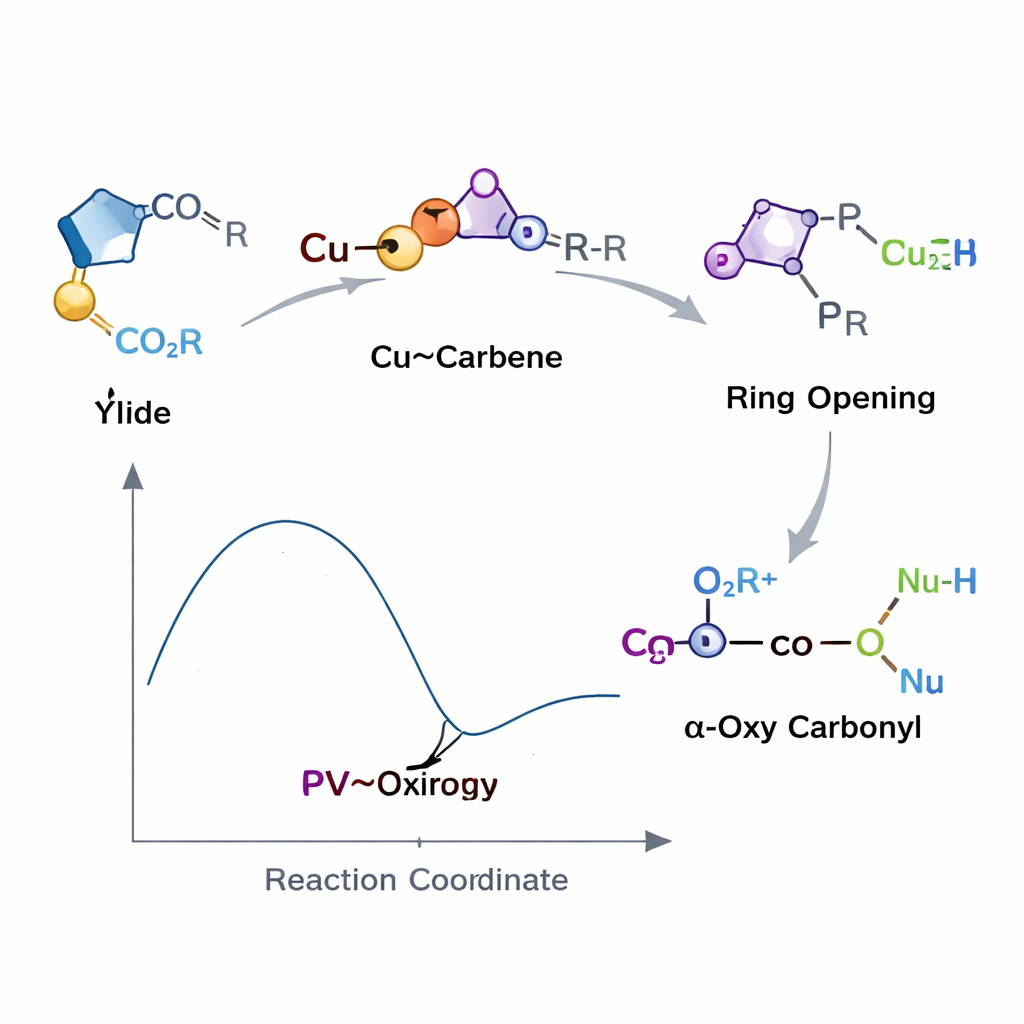
Des peptides aux herbicides et au‑delà
Pour illustrer le potentiel de cette chimie, les auteurs construisent de courtes chaînes de type peptide dans lesquelles des liaisons normales sont remplacées par des liaisons ester dérivées d’acides α‑hydroxy. Ces « dépseptides » sont des sondes précieuses pour comprendre comment de petits changements dans la structure de l’épine dorsale affectent la fonction biologique, mais ils sont généralement difficiles d’accès. La même stratégie permet aussi de produire en une seule étape un herbicide commercial, le lactofène, à partir d’un précurseur connu, et de générer rapidement de nouveaux analogues qui seraient lourds à obtenir par des voies plus anciennes. De plus, en combinant la nouvelle réaction avec quelques étapes simples, l’équipe montre comment allonger des acides carboxyliques d’un carbone tout en introduisant un groupe α‑hydroxy, une transformation prisée en chimie médicinale.
Ce que cela implique pour l’avenir
Concrètement, ce travail offre aux chimistes un outil polyvalent et facile d’utilisation pour installer des liaisons carbonylées α‑oxy presque partout où un acide carboxylique et un nucléophile sont présents, même dans des molécules bioactives complexes. À un niveau plus profond, il démontre qu’un intermédiaire autrefois ésotérique, l’oxirène, peut être apprivoisé et mis au service de la synthèse quotidienne. En transformant un cycle fugitif en une étape contrôlable d’une chaîne d’assemblage, la méthode élargit le catalogue des connecteurs moléculaires disponibles pour concevoir des médicaments, sonder des systèmes biologiques et développer de nouveaux matériaux.
Citation: Huang, S., Duan, D., Luo, J. et al. Harnessing PV-oxirene for the modular synthesis of α-Oxy carbonyls. Nat Commun 17, 1918 (2026). https://doi.org/10.1038/s41467-026-68671-2
Mots-clés: carbonylés α‑oxy, synthèse modulaire, catalyse au cuivre, dépseptides, fonctionnalisation d’acides carboxyliques