Clear Sky Science · fr
Photosynthèse de glycine via couplage C−N du plastique de déchets et du nitrate sur catalyseur diatomique Pd−B
Transformer les déchets en éléments constitutifs de la vie
Les bouteilles en plastique, les contenants alimentaires et les vêtements en polyester sont omniprésents—et leurs déchets aussi. Parallèlement, de nombreuses usines rejettent des eaux usées chargées en nitrates qui peuvent polluer rivières et mers. Cette étude montre comment s’attaquer simultanément à ces deux problèmes : en utilisant la lumière du soleil et un catalyseur spécialement conçu pour transformer le plastique jeté et les nitrates en glycine, un acide aminé simple largement utilisé dans l’alimentation, la médecine et l’agriculture.
Pourquoi la glycine et les déchets comptent
La glycine est l’un des éléments de base des protéines et est produite à l’échelle de centaines de milliers de tonnes par an. Les méthodes industrielles conventionnelles, en particulier le procédé de Strecker classique, reposent sur des composés cyanurés toxiques et des conditions de réaction sévères, posant des problèmes de sécurité et d’environnement. Par ailleurs, la production mondiale de PET—utilisé pour les bouteilles, les textiles et les emballages—dépassent 100 millions de tonnes par an, et plus de 80 % finit en décharge ou dans l’environnement. Lorsque le PET est décomposé chimiquement, l’un des produits est l’éthylène glycol, un liquide de faible valeur qui coûte cher à purifier. Les auteurs posent une question simple : au lieu de considérer l’éthylène glycol et le nitrate comme des déchets, pourraient-ils devenir des matières premières pour produire de la glycine en utilisant uniquement la lumière du soleil ?
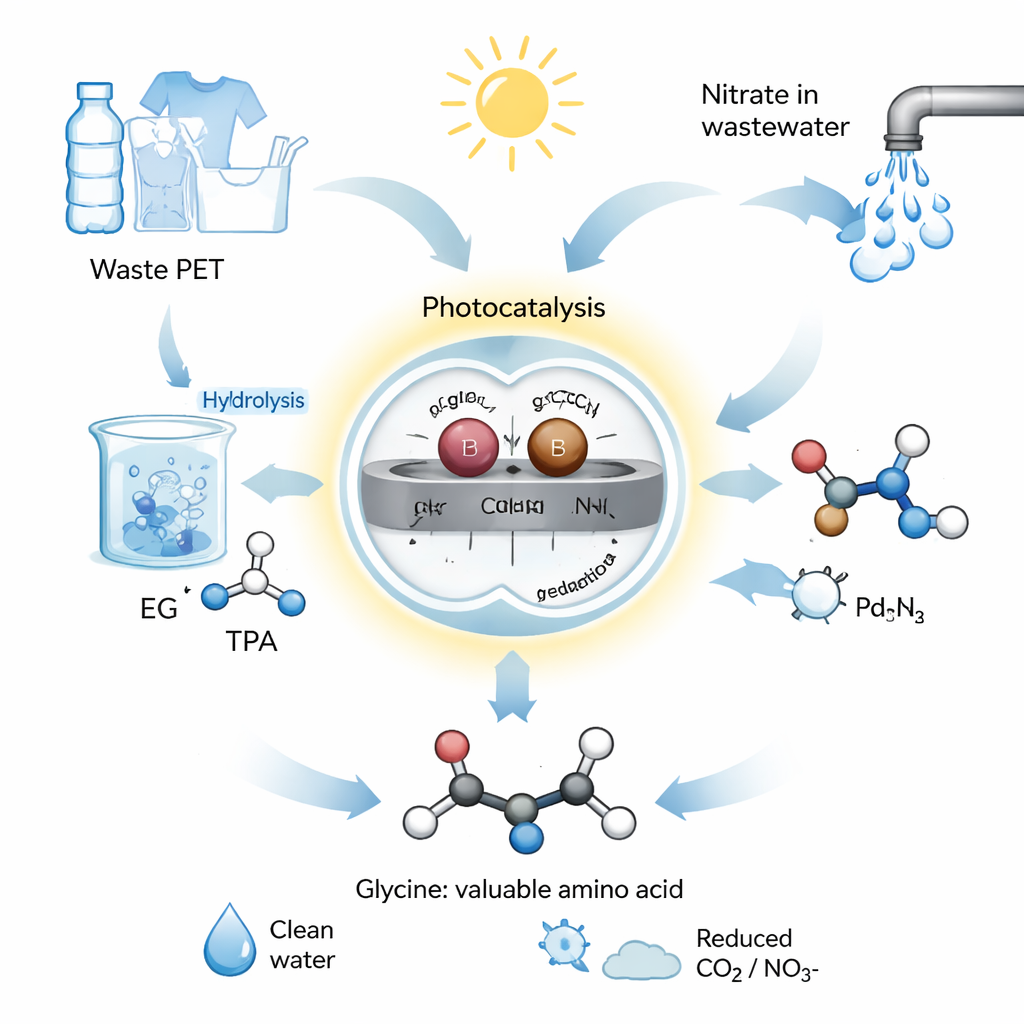
Un raccourci chimique propulsé par le soleil
L’équipe a conçu un système photocatalytique, c’est‑à‑dire qui utilise la lumière pour piloter des réactions chimiques. Ils ont fabriqué un catalyseur à partir de nitrure de carbone graphitique, un semi‑conducteur, et ont ancré des paires d’atomes individuels de palladium (Pd) et de bore (B) à sa surface. Ces atomes appariés agissent comme une équipe microscopique à deux membres, chacun gérant une moitié différente de la chimie. Dans leur procédé, les déchets de PET sont d’abord hydrolysés—dissociés dans une eau alcaline—pour libérer l’éthylène glycol. Cet éthylène glycol et les nitrates issus des eaux usées sont ensuite placés dans l’eau avec le catalyseur Pd–B et exposés à la lumière simulée ou naturelle. Dans ces conditions douces, le système convertit le mélange en glycine avec un rendement élevé et une sélectivité supérieure à 92 %, ce qui signifie que très peu de sous‑produits indésirables se forment.
Comment fonctionne le duo atomique
Le succès du catalyseur dépend de la manière dont il gère des intermédiaires réactionnels de courte durée de vie. Les sites en bore à la surface sont « riches en trous », ce qui signifie qu’ils acceptent facilement une charge positive lorsque le matériau absorbe la lumière. Sur ces sites B, l’éthylène glycol est doucement oxydé—privé d’hydrogène—pour former du glycolaldéhyde, une molécule instable qui a tendance normalement à s’oxyder excessivement en acides voire en dioxyde de carbone. Les sites en palladium, en revanche, sont « riches en électrons ». Ils utilisent les électrons générés par la lumière pour réduire les nitrates par étapes en ammonium ou en ammoniaque. L’étape clé est un couplage carbone–azote entre le glycolaldéhyde et ces espèces azotées pour former de l’éthanolamine, qui est ensuite oxydée davantage, principalement aux sites B, pour donner la glycine. En stabilisant le glycolaldéhyde juste assez longtemps pour réagir, et en maintenant une séparation spatiale des électrons et des trous, la paire Pd–B oriente la chimie loin des réactions secondaires gaspilleuses et vers l’acide aminé désiré.
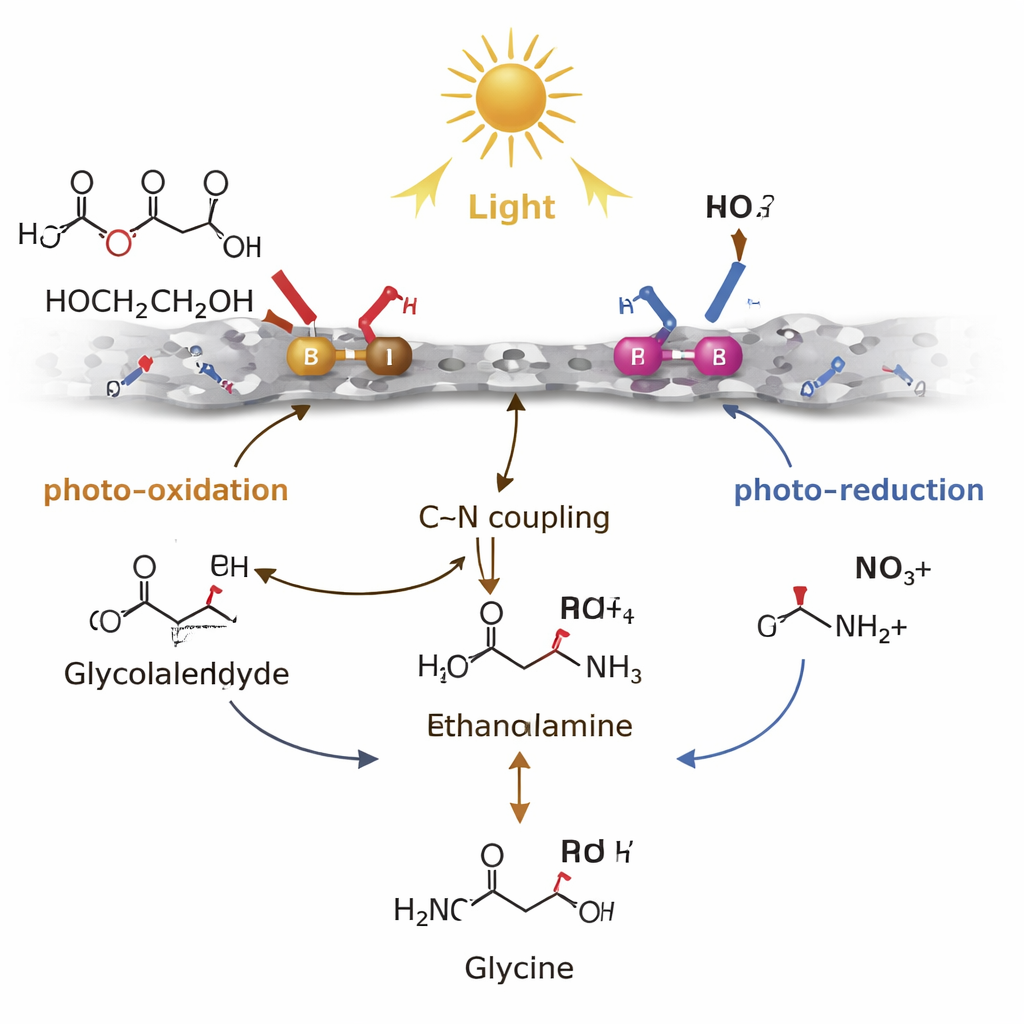
Du mécanisme en laboratoire aux déchets réels
Les chercheurs ont confirmé chaque partie de cette voie par une batterie de techniques, suivant en temps réel les radicaux, les intermédiaires et les produits azotés. Ils ont comparé différents matériaux catalytiques et métaux et ont constaté que des supports g‑C3N4 avec des paires Pd–B isolées offraient les meilleures performances, atteignant des vitesses de production de glycine de 2,9 millimoles par gramme de catalyseur et par heure. Le catalyseur est resté actif sur plusieurs cycles et sa structure est demeurée stable. Fait important, l’équipe est allée au‑delà des produits chimiques de laboratoire purs. Ils ont démontré une production de glycine à l’échelle du gramme à partir de PET post‑consommation réel—poudre, bouteilles, vêtements, sacs et plus—combiné à des solutions de nitrate et même à des eaux usées complexes. Ils ont aussi montré que des alcools apparentés issus de la biomasse, comme la glycérine, peuvent servir de sources de carbone alternatives, élargissant la pertinence de l’approche.
Une voie gagnant‑gagnant pour les déchets et le climat
Pour rapprocher le concept d’une application pratique, les auteurs ont testé leur procédé sous la lumière naturelle du soleil concentrée par une simple lentille de Fresnel. Le système a produit de la glycine de façon constante avec une grande sélectivité, et la modélisation suggère que sa mise à l’échelle pourrait éviter des émissions substantielles de dioxyde de carbone et empêcher le rejet de nitrates dans l’environnement. En termes clairs, ce travail décrit une manière de convertir des piles de plastique usagé et de l’eau polluée en un acide aminé utile, en n’utilisant que la lumière et un catalyseur finement conçu. Bien que des défis d’ingénierie subsistent avant un déploiement industriel, l’étude illustre comment la conception de catalyseurs au niveau atomique peut transformer deux flux de déchets majeurs en un produit chimique unique et précieux.
Citation: Ya, Z., Li, M., Fu, D. et al. Glycine photosynthesis via C−N coupling of waste plastic and nitrate over diatomic Pd−B catalyst. Nat Commun 17, 1887 (2026). https://doi.org/10.1038/s41467-026-68666-z
Mots-clés: glycine, recyclage du plastique, photocatalyse, eaux usées nitrates, catalyseurs monoatomiques