Clear Sky Science · fr
Régulation de l’assemblage de l’adaptateur AP1 par la chaperonne à deux mains MEA1
Pourquoi cet aide-cellule caché est important
À l’intérieur de chaque cellule humaine, des milliers de petits colis transportent des protéines vers leur destination ou vers le « centre de recyclage » cellulaire pour être dégradées. Ce trafic maintient nos cellules en bonne santé et régule nos défenses immunitaires. L’article résumé ici met au jour une protéine jusqu’alors mystérieuse, nommée MEA1, qui s’avère essentielle à la construction de l’un des principaux engins de tri chargés de charger ces colis. Comprendre le fonctionnement de MEA1 aide à expliquer comment les cellules contrôlent des cargaisons importantes, y compris des molécules qui activent ou désactivent les réponses antivirales.
Contrôle du trafic au centre d’expédition de la cellule
Une grande partie de l’activité d’expédition de la cellule passe par une structure appelée Golgi, un empilement de sacs aplatis qui fonctionne comme un bureau de poste central. Depuis le Golgi, les cargaisons peuvent être envoyées vers la surface cellulaire ou redirigées vers des compartiments internes pour dégradation. Un complexe protéique connu sous le nom d’AP1 se trouve au cœur de cette voie. AP1 reconnaît des étiquettes sur les protéines cargo, aide à courber la membrane et recrute une coque externe de clathrine pour former de petites vésicules de transport. Sans un AP1 correctement assemblé, des cargaisons cruciales s’accumulent au mauvais endroit et des voies de signalisation normales, y compris celles liées à l’immunité, peuvent être perturbées. 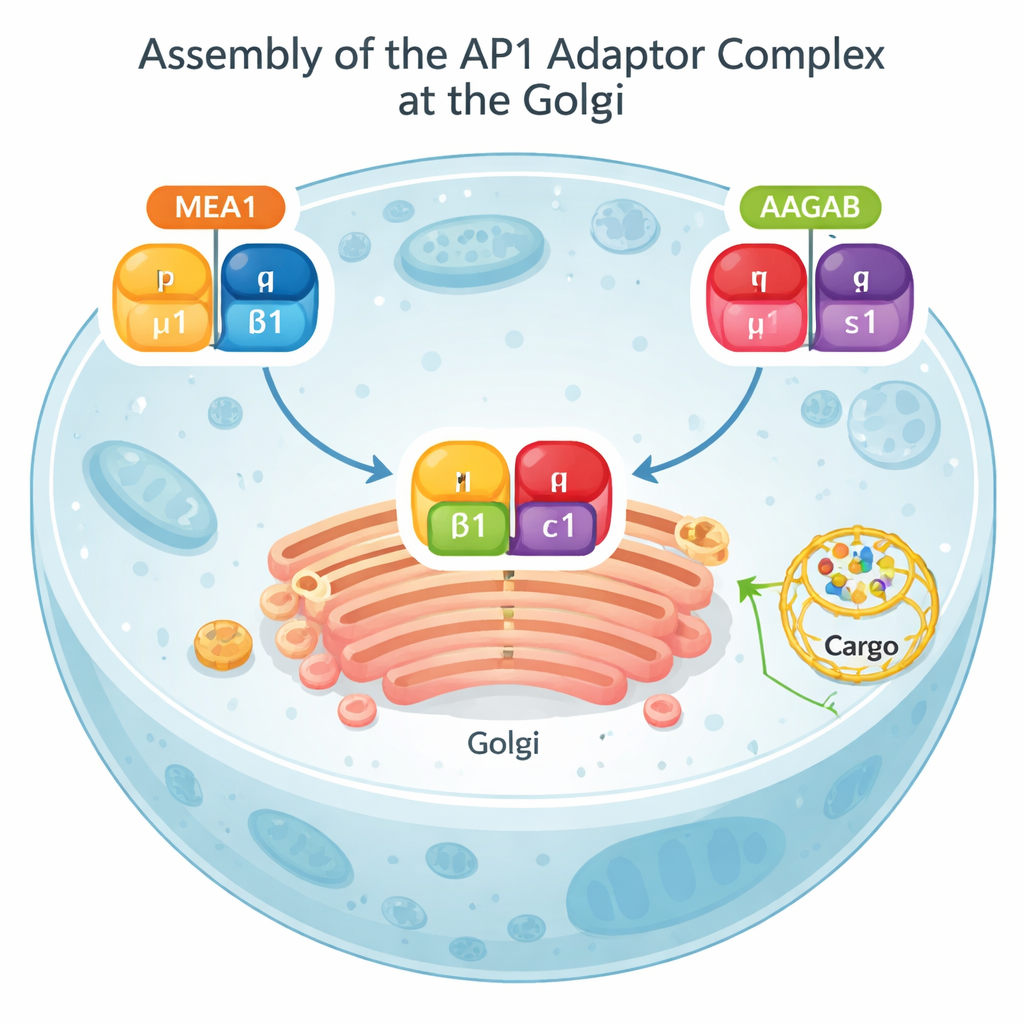
Trouver un ouvrier d’assemblage manquant
Les auteurs ont cherché à identifier des protéines qui s’associent physiquement à AP1 et pourraient aider à son assemblage. Ils ont exploité une grande base de données d’interactions protéiques, écarté les candidats peu susceptibles de fonctionner avec AP1, puis utilisé un outil d’intelligence artificielle, AlphaFold, pour prédire comment les protéines restantes pourraient entrer en contact avec les différentes parties d’AP1. Cette recherche a mis en évidence MEA1, une petite protéine jusqu’alors non caractérisée présente dans de nombreux tissus. Des expériences de suivi dans des cellules humaines ont confirmé que MEA1 se lie à deux sous-unités spécifiques d’AP1, connues sous les noms μ1 et β1, à la fois lorsqu’elles sont testées isolément et dans leurs formes naturelles non modifiées.
MEA1 maintient AP1 intact et le trafic des cargaisons en marche
Pour déterminer ce que fait réellement MEA1, les chercheurs ont supprimé le gène MEA1 dans des lignées cellulaires humaines. En l’absence de MEA1, les quatre composants d’AP1 étaient fortement réduits et les points caractéristiques d’AP1 près du Golgi avaient presque disparu. Cette perte a eu des conséquences fonctionnelles évidentes. Une cargaison d’AP1, le récepteur du folate FOLR1, s’est accumulée à la surface cellulaire au lieu d’être envoyée vers l’intérieur, signalant un tri AP1 défectueux. Une autre cargaison, la protéine de signalisation immunitaire STING, n’était plus efficacement empaquetée dans des vésicules à destination des lysosomes, les centres de recyclage cellulaires. En conséquence, STING activé et sa kinase partenaire TBK1 sont restés élevés, indiquant que l’interrupteur d’arrêt de cette voie antivirale ne fonctionnait pas correctement. La réintroduction de MEA1 a restauré les niveaux d’AP1 et corrigé ces défauts de trafic.
Une chaperonne à deux mains et un processus d’assemblage par collision
Des tests biochimiques et des modèles AlphaFold ont montré que MEA1 se comporte comme une chaperonne d’assemblage « à deux mains » : sa partie avant saisit la sous-unité μ1, tandis que sa partie arrière saisit β1. Isolées, μ1 et β1 sont instables et ont tendance à s’agréger ou à être détruites ; liées à MEA1, elles deviennent solubles et prêtes à s’assembler. Une autre chaperonne connue, AAGAB, accomplit un rôle parallèle pour les deux autres sous-unités d’AP1, γ et σ1. Lorsque les complexes MEA1–μ1–β1 et AAGAB–γ–σ1 se rencontrent, leurs sous-unités se combinent pour former un adaptateur AP1 complet à quatre parties. À ce stade, les deux chaperonnes se détachent et retournent au fluide cellulaire, tandis que l’AP1 nouvellement formé se dirige vers les membranes pour effectuer son travail de tri. Ce mécanisme de « collision entre deux chaperonnes » montre que l’assemblage d’AP1 est finement orchestré plutôt que laissé au hasard.
Enseignements plus larges sur le contrôle qualité cellulaire
Au-delà d’AP1, l’étude suggère une stratégie plus générale que les cellules pourraient utiliser pour construire de nombreuses grandes machines protéiques. MEA1 peut également aider faiblement un autre complexe adaptateur appelé AP2, et, conjointement avec AAGAB et une troisième chaperonne nommée CCDC32, illustre une voie plus large que les auteurs appellent « Assemblage d’Adapteurs Protéiques Assisté par Chaperonnes ». Dans ce schéma, des chaperonnes spécialisées stabilisent des sous-unités fragiles, rapprochent les paires appropriées et bloquent temporairement les sites de liaison des cargaisons jusqu’à ce que le complexe soit entièrement formé et sûr à déployer. 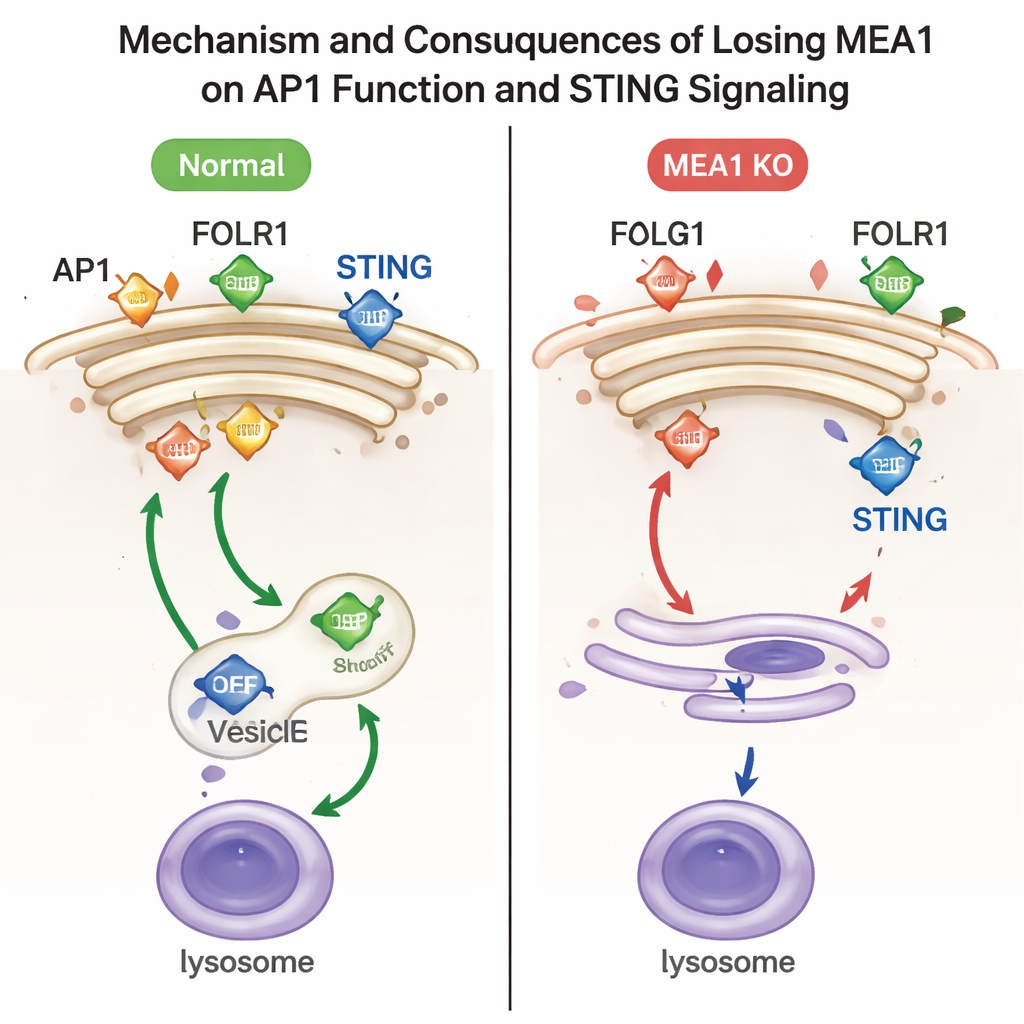
Ce que cela signifie pour la santé et la maladie
Pour les non-spécialistes, l’essentiel est que MEA1 est un acteur crucial en coulisses qui aide à assembler AP1, une machine de tri centrale dans nos cellules. Lorsque MEA1 est absent, AP1 se désagrège, des embouteillages se forment et des régulateurs importants comme STING ne sont pas correctement éteints. Cette nouvelle compréhension pourrait éventuellement aider à expliquer certains troubles immunitaires ou d’autres maladies liés à un trafic protéique défaillant, et elle révèle un principe général sur la manière dont les cellules construisent en toute sécurité des machines moléculaires complexes à partir de composants instables.
Citation: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Mots-clés: trafic des protéines, protéine adaptatrice AP1, chaperonnes moléculaires, signalisation STING, biologie cellulaire