Clear Sky Science · fr
Reconnaissance moléculaire de la thyroglobuline par la sortiline
Comment les cellules thyroïdiennes décident quand libérer l’hormone
Les hormones thyroïdiennes règlent notre « thermostat » métabolique, influençant tout, du rythme cardiaque à la température corporelle. Ces hormones sont fabriquées et stockées à l’intérieur d’une très grande protéine appelée thyroglobuline. Cette étude révèle comment une autre protéine, la sortiline, aide les cellules thyroïdiennes à choisir quelle forme de thyroglobuline reprendre à l’intérieur de la cellule afin que l’hormone puisse être libérée dans la circulation — une décision qui détermine in fine la quantité d’hormone thyroïdienne disponible pour l’organisme.
Une protéine de stockage en attente d’être traitée
La thyroglobuline est une protéine massive en forme de Y, produite et sécrétée par les cellules thyroïdiennes dans une matrice gélatineuse appelée colloïde. Là, elle sert à la fois de matière première et d’entrepôt pour l’hormone thyroïdienne : certains résidus d’acides aminés au sein de la thyroglobuline sont chimiquement iodés pour devenir des hormones thyroïdiennes, tout en restant intégrés à la plus grande protéine. Pour libérer ces hormones, la thyroglobuline doit être reprise dans la cellule, fragmentée dans des compartiments de recyclage appelés lysosomes, puis ses fragments hormonaux exportés vers le sang.
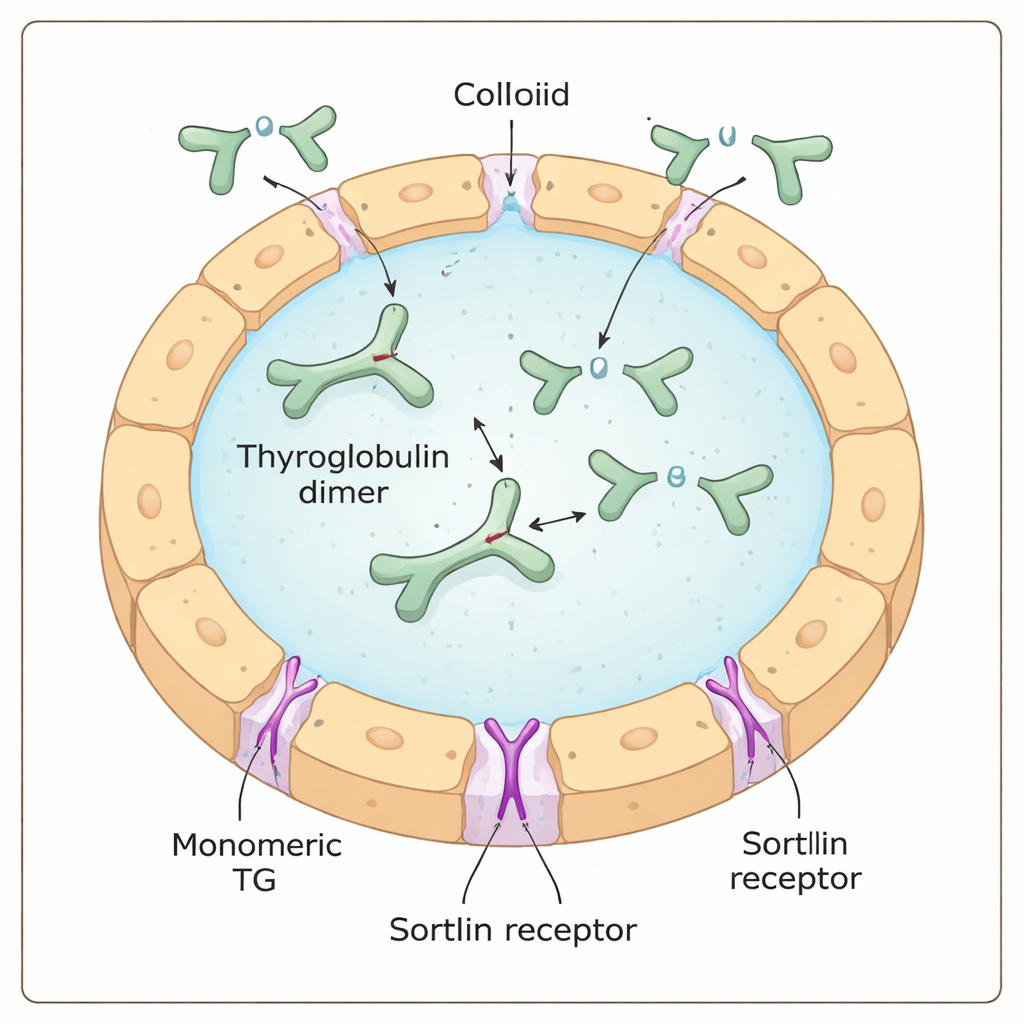
Un portier cellulaire avec une préférence cachée
Le récepteur sortiline a été proposé comme l’un des « portiers » qui se lient à la thyroglobuline à la surface cellulaire et la guident vers l’intérieur. Des travaux antérieurs suggéraient que la sortiline préférait la thyroglobuline fortement iodée, laissant entendre que le récepteur pourrait d’une façon ou d’une autre détecter directement la teneur en iode. En combinant des tests biochimiques, des mesures de masse monocellulaire et des expériences d’absorption en culture cellulaire, les auteurs ont plutôt montré que la sortiline favorise fortement la forme monomère (à unité simple) de la thyroglobuline par rapport à sa forme plus courante, dimérique (paire). Plus il y a de monomères dans un échantillon, plus ils forment efficacement des complexes avec la sortiline et sont internalisés par les cellules thyroïdiennes, indépendamment de la quantité d’iode qu’ils contiennent.
Zoom sur le point de contact
Pour comprendre cette préférence au niveau atomique, l’équipe s’est tournée vers la cryo–microscopie électronique à haute résolution et la spectrométrie de masse après réticulation. Ces méthodes ont montré que la sortiline reconnaît une courte queue flexible située à l’extrémité C-terminale (une des extrémités) de la thyroglobuline monomérique. Cette queue s’insère dans une cavité centrale de la sortiline, façonnée comme une hélice à dix pales, et s’ancre sur deux petits « points chauds » internes. De manière frappante, dans la forme dimérique de la thyroglobuline, une partie de la région entourant cette queue est enfouie et inaccessible à la sortiline, ce qui explique pourquoi le dimère interagit mal. Les données suggèrent que l’éclaircissement extracellulaire ou le relâchement de la thyroglobuline — via une dégradation protéique naturelle — contribue à convertir les dimères en monomères que la sortiline peut saisir.
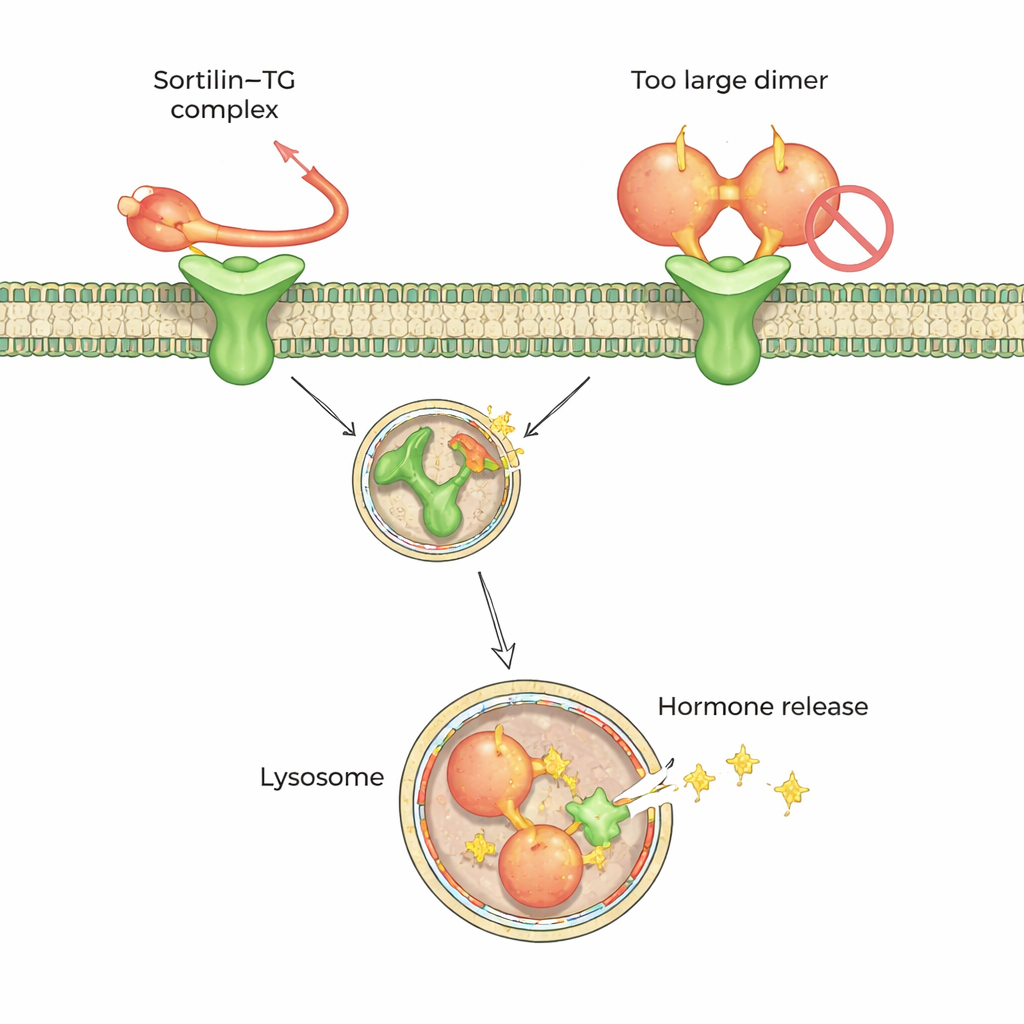
Un code d’amarrage partagé par de nombreuses cargaisons protéiques
La sortiline n’est pas seulement une protéine thyroïdienne ; elle participe au trafic de nombreuses molécules dans l’organisme, y compris de facteurs liés aux maladies cardiaques et aux troubles cérébraux. En combinant leur travail structural avec des outils avancés de prédiction de structure comme AlphaFold et AlphaPulldown, les chercheurs ont comparé comment des dizaines de partenaires connus de la sortiline pourraient se lier à sa cavité en forme de rotor. Ils ont trouvé un motif récurrent : de nombreuses cargaisons présentent un segment peptidique non structuré d’environ vingt acides aminés qui s’insère dans la même poche que la queue de la thyroglobuline, parfois dans le même sens que un peptide cérébral connu, la neurotensine, et parfois dans le sens inverse. Malgré cette orientation inversée, ces peptides partagent des caractéristiques similaires — un groupe acide ou chargé négativement à une extrémité, un résidu aromatique volumineux à l’autre, et un segment flexible souvent riche en prolines entre les deux.
Pourquoi l’iode importe moins que la forme
Comme le contact clé entre la sortiline et la thyroglobuline est cette queue flexible, les auteurs ont testé si l’addition d’iode sur une tyrosine formant l’hormone dans la queue modifiait la liaison. Il n’en fut rien : un peptide synthétique portant une hormone thyroïdienne pleinement formée se comportait presque identiquement à la version non modifiée. La modélisation a montré que l’anneau iodé dépasse dans le solvant sans créer de nouveaux contacts serrés. Avec les expériences d’absorption, cela appuie une vue révisée : la sortiline ne « compte » pas les atomes d’iode sur la thyroglobuline. Elle détecte plutôt si la protéine s’est détendue ou a été partiellement dégradée suffisamment pour exposer sa forme monomérique et sa queue de manière accessible.
Ce que cela signifie pour la santé thyroïdienne
Pour un non-spécialiste, le message central est que la libération des hormones thyroïdiennes est contrôlée moins par un capteur intégré d’iode que par une vérification mécanique de la forme et de la flexibilité des protéines. La sortiline agit comme un scanner à la surface cellulaire, recherchant des molécules de thyroglobuline qui ont été assouplies ou rognées en monomères, puis les internalise pour la libération finale des hormones et le recyclage de l’iode. Ce travail clarifie une étape clé de la biologie des hormones thyroïdiennes et suggère que des médicaments visant à bloquer la sortiline — aujourd’hui étudiés pour d’autres maladies — pourraient involontairement modifier la gestion des hormones thyroïdiennes en perturbant cette étape de reconnaissance.
Citation: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Mots-clés: hormone thyroïdienne, thyroglobuline, sortiline, trafic des protéines, endocytose