Clear Sky Science · fr
L’hélice pontée de Cas12a est un régulateur allostérique de la formation du R-loop et de l’activation de RuvC
Pourquoi cela compte pour l’édition génétique
De nombreux outils puissants d’édition génétique, y compris ceux utilisés dans des thérapies émergentes et des tests diagnostiques rapides, reposent sur des protéines CRISPR qui coupent l’ADN à des sites choisis. Mais si ces ciseaux moléculaires sectionnent le mauvais endroit, ils peuvent provoquer des effets secondaires nocifs. Cette étude dissèque une petite pièce mobile à l’intérieur de l’éditeur Cas12a, appelée hélice pontée, et montre comment ses changements de conformation agissent comme un interrupteur de sécurité interne liant la reconnaissance correcte de la cible à la coupure de l’ADN. Comprendre cet interrupteur offre une feuille de route pour concevoir des outils CRISPR à la fois plus précis et plus sûrs pour les applications médicales et biotechnologiques.
Une pince moléculaire aux pièces mobiles
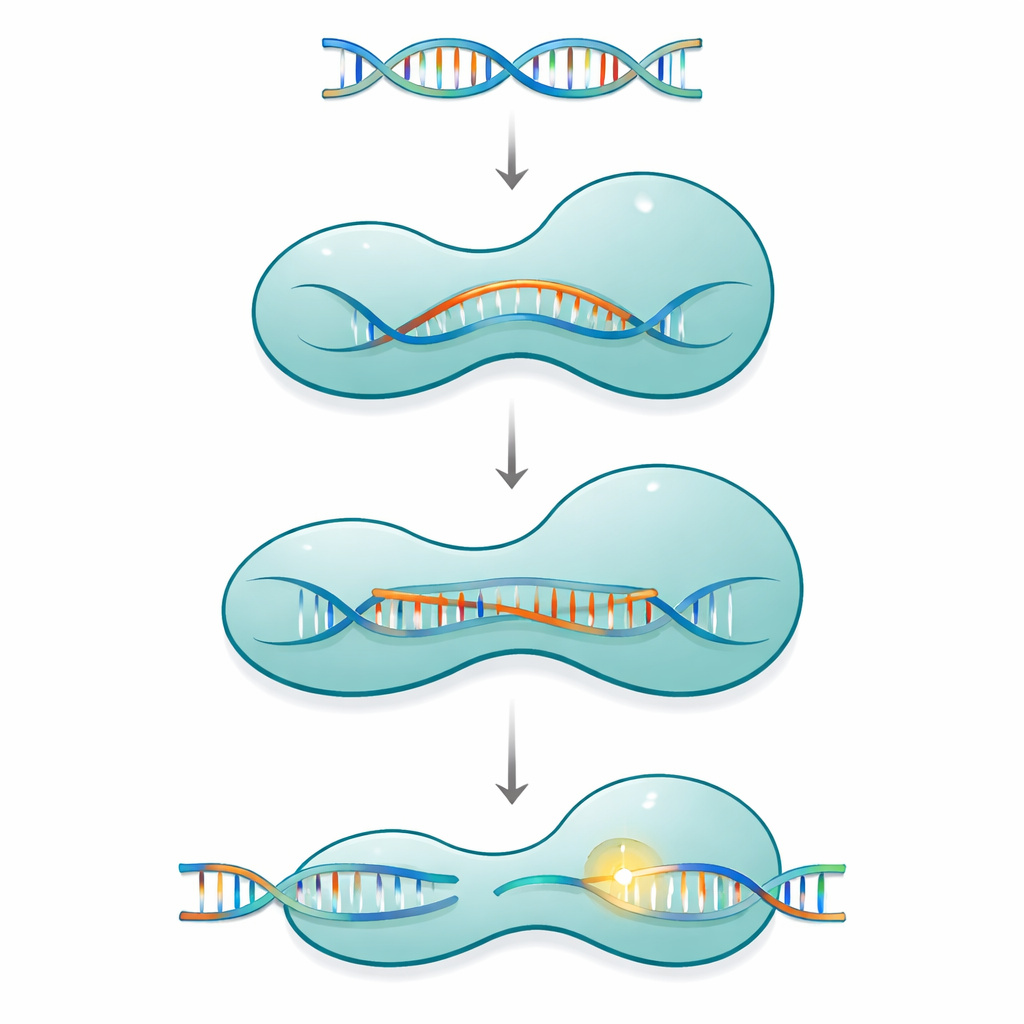
Cas12a appartient à une famille de systèmes CRISPR mono-protéiques qui utilisent un court ARN guide pour trouver et couper l’ADN correspondant dans des virus ou dans le génome d’une cellule. La protéine a la forme d’une pince à deux bras : un côté de reconnaissance qui vérifie la séquence, et un côté de coupure qui abrite la machinerie chimique. Ces deux moitiés sont reliées par un segment mince et chargé positivement appelé hélice pontée. Lorsque Cas12a se lie à son ARN guide puis à sa cible ADN, la protéine ne se comporte pas comme un outil rigide. Elle traverse plutôt une série de grands et petits changements de forme qui se referment progressivement autour d’un hybride ARN–ADN croissant, connu sous le nom de R-loop, n’activant pleinement le site de coupure que lorsqu’une longueur suffisante d’appariements corrects est formée.
Explorer l’interrupteur de sécurité intégré
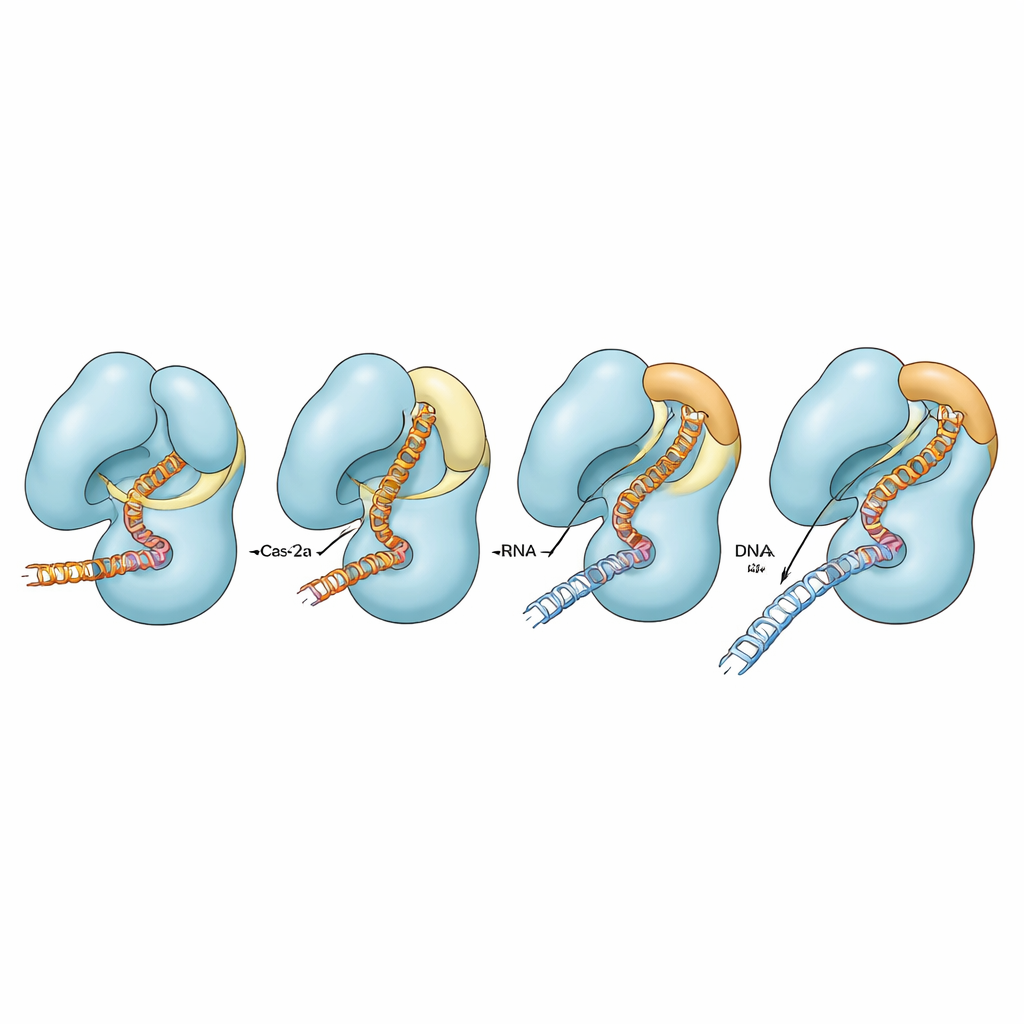
Les chercheurs se sont concentrés sur un Cas12a provenant de la bactérie Francisella novicida et sur une version précédemment conçue dans laquelle deux acides aminés de l’hélice pontée ont été remplacés par des prolines, un changement connu pour rigidifier ou rompre les hélices. Cette variante, appelée FnoCas12aKD2P, coupe l’ADN de façon plus sélective mais plus lente que la protéine naturelle. Grâce à la cryo–microscopie électronique, ils ont capturé cinq instantanés structurels distincts de cette variante liée à son ARN guide et à un fragment d’ADN cible. Ces clichés montrent la protéine à différents stades de sa voie d’activation, depuis la reconnaissance initiale de l’ADN jusqu’à des états plus avancés où une partie de l’hybride ARN–ADN est formée mais où la pleine préparation à la coupure n’est pas encore atteinte.
Comment les changements de conformation entraînent une coupure précise
La comparaison de la variante avec des structures de Cas12a normales précédemment déterminées a révélé un schéma clair. Chez la protéine naturelle, un segment de l’hélice pontée se convertit d’une boucle lâche en une hélice plus longue et droite et se courbe vers l’hybride ARN–ADN en croissance, entrant en contact étroit avec lui. Simultanément, une hélice voisine dans le domaine de coupure se relâche, et une petite région appelée la « languette », qui bloque normalement le site actif, bascule d’une boucle à une hélice et s’ouvre. Ensemble, ces mouvements coordonnés ouvrent une poche qui permet à un brin d’ADN simple de pénétrer et d’être coupé. Dans la variante contenant des prolines, l’hélice pontée ne peut pas effectuer complètement cette transition boucle→hélice ni se courber correctement. En conséquence, l’hybride ARN–ADN reste déformé et plus éloigné, la languette demeure dans un état fermé semblable à une boucle, et le complexe atteint rarement une conformation entièrement pré‑catalytique. Cet goulot mécanique ralentit la coupure sur cible et complique la pénétration d’ADN présentant des mésappariements à travers les points de contrôle internes.
Affiner la fidélité en modulant les contacts
Pour tester comment différents contacts autour de la languette et de l’hélice pontée contribuent à l’activité, les auteurs ont modifié des résidus chargés spécifiques qui relient ces régions. Dans le Cas12a normal, rompre ces contacts n’a eu que des effets modestes sur la coupure d’un ADN parfaitement apparié, bien que certaines conditions aient affecté l’efficacité de la clivage du second brin d’ADN en présence de mésappariements. Dans le contexte d’une hélice pontée altérée, cependant, les mêmes substitutions ont sévèrement réduit ou presque supprimé la coupure des deux brins, en particulier lorsque l’ARN guide et l’ADN n’étaient pas parfaitement complémentaires. Des simulations informatiques ont corroboré ces résultats, montrant que ce n’est que lorsque l’hélice pontée peut adopter pleinement sa forme hélicoïdale que la pontée, l’hélice adjacente, la languette et les acides nucléiques se déplacent de façon fortement coordonnée. Lorsque l’hélice est compromise, ces mouvements deviennent partiellement ou totalement découplés, et l’enzyme peine à compléter son cycle catalytique.
Un guide de conception pour les outils CRISPR de nouvelle génération
Dans l’ensemble, le travail révèle l’hélice pontée comme un levier de contrôle interne qui relie la longueur et la qualité de l’hybride ARN–ADN à l’ouverture de la poche de coupure chez Cas12a. En forçant la protéine à accomplir une séquence spécifique de changements de conformation avant de cliver l’ADN, ce mécanisme impose naturellement une discrimination des mésappariements. Les résultats contribuent à expliquer pourquoi des modifications ciblées dans cette petite région peuvent produire des variantes de Cas12a avec une réduction des coupures hors cible et une activité « collatérale » d’ADN diminuée, des propriétés souhaitables pour une édition du génome et des diagnostics plus sûrs. Plus largement, l’étude met en lumière comment de subtiles variations dans de courtes hélices peuvent coordonner une communication à longue portée dans de grandes machines moléculaires, offrant des principes généraux pour l’ingénierie d’enzymes de traitement des acides nucléiques à haute fidélité.
Citation: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Mots-clés: CRISPR-Cas12a, fidélité de l’édition génétique, hélice pontée, formation du R-loop, régulation allostérique