Clear Sky Science · fr
RoboA renforce le destin des cellules souches planaires via FoxA et Anosmin1a
Comment les vers regénèrent leurs organes
Certaines plathelminthes peuvent reconstituer presque n’importe quelle partie manquante du corps, de leur tube alimentaire jusqu’au cerveau. Cette capacité remarquable dépend de cellules souches adultes capables de se différencier en de nombreux types cellulaires à la demande. Mais avec autant de liberté, comment ces cellules évitent-elles de construire un tissu inapproprié au mauvais endroit — par exemple des cellules stomacales dans la tête au lieu de neurones ? Cette étude utilise le planaire pour découvrir comment un petit ensemble de signaux maintient des cellules souches très flexibles dans la bonne voie lors de la régénération.
Le ver régénérant et son potentiel caché
Le planaire Schmidtea mediterranea est un modèle privilégié pour étudier la régénération car une grande population de cellules souches est répartie dans tout son corps. Un organe clé est le pharynx, un tube musculaire d’alimentation situé au milieu du ver et qui se connecte à l’extérieur lorsque l’animal se nourrit. Des travaux antérieurs ont montré qu’un gène appelé foxA est crucial pour reconstruire ce pharynx après une lésion, et que seules certaines cellules souches proches du pharynx activent normalement foxA. La nouvelle étude pose une question apparemment simple : qu’est-ce qui empêche les cellules souches d’autres régions — en particulier la tête et le cerveau — de choisir elles aussi une identité de pharynx ?
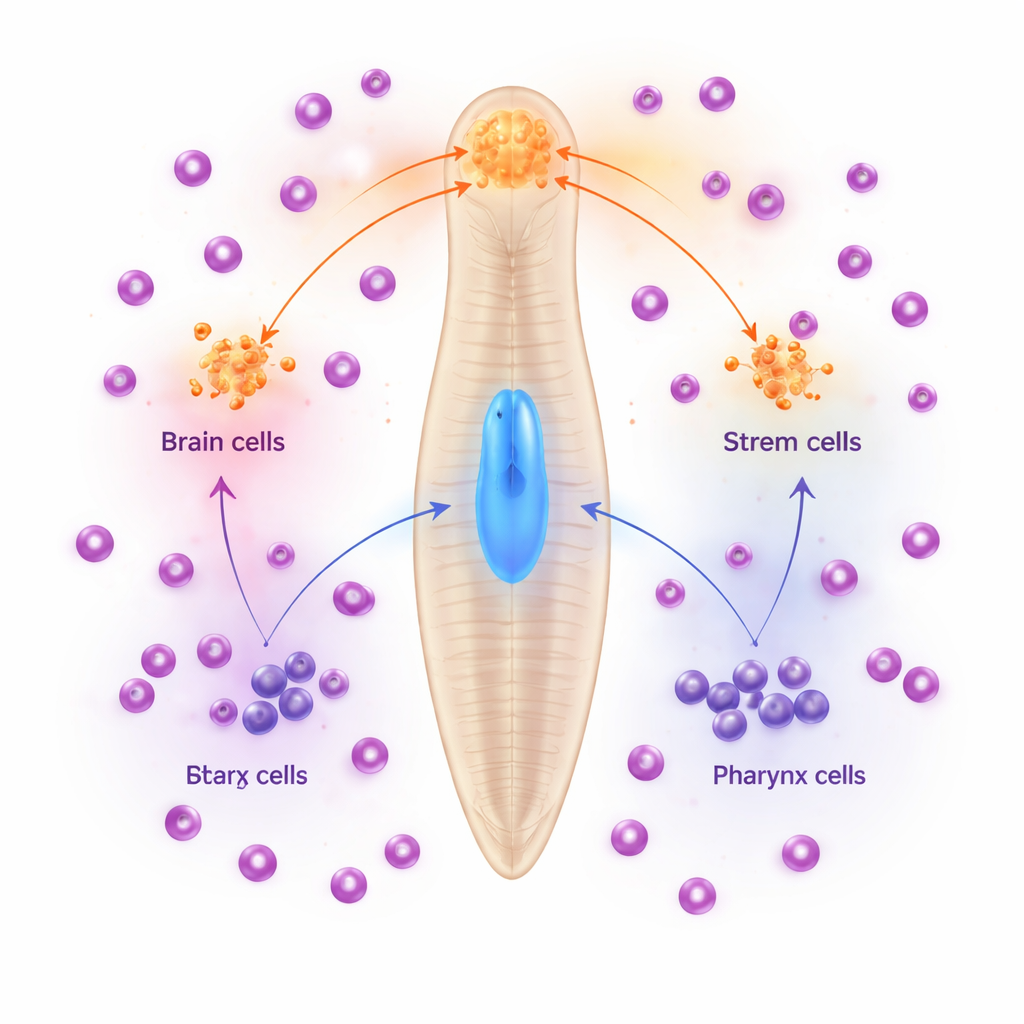
Quand l’orientation fait défaut
Les chercheurs se sont concentrés sur une protéine réceptrice appelée RoboA, présente à faibles niveaux dans de nombreux types cellulaires, y compris les cellules souches. Lorsqu’ils ont réduit l’activité de RoboA par interférence ARN, les animaux développaient souvent des pharynx supplémentaires et mal placés après amputation. Un examen plus attentif a révélé quelque chose de plus subtil : même chez des vers non blessés, la diminution de RoboA entraînait l’apparition de neurones et de muscles de type pharynx dans la région cérébrale. Ces « neurones pharyngés ectopiques » exprimaient des gènes caractéristiques du pharynx, mais se trouvaient au mauvais endroit. Fait important, le plan corporel global et l’architecture cérébrale restaient en grande partie intacts, ce qui suggère que RoboA ne remodelait pas l’animal entier, mais ajustait finement ce que devenaient les cellules souches voisines.
Un commutateur à trois acteurs pour le destin cellulaire
Pour comprendre le fonctionnement de RoboA, l’équipe a cherché des partenaires extérieurs à la cellule. Bien que les protéines Robo soient surtout connues pour se lier à un ligand appelé Slit, l’inhibition de Slit n’a pas reproduit l’apparition des cellules pharyngées mal placées. Un écran RNAi étendu ciblant les protéines sécrétées et membranaires a plutôt identifié Anosmin1a (Anos1a), une protéine sécrétée apparentée à un facteur humain impliqué dans le syndrome de Kallmann. La réduction d’Anos1a provoquait des neurones pharyngés supplémentaires semblables, et les doubles inactivations RoboA–Anos1a se comportaient comme s’ils intervenaient dans la même voie. Parallèlement, le profilage moléculaire a montré que le facteur de transcription FoxA est au cœur de la décision : lorsque RoboA est présent, il maintient FoxA éteint dans les cellules souches de la tête ; quand la signalisation RoboA est supprimée, FoxA s’active et ces mêmes cellules souches peuvent adopter une identité de neurone pharyngé même en restant dans le cerveau.
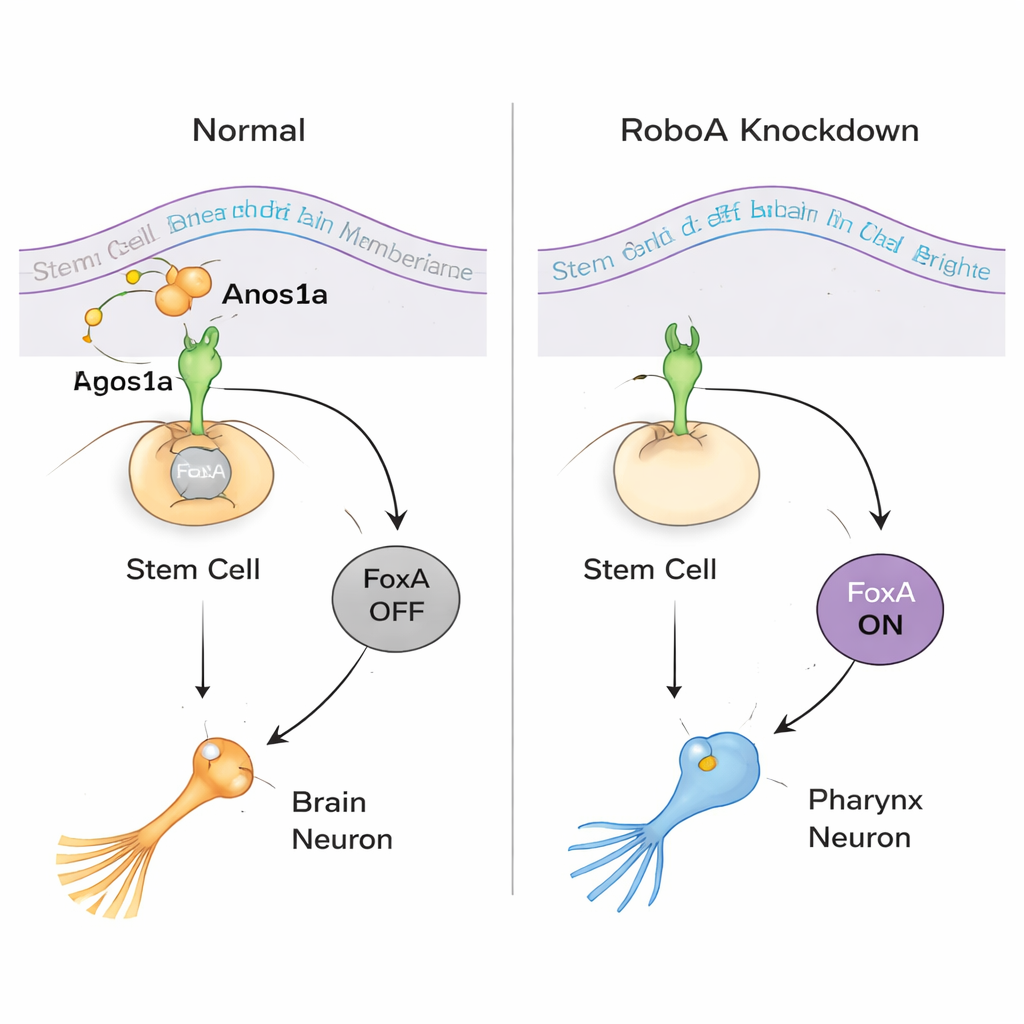
Mettre au jour un choix bidirectionnel chez les cellules souches
L’équipe s’est ensuite demandé si cette flexibilité fonctionnait dans les deux sens. Chez les animaux normaux, les cellules souches autour du pharynx dépendent de FoxA pour devenir des neurones pharyngés et des cellules épithéliales, tandis que les muscles du pharynx suivent une voie différente. Lorsque FoxA a été inhibé pendant des périodes prolongées, les vers ont perdu leurs pharynges et développé des excroissances anormales au milieu du corps. Le séquençage ARN unicellulaire et l’analyse des marqueurs ont révélé que ces excroissances contenaient de nombreux types cellulaires normalement limités à la tête, y compris des cellules oculaires et des neurones spécifiques au cerveau. En d’autres termes, lorsque FoxA manque là où le pharynx devrait se former, les cellules souches locales dérivent par défaut vers un destin de type cérébral. Cette découverte montre que les mêmes cellules souches peuvent être poussées soit vers une identité « pharynx », soit vers une identité « cerveau » selon les signaux qu’elles reçoivent.
Affiner la régénération, sans redessiner la carte
En rassemblant toutes les preuves, les auteurs proposent que la régénération des planaires soit guidée sur deux niveaux. Des signaux de « contrôle de position » larges, tels que Wnt et d’autres molécules de patterning, établissent la carte grossière de la tête, du tronc et de la queue. Par-dessus cela, des gènes locaux « renforçant le destin » comme RoboA et Anos1a agissent comme des dispositifs de sécurité, bloquant les options inappropriées. Dans la tête, la signalisation RoboA–Anos1a maintient FoxA éteint afin que les cellules souches produisent des neurones cérébraux plutôt que des cellules pharyngées ; près du pharynx, FoxA peut s’activer et promouvoir des destins spécifiques au pharynx. Ce contrôle en couches permet aux cellules souches planaires de rester extraordinairement plastiques tout en reconstruisant les organes au bon endroit, offrant un schéma expliquant comment une régénération robuste peut coexister avec un ordre anatomique strict.
Citation: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Mots-clés: régénération des planaires, plasticité des cellules souches, patterning des organes, signalisation RoboA, facteur de transcription FoxA