Clear Sky Science · fr
NeoPrecis : améliorer la prédiction de la réponse à l’immunothérapie par l’intégration de néoantigènes qualifiés et d’un paysage clonality-aware
Pourquoi certains cancers répondent à l’immunothérapie et d’autres non
L’immunothérapie a transformé la prise en charge du cancer, mais de nombreux patients n’en bénéficient toujours pas et certains subissent des effets secondaires graves. Une grande question est de savoir pourquoi certains tumeurs sont repérées et détruites par le système immunitaire tandis que d’autres passent inaperçues. Cette étude présente NeoPrecis, une méthode computationnelle qui examine plus finement les « drapeaux » que les tumeurs exhibent au système immunitaire — appelés néoantigènes — et qui utilise ces informations pour mieux prédire quels patients sont susceptibles de répondre aux immunothérapies modernes.
De nouveaux signaux à la surface des cellules cancéreuses
Les cellules cancéreuses accumulent des mutations de l’ADN qui peuvent modifier les protéines qu’elles produisent. De petits fragments de ces protéines altérées, appelés néoantigènes, peuvent être exposés à la surface cellulaire et reconnus comme étrangers par les cellules T, les effectrices du système immunitaire. Pendant des années, médecins et chercheurs se sont appuyés sur des mesures grossières telles que la charge mutationnelle tumorale — le nombre total de mutations — pour estimer la probabilité de réponse aux inhibiteurs de points de contrôle. Mais cet indicateur est approximatif : toutes les mutations ne génèrent pas une cible visible ou attrayante pour les cellules T, et les tumeurs peuvent être des mosaïques de nombreux sous-types cellulaires. NeoPrecis a été conçu pour dépasser le simple comptage des mutations et évaluer combien d’entre elles sont réellement des cibles prometteuses à l’échelle de la tumeur entière.
Examiner trois ingrédients clés simultanément
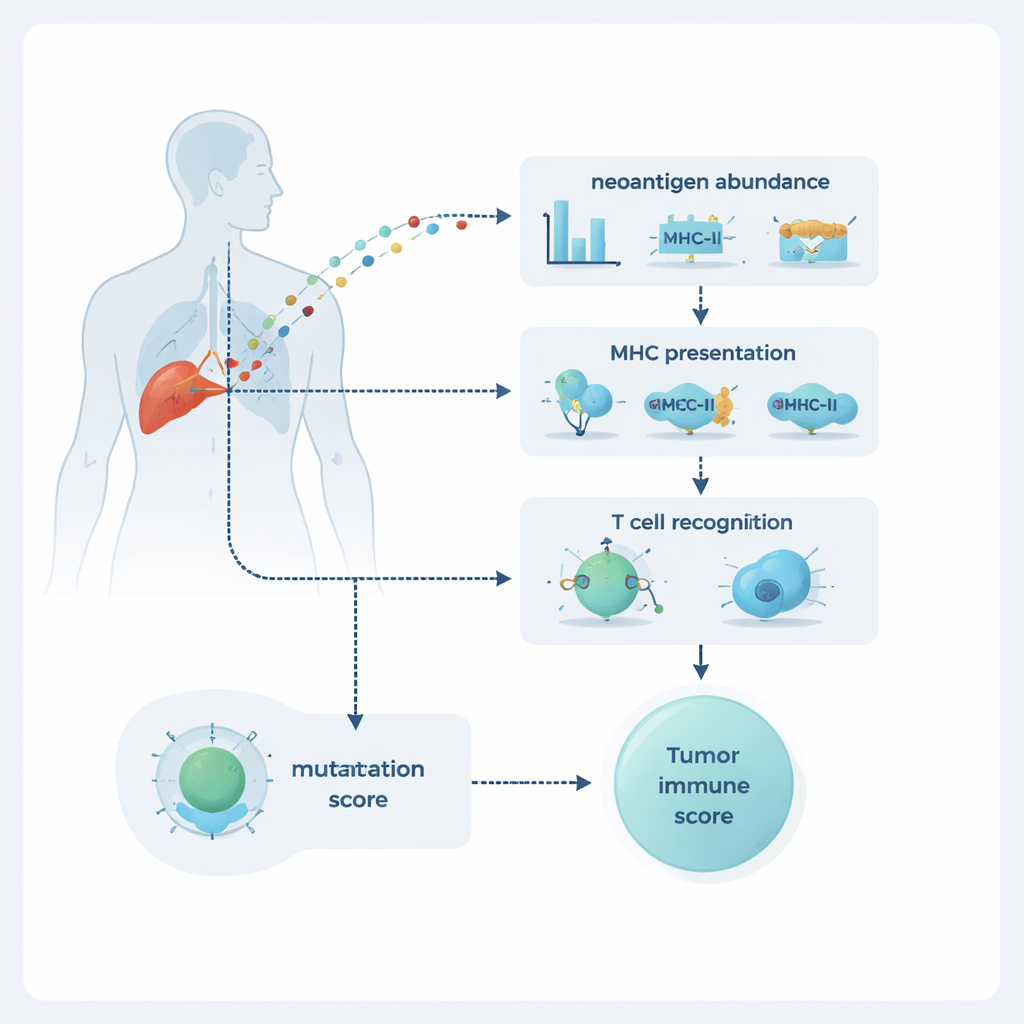
NeoPrecis évalue chaque mutation selon trois dimensions : son abondance dans la tumeur, sa probabilité d’être présentée à la surface cellulaire, et sa probabilité d’être repérée par les cellules T. L’abondance est estimée à partir du séquençage ADN et ARN, qui révèle la fréquence de la mutation et l’intensité de son expression. La présentation est modélisée via la liaison aux molécules du CMH de classe I et II, qui font office de panneaux d’affichage montrant des fragments protéiques aux cellules T. La partie la plus novatrice est le composant de reconnaissance par les cellules T, NeoPrecis-Immuno. Ce modèle apprend à partir de larges bases de données d’interactions connues entre cellules T et peptides pour évaluer en quoi un fragment muté diffère de son homologue normal d’une manière pertinente pour la reconnaissance par les cellules T, tout en tenant compte des variants spécifiques de CMH que porte chaque individu.
Apprendre à un ordinateur ce que les cellules T « voient »
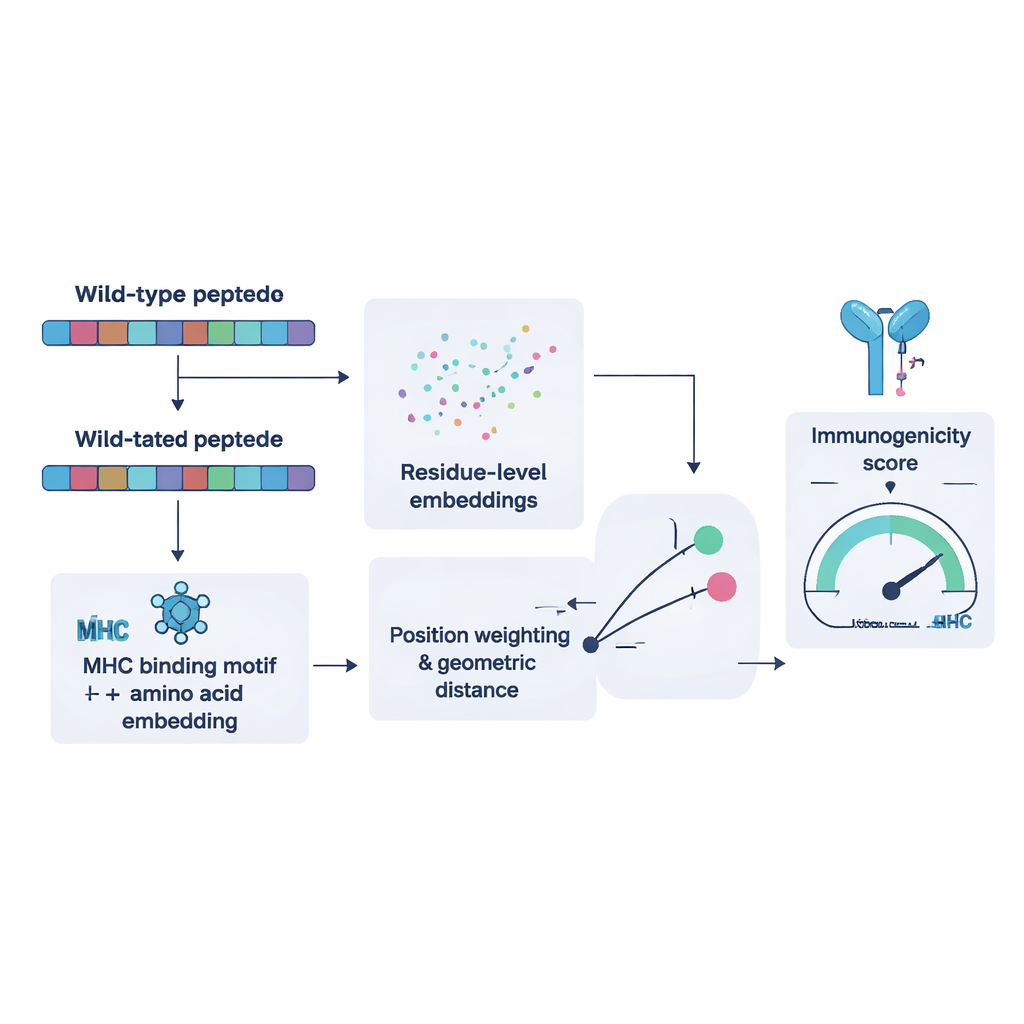
Pour entraîner NeoPrecis-Immuno, les chercheurs ont d’abord rassemblé des milliers d’exemples où la même cellule T reconnaît plusieurs peptides similaires et d’autres qu’elle ne reconnaît pas. Ils s’en sont servis pour enseigner au modèle que les fragments mutants très proches des fragments normaux ont moins de chances de déclencher une attaque immunitaire, car ces cibles semblables au soi sont généralement éliminées lors du développement des cellules T. Le modèle représente chaque peptide comme un point dans un espace mathématique façonné à la fois par sa séquence d’acides aminés et par les préférences de liaison des molécules CMH de l’individu. Il mesure ensuite à quelle distance se trouve le peptide muté par rapport à l’original. Des distances plus grandes, informées par des motifs, correspondent à une probabilité plus élevée d’immunogénicité. Testé face aux outils existants sur des jeux de données indépendants de cancers, NeoPrecis-Immuno a égalé ou surpassé ces outils, en particulier pour le CMH de classe II, qui présente aux cellules T auxiliaires participant et soutenant les réponses anti‑tumorales.
Des mutations individuelles à la tumeur entière
Les mutations individuelles ne racontent qu’une partie de l’histoire ; leur répartition au sein de la tumeur importe aussi. Certaines mutations sont « clonales », présentes dans presque toutes les cellules tumorales, tandis que d’autres sont « sous‑clonales », limitées à des poches spécifiques. NeoPrecis construit un « paysage de néoantigènes » en sommant ses scores d’immunogénicité à travers les mutations et en superposant des informations sur les sous‑clones auxquels elles appartiennent et sur la prévalence de ces sous‑clones. Cela produit des scores au niveau tumoral qui mettent en avant les cancers riches en néoantigènes forts et largement partagés — en particulier ceux pouvant être présentés à la fois par le CMH de classe I et de classe II et susceptibles de déclencher des réponses coordonnées des cellules T auxiliaires et cytotoxiques. Dans des cohortes de patients atteints de mélanome et de cancer du poumon non à petites cellules traités par inhibiteurs de points de contrôle, ces scores basés sur NeoPrecis ont séparé plus précisément les répondeurs des non‑répondeurs que le simple comptage des mutations, et se sont montrés particulièrement utiles dans les tumeurs pulmonaires complexes et hétérogènes.
Ce que cela signifie pour les patients
Pour les patients, la promesse de NeoPrecis est un appariement plus précis des immunothérapies aux personnes les plus susceptibles d’en bénéficier, et une compréhension plus claire des raisons pour lesquelles certaines tumeurs résistent au traitement. En se concentrant sur la qualité et la distribution des néoantigènes — et non seulement sur leur quantité — le cadre aide à expliquer pourquoi des tumeurs avec des charges mutationnelles similaires peuvent se comporter très différemment. À l’avenir, de telles cartes détaillées du paysage immuno‑visible d’une tumeur pourraient guider non seulement l’utilisation des inhibiteurs de points de contrôle, mais aussi la conception de vaccins anticancéreux personnalisés qui priorisent les cibles les plus puissantes et les plus largement partagées au sein du cancer de chaque personne.
Citation: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Mots-clés: immunothérapie du cancer, néoantigènes, hétérogénéité tumorale, inhibiteurs de points de contrôle, oncologie computationnelle