Clear Sky Science · fr
NR6A1 est essentiel pour la spécification, la formation et la survie des cellules de la crête neurale
Comment les décisions cellulaires précoces façonnent le visage et le corps
Avant notre naissance, un groupe particulier de cellules, appelé cellules de la crête neurale, migre dans l’embryon pour participer à la construction du visage, du cœur, des nerfs, et d’autres structures. Lorsque ces cellules dysfonctionnent, des malformations congénitales graves peuvent survenir. Cette étude met en lumière un commutateur moléculaire jusqu’ici sous-estimé — une protéine nommée NR6A1 — qui contribue à décider quand et où les cellules de la crête neurale se forment chez les mammifères, et ce qui se passe lorsque ce commutateur fait défaut.
Les bâtisseurs vagabonds de l’embryon
Les cellules de la crête neurale apparaissent très tôt au cours du développement, le long de la frontière du cerveau et de la moelle épinière en formation. Après s’être détachées de ce tissu, elles migrent sur de longues distances pour générer de nombreuses structures différentes, des os et cartilages faciaux à des éléments du système nerveux périphérique et aux cellules pigmentaires de la peau. Parce qu’elles contribuent à tant d’organes, même de petites perturbations de leur formation peuvent provoquer des pathologies étendues appelées neurocristopathies, y compris des syndromes craniofaciaux comme la maladie de Treacher Collins. Comprendre comment ces cellules apparaissent pour la première fois est donc essentiel pour expliquer à la fois le développement normal et les anomalies congénitales.
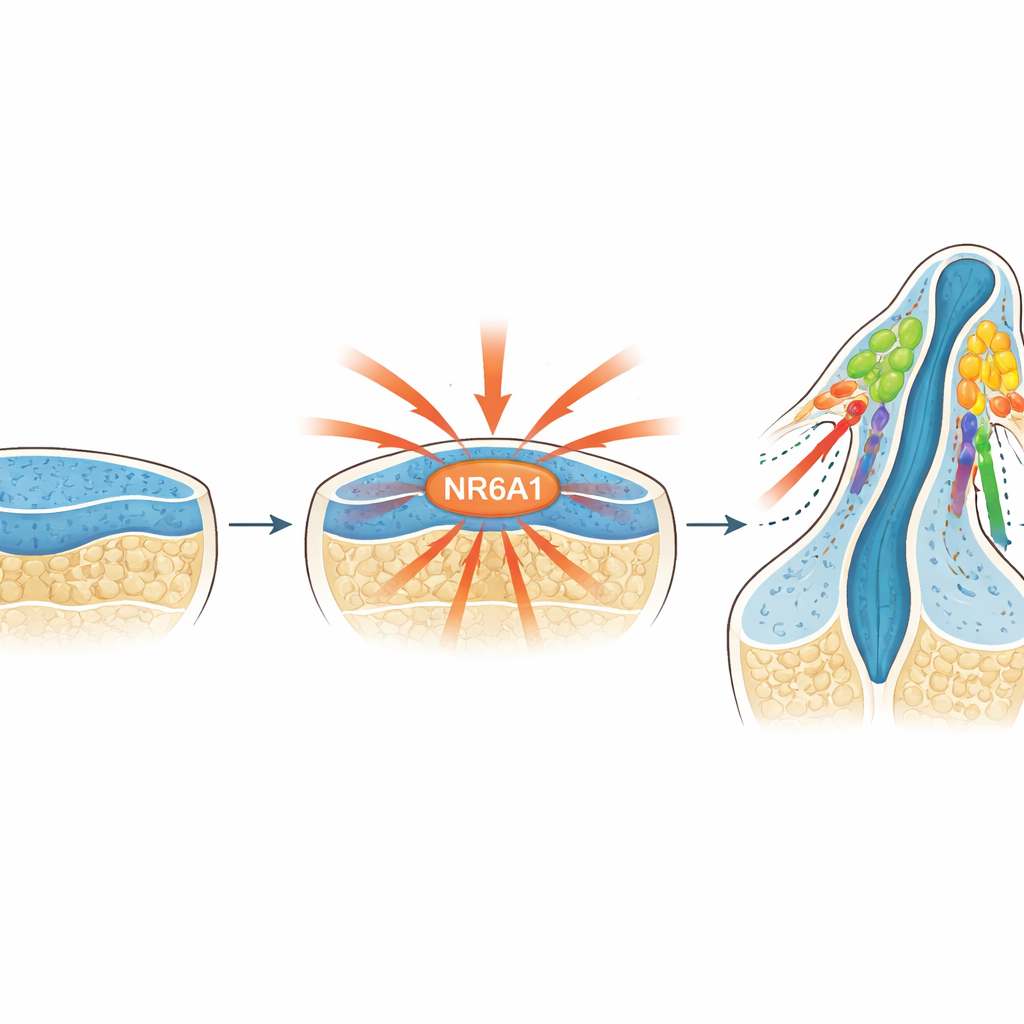
Un commutateur maître nouvellement reconnu
Les chercheurs se sont concentrés sur NR6A1, un membre de la famille des récepteurs nucléaires qui régulent l’activité des gènes. Des travaux antérieurs laissaient entendre que NR6A1 pourrait être impliqué dans des malformations de la tête et du visage, mais son rôle dans les cellules de la crête neurale était inconnu. En suivant NR6A1 chez des embryons de souris dès juste après l’implantation, l’équipe a constaté que sa présence correspond étroitement aux lieux et moments où naissent normalement les cellules de la crête neurale : elle apparaît dans le tissu neural précoce, se concentre le long du côté dorsal du cerveau et de la moelle en développement, et est aussi observée dans les cellules au moment où elles quittent ce tissu pour commencer à migrer.
Que se passe-t-il quand le commutateur manque
Les souris dépourvues de NR6A1 meurent précocement durant le développement, aussi l’équipe a-t-elle examiné des embryons juste avant ce point. Ils ont observé une pénurie sévère de cellules de la crête neurale, en particulier derrière le premier arc qui formera des parties de la mâchoire et du cou, où les cellules migratrices de la crête neurale étaient presque entièrement absentes. Les programmes géniques clés qui marquent normalement l’identité de la crête neurale et permettent aux cellules de se détacher et de migrer étaient fortement diminués. Parallèlement, les gènes qui maintiennent les cellules dans un état de type souche, hautement prolifératif, restaient activés, et de nombreuses cellules ressemblant à des cellules de la crête neurale qui se formaient mouraient rapidement. Ces résultats indiquent que sans NR6A1, les cellules souches neurales n’arrivent pas à effectuer correctement la transition vers des cellules de la crête neurale migratoires et ne peuvent pas survivre.
Éteindre la pluripotence et activer le mouvement
Pour comprendre comment NR6A1 exerce ce contrôle, les auteurs ont combiné plusieurs techniques moléculaires puissantes, y compris le séquençage ARN unicellulaire, le cartographiage de l’accessibilité de la chromatine et des essais ciblés d’interaction ADN–protéine, tant chez la souris que dans des cellules humaines dérivées de cellules souches devenues crête neurale. Ils ont trouvé que NR6A1 se lie physiquement à des motifs d’ADN spécifiques près de gènes qui contrôlent deux programmes antagonistes : l’un qui maintient la pluripotence (la capacité de devenir de nombreux types cellulaires) et l’autre qui impulse l’identité de la crête neurale et la migration cellulaire. Lorsque NR6A1 est présent, la chromatine autour de gènes de « stemness » tels qu’Oct4 et Nanog devient moins accessible et ces gènes sont réprimés, tandis que les régions proches des gènes de la crête neurale et de la transition épithélio–mésenchymateuse s’ouvrent et s’activent. La surexpression d’Oct4 durant la fenêtre critique de formation de la crête neurale a reproduit l’effet de la perte de NR6A1, montrant ainsi que la pluripotence doit être mise en sourdine pour que les cellules de la crête neurale émergent.
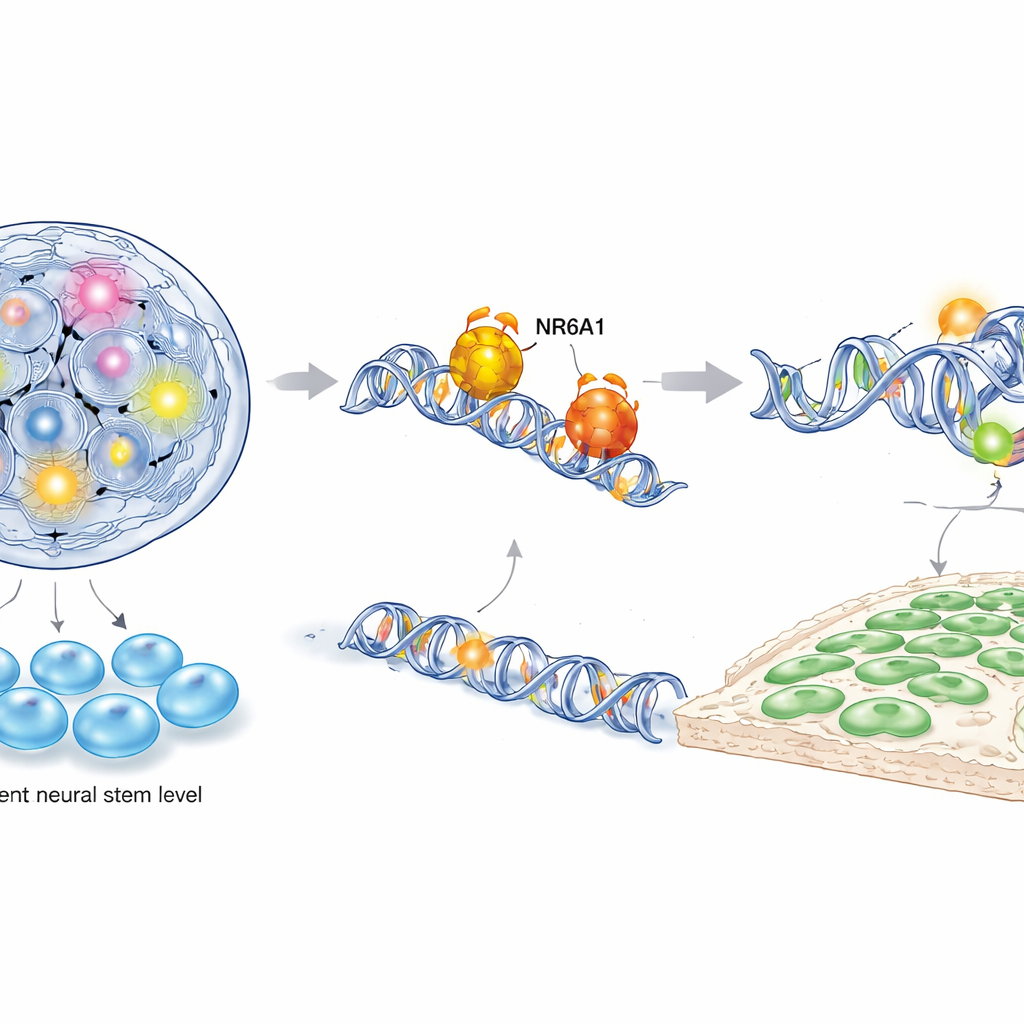
Réécrire la chronologie du développement précoce
L’étude révise également le calendrier du moment où les cellules de la crête neurale commencent à être spécifiées chez les mammifères. En utilisant un système génétique inductible pour supprimer NR6A1 à différents moments, l’équipe a montré que sa suppression à la mi-gastrulation — un stade plus précoce que traditionnellement envisagé — suffisait à bloquer l’activation des gènes de la crête neurale. En revanche, supprimer NR6A1 plus tard, y compris avec une lignée conductrice largement utilisée et supposée spécifique de la crête neurale, n’a produit aucun défaut évident. Cela signifie que des décisions cruciales concernant le destin de la crête neurale sont prises avant que ces outils standards n’entrent en action, ce qui explique pourquoi certaines études antérieures chez la souris ont pu manquer ces exigences précoces.
Pourquoi c’est important pour les malformations congénitales et les maladies
Dans l’ensemble, ce travail révèle NR6A1 comme un coordinateur central qui aide les cellules souches neurales à « grandir » en cellules de la crête neurale en réprimant simultanément les programmes de pluripotence et en activant les programmes de migration et de survie. Cette double action semble commencer à la mi-gastrulation, plus tôt qu’on ne le reconnaissait auparavant chez les mammifères, et rapproche le développement de la souris de celui d’autres vertébrés. En clarifiant quand et comment ce commutateur fonctionne, l’étude fournit un cadre pour réinterpréter des expériences génétiques antérieures, identifier de meilleurs outils pour étudier la biologie de la crête neurale, et finalement comprendre et potentiellement prévenir les neurocristopathies qui résultent d’une défaillance de cette décision développementale précoce.
Citation: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Mots-clés: cellules de la crête neurale, NR6A1, développement embryonnaire, interrupteur de pluripotence, neurocristopathie