Clear Sky Science · fr
Ingénierie du système MmeFz2-ωRNA pour une édition du génome efficace via un cadre intégré computationnel-expérimental
Ciseaux génétiques plus petits pour de grands problèmes médicaux
L’édition génétique a déjà transformé la manière dont les scientifiques étudient les maladies, mais en faire une médecine sûre et utilisable demeure un défi de taille. Un obstacle majeur est que les « ciseaux » ADN les plus puissants d’aujourd’hui, comme CRISPR-Cas9, sont physiquement volumineux et difficiles à packager dans les minuscules vecteurs de délivrance utilisés chez les patients. Cette étude présente un nouvel outil d’édition génétique compact issu d’une famille d’enzymes peu connue, les Fanzor2, et montre comment l’intelligence artificielle peut le redesigner rapidement pour en faire un candidat prometteur pour de futures thérapies génétiques.
Une nouvelle classe d’éditeurs génétiques compacts
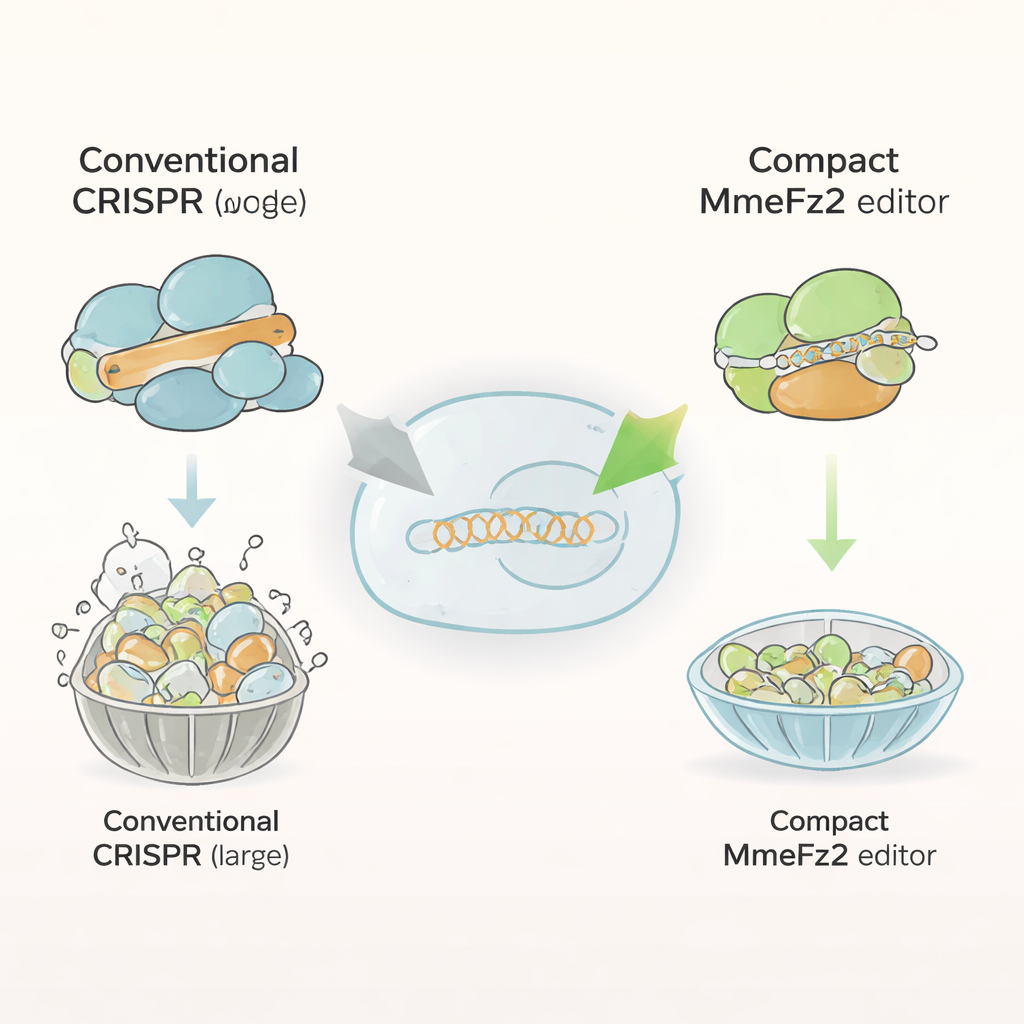
La plupart des éditeurs du génome actuels, tels que Cas9 et Cas12a, sont des protéines volumineuses composées de plus d’un millier d’acides aminés. Cette taille complique leur insertion dans les virus adéno-associés (AAV), le principal système de délivrance pour les thérapies géniques. En revanche, les protéines Fanzor2 sont beaucoup plus petites et se rencontrent naturellement chez les eucaryotes, le groupe de la vie qui inclut les animaux et les humains. Les auteurs se sont concentrés sur un membre de cette famille, MmeFz2, qui utilise une courte molécule d’ARN appelée ωRNA pour localiser et couper des séquences d’ADN spécifiques. Sur le papier, MmeFz2 semblait idéale pour la thérapie : compacte et programmable. En pratique, cependant, son activité dans les cellules humaines était médiocre, avec moins d’un pour cent des sites cibles édités. L’équipe a entrepris de transformer cette enzyme peu performante en un outil pratique.
Utiliser l’IA pour redesigner la molécule guide
La première cible fut le ωRNA, le guide qui indique à MmeFz2 où couper. En utilisant AlphaFold3, un programme de pointe qui prédit les structures 3D de complexes protéine–ARN–ADN, les chercheurs ont construit un modèle de MmeFz2 lié à son ωRNA et à une cible d’ADN. Cette structure virtuelle a révélé que certaines parties du ωRNA étaient lâches, mal appariées et à peine en contact avec la protéine. Guidée par ces informations, l’équipe a remplacé de manière systématique des liaisons instables dans l’ARN et a supprimé des séries d’uridines qui peuvent gêner la transcription. Ils ont ensuite testé des dizaines de variantes dans des cellules humaines. En combinant les meilleures modifications et en raccourcissant une tige inutile, ils ont créé un ωRNA réduit de 30 % qui a toutefois apporté près d’un gain de 20 fois en efficacité d’édition sur de nombreux sites d’ADN.
Affiner la protéine avec l’apprentissage automatique
Puis l’équipe a affiné la protéine elle-même. Ils ont de nouveau utilisé AlphaFold3 pour cartographier où MmeFz2 touchait l’ARN et l’ADN et ont conçu plus d’une centaine de substitutions d’un seul acide aminé visant à renforcer ces contacts ou améliorer la flexibilité. Après avoir criblé ces variantes dans des cellules, ils ont alimenté les données de performance dans EVOLVEpro, un système d’apprentissage machine fondé sur des modèles de langage proteique entraînés sur des millions de séquences naturelles. Cet outil a appris quelles caractéristiques favorisaient l’activité et a suggéré de nouvelles combinaisons de mutations censées être encore plus efficaces. À travers quelques cycles de cette boucle computationnelle–expérimentale, les scientifiques sont parvenus à deux variantes enzymatiques optimisées qui, associées au ωRNA amélioré, ont augmenté l’activité d’édition de plus de 60 fois par rapport au système de départ.
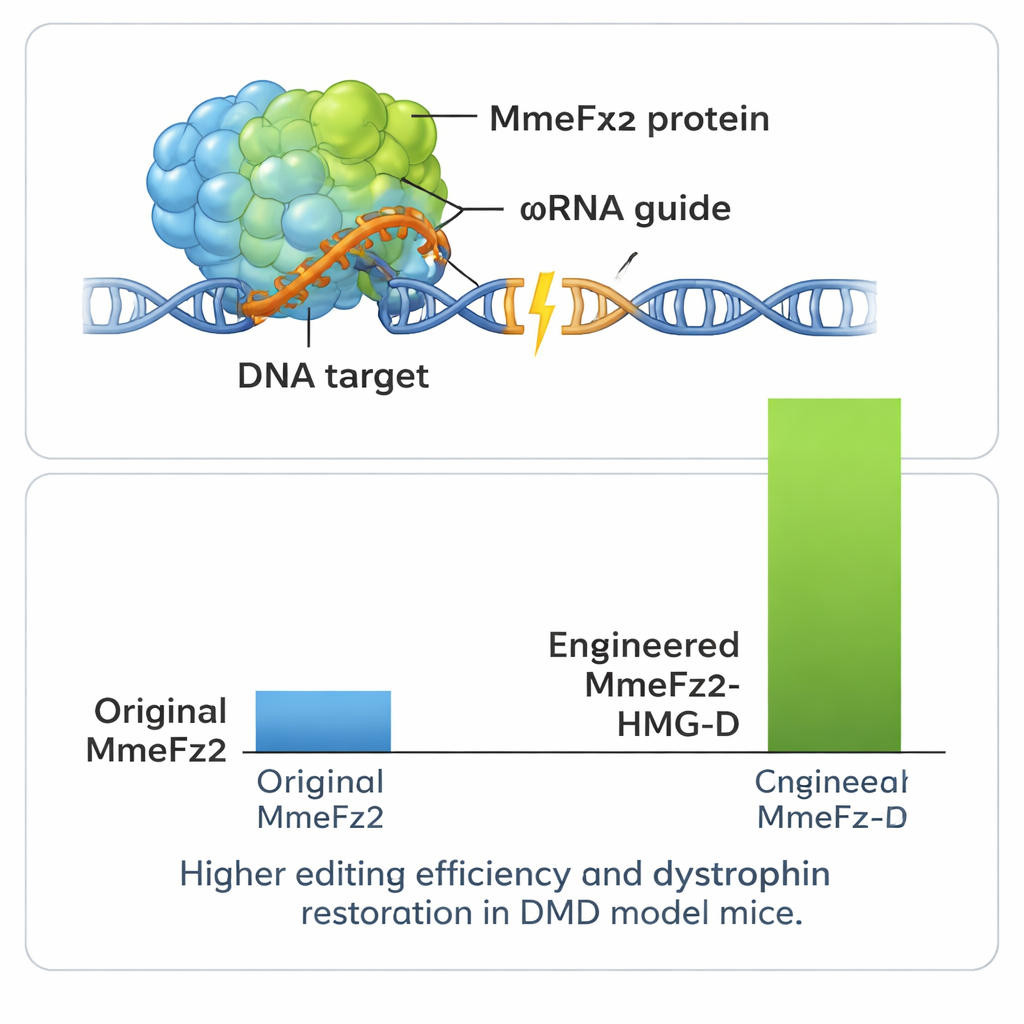
Accroître la puissance et tester dans un modèle de maladie
Pour extraire encore plus de performance du système, les auteurs ont fusionné MmeFz2 à de petits domaines de liaison à l’ADN qui aident les protéines à s’ancrer sur le matériel génétique. L’un d’eux, appelé HMG-D, s’est avéré particulièrement efficace lorsqu’il était fixé à l’extrémité de l’enzyme ingénierée, produisant des niveaux d’édition supérieurs à 80 % sur certains sites. Fait important, les tests sur des sites d’édition hors cible prédits dans le génome ont montré que cette puissance accrue n’entraînait pas une perte majeure de précision. Parce que l’éditeur de gène entier — protéine et ARN guide — est si compact, il tient confortablement dans un seul vecteur AAV, ce qui n’est pas possible pour la plupart des systèmes CRISPR. L’équipe a mis cet avantage à profit dans un modèle murin de la dystrophie musculaire de Duchenne, une maladie mortelle caractérisée par l’atrophie musculaire due à des erreurs dans le gène de la dystrophine. Une injection unique de l’éditeur délivré par AAV dans le muscle de la patte a entraîné des corrections détectables de l’ARN du gène et une restauration de la protéine dystrophine dans une fraction substantielle des fibres musculaires.
Ce que cela signifie pour les futures thérapies géniques
Pour les non-spécialistes, le message clé est que les auteurs ont transformé une enzyme de découpage génétique faible et obscure en un éditeur compact et performant qui peut être délivré dans un seul paquet viral et réparer une maladie génétique grave dans un modèle animal réaliste. Tout aussi important est le chemin suivi : en combinant étroitement la prédiction de structure basée sur l’IA et l’apprentissage automatique avec des tests de laboratoire ciblés, ils ont amélioré à la fois la protéine et son ARN guide beaucoup plus efficacement que par des approches traditionnelles d’essais et d’erreurs. Cette stratégie intégrée pourrait accélérer la création de nombreuses générations d’éditeurs du génome, rapprochant des thérapies géniques plus précises et plus sûres des patients atteints de dystrophie musculaire et d’autres maladies héréditaires.
Citation: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Mots-clés: édition génétique, alternatives au CRISPR, dystrophie musculaire de Duchenne, thérapie génique virale, intelligence artificielle en biologie