Clear Sky Science · fr
Des nanorobots camouflés ciblent et régulent les échanges subcellulaires des macrophages pour favoriser la régénération neuronale
Pourquoi de petits « assistants » camouflés comptent pour les lésions médullaires
Une lésion de la moelle épinière entraîne souvent une paralysie permanente parce que le tissu nerveux endommagé est extrêmement difficile à réparer. Une des raisons principales est que le site de la blessure devient une zone hostile, remplie d’inflammation et de stress cellulaire qui bloquent la guérison. Cette étude décrit un nouveau type de nanorobot camouflé qui circule dans le sang, contourne les défenses de l’organisme et reprogramme les cellules immunitaires au niveau de la lésion pour qu’elles passent d’un mode d’attaque à un mode de réparation, facilitant la repousse des nerfs chez des animaux souffrant d’une lésion de la moelle épinière.
Le problème : une inflammation qui ne s’éteint pas
Après une lésion médullaire, la première vague de dégâts provient du traumatisme physique lui‑même. Mais une seconde vague, plus lente, est alimentée par l’inflammation, des molécules toxiques appelées espèces réactives de l’oxygène et une mort cellulaire étendue. Des cellules immunitaires appelées macrophages affluent pour nettoyer les débris. Dans un premier temps, elles adoptent un état agressif « M1 » qui tue les agents pathogènes et les cellules endommagées mais libère aussi des signaux inflammatoires puissants. Pour qu’une véritable réparation commence, ces mêmes cellules doivent ensuite basculer vers un état apaisant « M2 » qui soutient la réparation tissulaire, la néovascularisation et la régénération nerveuse. Malheureusement, le stress intense dans le tissu lésé peut piéger les macrophages dans l’état délétère M1, verrouillant un cycle d’inflammation chronique qui empêche la récupération fonctionnelle.
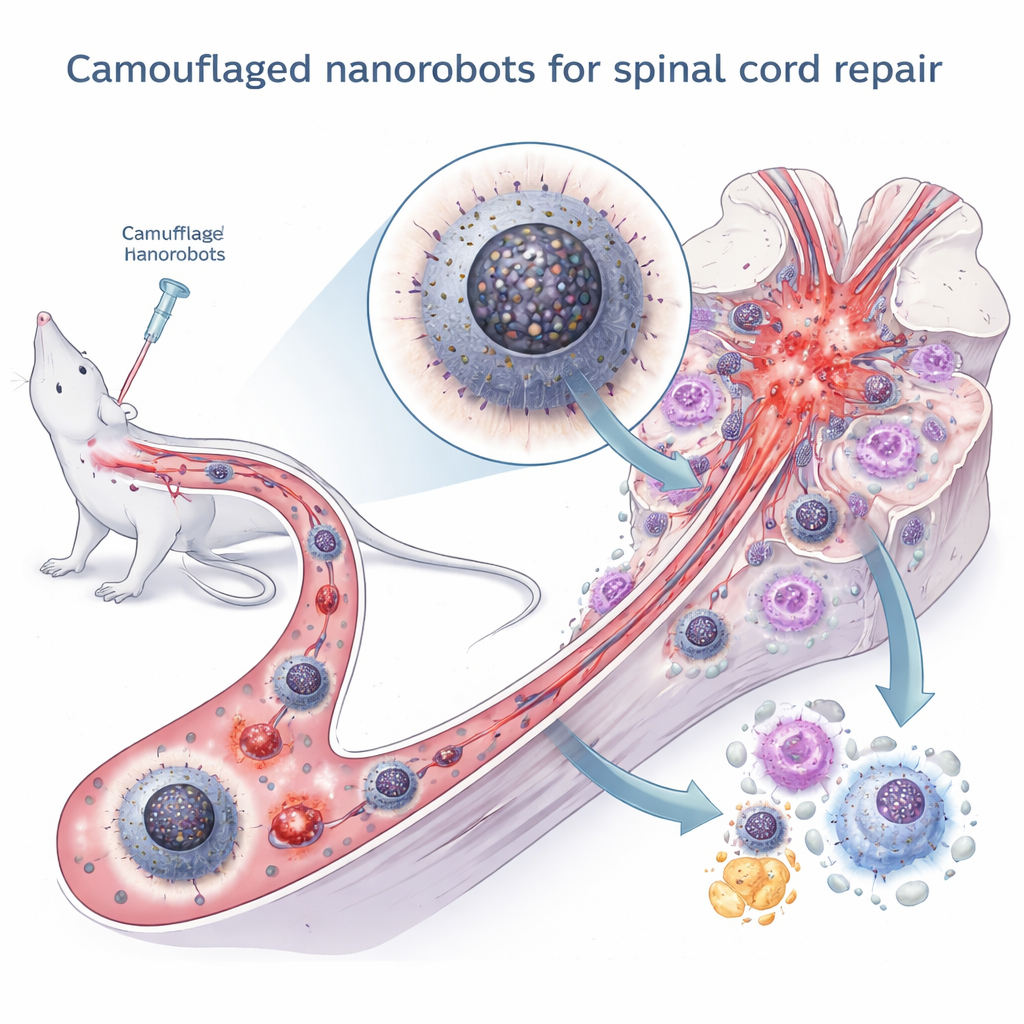
Conversation cachée entre composants cellulaires
Les auteurs se sont concentrés sur une « conversation » interne subtile mais cruciale au sein des macrophages : l’échange entre deux compartiments clés, le réticulum endoplasmique (qui aide au repliement des protéines et stocke le calcium) et les mitochondries (les centrales énergétiques de la cellule). Dans des conditions normales, ces structures partagent de petites quantités d’ions calcium via des zones de contact spécialisées, ce qui aide à l’ajustement de la production d’énergie aux besoins cellulaires. Après la blessure, cependant, un excès d’espèces réactives de l’oxygène provoque des erreurs de repliement protéique et du stress dans le réticulum endoplasmique. Ce stress entraîne à son tour un transfert excessif de calcium vers les mitochondries, conduisant à un effondrement énergétique, à la production de plus de molécules toxiques et à la fuite d’ADN mitochondrial dans le fluide cellulaire. Cet ADN échappé déclenche une voie d’alerte puissante appelée cGAS–STING–NFκB, qui maintient davantage les macrophages dans l’état inflammatoire M1.
Conception d’un nanorobot camouflé
Pour rompre ce cercle vicieux, l’équipe a construit un nanorobot multicouche nommé BP@D/N. En son cœur se trouvent des points quantiques de phosphore noir, de minuscules particules à forte activité antioxydante et anti‑inflammatoire mais de faible stabilité in vivo. Ces points sont encapsulés dans une coque creuse de polydopamine, un matériau biocompatible qui les protège d’une dégradation prématurée et apporte ses propres propriétés antioxydantes. Enfin, la particule entière est enveloppée d’une membrane prélevée sur des neutrophiles activés, un type de globule blanc naturellement attiré par les zones d’inflammation. Ce « déguisement » permet au nanorobot d’échapper à l’élimination immunitaire, de suivre les signaux inflammatoires jusqu’à la moelle épinière lésée et d’adhérer aux macrophages pour une prise en charge efficace.
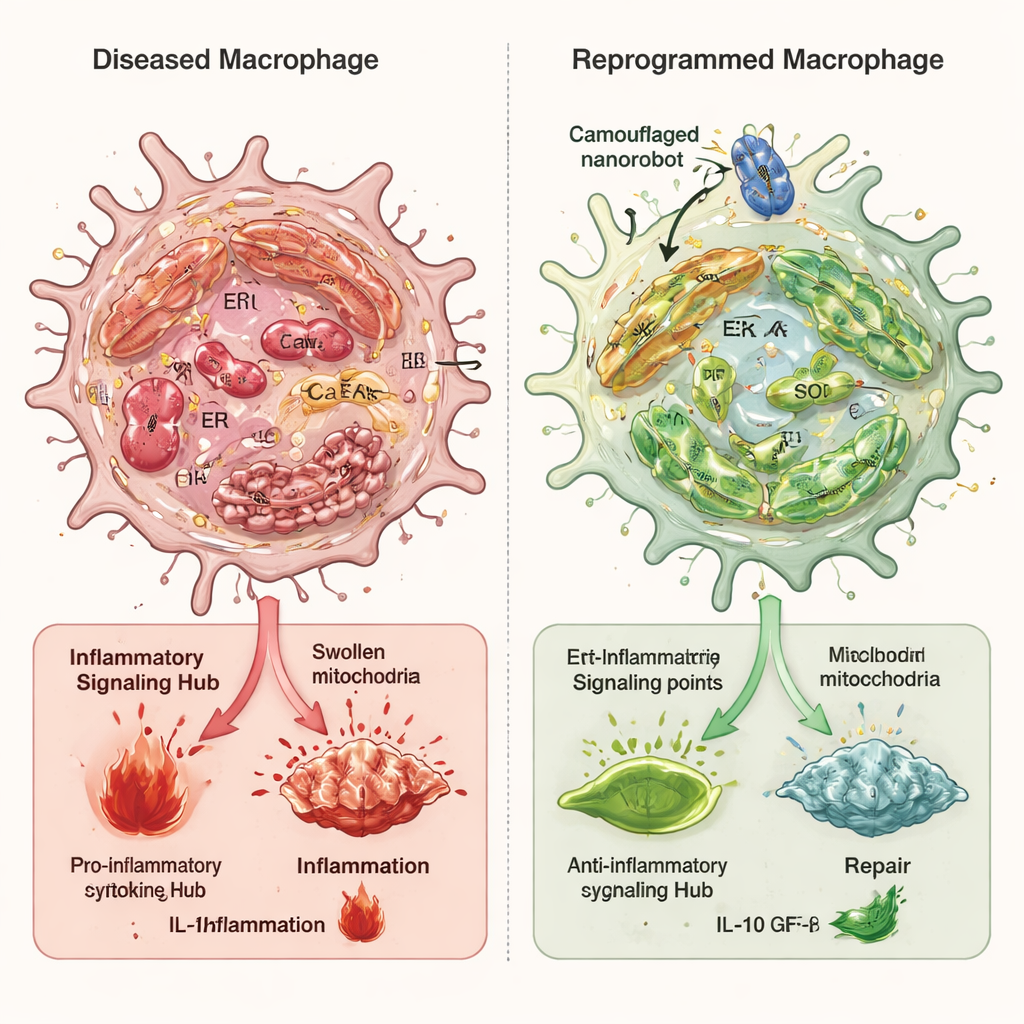
Reprogrammer des cellules immunitaires stressées
Dans des études cellulaires, des macrophages exposés à des déclencheurs inflammatoires présentaient de forts signes de stress du réticulum endoplasmique, des mitochondries gonflées et endommagées, une surcharge en calcium et une activation marquée de la voie d’alerte cGAS–STING–NFκB. Lorsqu’ils ont été traités avec les nanorobots camouflés, le stress oxydatif global a fortement diminué, les membranes internes entre le réticulum endoplasmique et les mitochondries sont devenues moins surconnectées, et le calcium mitochondrial est revenu vers la normale. Cela a empêché l’ADN mitochondrial de fuir dans le fluide cellulaire et a atténué la cascade de signalisation inflammatoire. Un acteur clé de ce processus est une enzyme appelée Ero1α, qui aide à contrôler l’environnement oxydatif et la libération de calcium du réticulum endoplasmique. Les nanorobots ont réduit l’activité d’Ero1α, et lorsque les chercheurs ont artificiellement augmenté Ero1α, cela a en grande partie annulé les bénéfices des nanorobots, confirmant son rôle central.
De l’apaisement de l’inflammation à la repousse des nerfs
Ces modifications internes ont fait basculer les macrophages de l’état destructeur M1 vers l’état réparateur M2. En culture, les cellules orientées M2 ont sécrété moins de molécules inflammatoires comme le TNF‑α et l’IL‑6 et davantage de facteurs de croissance qui encouragent les neurones et les cellules de soutien à croître et à étendre leurs axones. Chez des rats modèles de lésion médullaire, des injections répétées de nanorobots ont entraîné une diminution des signaux immunitaires délétères au niveau de la lésion, moins de cicatrisation excessive, une formation de cavités réduite et davantage de fibres nerveuses en régénération. Les animaux ayant reçu les nanorobots camouflés ont retrouvé une meilleure mobilité des membres postérieurs, des réponses musculaires plus fortes et une structure vésicale améliorée comparativement aux traitements non traités ou aux nanoparticules moins ciblées.
Ce que cela pourrait signifier pour les patients futurs
Ce travail montre que régler précisément le stress interne et la communication entre compartiments cellulaires peut transformer des cellules immunitaires nuisibles en alliées de la réparation nerveuse. En encapsulant des particules antioxydantes puissantes mais fragiles dans un nanorobot camouflé et ciblé, les chercheurs ont rétabli un équilibre plus sain entre inflammation et réparation dans la moelle épinière lésée de rats. Bien qu’il reste beaucoup de chemin avant de pouvoir tester cette approche chez l’humain, elle offre un plan prometteur : au lieu de simplement supprimer l’inflammation de manière générale, les thérapies futures pourraient orienter des machineries cellulaires spécifiques à l’intérieur des macrophages pour créer un environnement plus favorable à la régénération neuronale après une lésion de la moelle épinière.
Citation: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
Mots-clés: lésion de la moelle épinière, nanorobots, macrophages, régénération neuronale, nanomédecine