Clear Sky Science · fr
Caractérisation métabolique des interactions tumeur‑immunité par immunofluorescence multiplexée révèle des mécanismes spatiaux de réponse à l’immunothérapie dans le carcinome pulmonaire non à petites cellules (CPNPC)
Pourquoi cette recherche importe
L’immunothérapie a transformé le traitement pour certains patients atteints de cancer du poumon avancé, mais la majorité voit encore sa maladie progresser malgré ces médicaments puissants. Cette étude pose une question simple mais cruciale : peut‑on examiner plus finement le tissu tumoral lui‑même — où se trouvent les différentes cellules et quelle énergie elles consomment — pour prédire qui bénéficiera réellement de l’immunothérapie ? En transformant de petites biopsies en cartes cellulaires détaillées, les chercheurs visent à rapprocher la prise en charge du cancer du poumon d’une vraie médecine personnalisée.
Regarder l’intérieur des tumeurs pulmonaires comme une carte urbaine
L’équipe a analysé des prélèvements issus de 55 personnes atteintes de carcinome pulmonaire non à petites cellules (CPNPC) avancé traitées par inhibiteurs de points de contrôle immunitaire, une classe majeure d’immunothérapies. Avant traitement, leurs échantillons tumoraux ont été marqués avec un panel de 44 marqueurs par immunofluorescence multiplexée, permettant de visualiser de nombreux protéines simultanément. Un système d’apprentissage profond a ensuite identifié les types cellulaires clés — cellules tumorales, lymphocytes T, lymphocytes B, macrophages et fibroblastes — et classé leur état fonctionnel (par exemple activé, en division ou épuisé) ainsi que leur profil métabolique, c’est‑à‑dire la manière dont elles produisent et utilisent l’énergie. Plutôt que de se limiter au comptage des cellules, les chercheurs ont aussi cartographié leur position relative, créant des régions proches de voisinage au sein de chaque biopsie.
Tumeurs énergivores et leurs environs immunitaires
Un axe majeur portait sur le métabolisme — les façons dont les cellules génèrent le carburant nécessaire à leur croissance ou à la défense contre la maladie. Les chercheurs ont défini des « voisinages métaboliques » présentant différents niveaux et types d’activité énergétique, depuis des zones peu actives jusqu’à des zones très actives riches en phosphorylation oxydative et en glycolyse. Ils ont observé que les cellules tumorales et certains éléments du système immunitaire, comme les macrophages, présentaient souvent des voies de production d’énergie intenses. Certains de ces profils se sont corrélés aux résultats cliniques. Par exemple, les tumeurs montrant une activité élevée des voies permettant l’utilisation des acides aminés et le fonctionnement du cycle de l’acide citrique (TCA) étaient plus fréquentes chez les patients en rechute précoce après immunothérapie. En revanche, certains plasmocytes (lymphocytes B producteurs d’anticorps) présentant des voies énergétiques actives au sein de la tumeur étaient plus courants chez les patients ayant de meilleurs résultats, suggérant que toutes les cellules énergétiquement actives ne sont pas forcément néfastes — certaines peuvent soutenir une immunité antitumorale efficace.
Bons et mauvais acteurs immunitaires dans le paysage tumoral
Au‑delà de l’abondance simple, le type et le comportement des cellules immunitaires importaient également. Les macrophages exprimant la molécule cytotoxique granzyme B étaient fortement associés à une survie sans progression plus courte, en particulier lorsqu’ils se trouvaient dans des voisinages métaboliquement faibles ou inactifs. Ces régions pourraient représenter des zones pauvres en nutriments ou en dormance où l’attaque immunitaire est atténuée. À l’inverse, certaines dispositions de cellules T régulatrices (Tregs) et de fibroblastes à la frontière entre la tumeur et le tissu environnant semblaient liées à de meilleurs résultats, ce qui pourrait refléter un schéma où les cellules suppressives restent en périphérie plutôt que d’infiltrer profondément la tumeur. Des ratios entre différents types de cellules immunitaires, comme celui des granulocytes par rapport aux cellules T CD8, suivaient aussi la réponse, soulignant que l’équilibre et la localisation du système immunitaire, et non seulement les comptes totaux, sont importants.
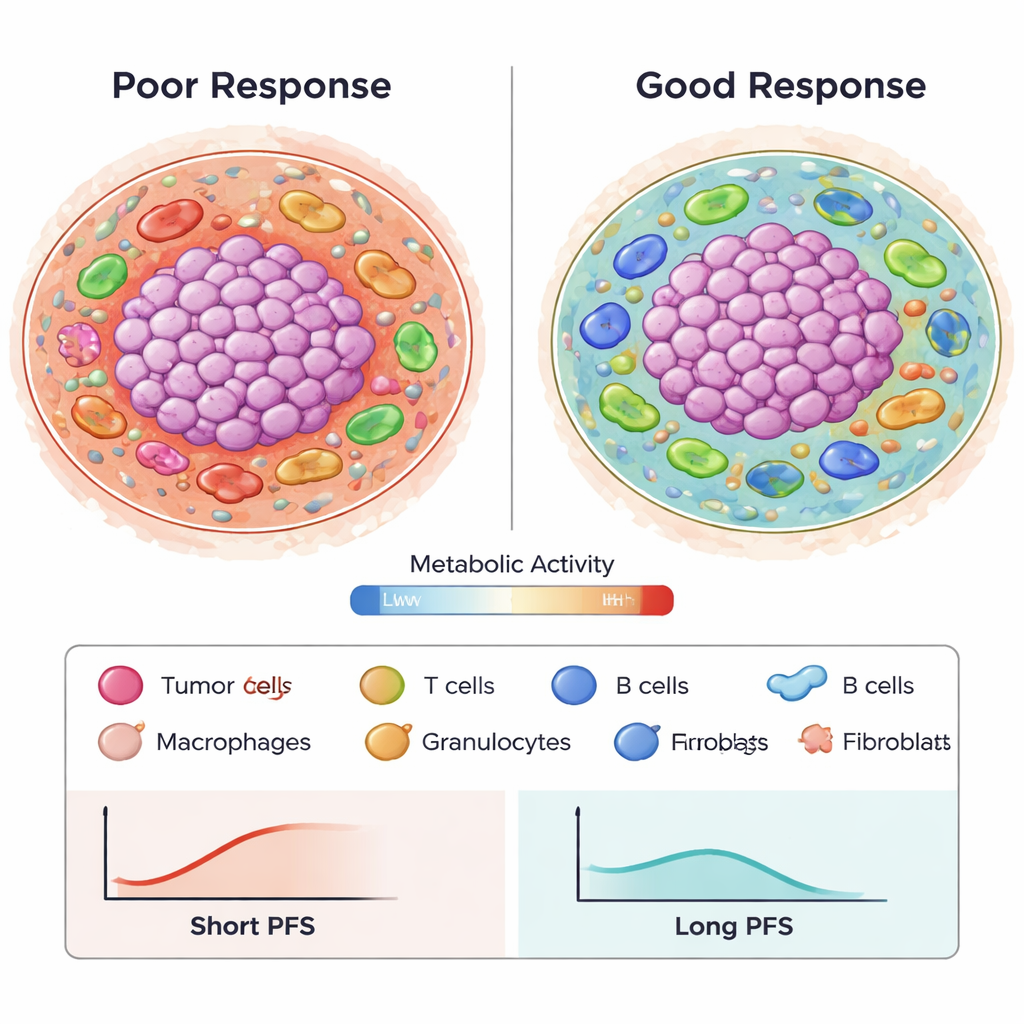
Des images complexes aux motifs prédictifs
Pour interpréter plus d’un million de caractéristiques spatiales construites décrivant types cellulaires, distances et états métaboliques, les auteurs ont utilisé une méthode avancée de sélection de variables (Stabl) et des outils de modélisation de survie. Ils ont identifié 87 caractéristiques clés, beaucoup reflétant comment des cellules tumorales métaboliquement actives interagissent avec des macrophages et des lymphocytes T, ou comment des types cellulaires immunitaires spécifiques se regroupent près des vaisseaux sanguins et des fibroblastes. En utilisant ces caractéristiques dans des modèles de régression de Cox, ils ont construit un prédicteur estimant la survie sans progression avec une précision (AUC) d’environ 0,8 sur 24 mois, surpassant des marqueurs uniques traditionnels comme la coloration PD‑L1 ou la charge mutationnelle tumorale dans des travaux antérieurs. De manière importante, plusieurs caractéristiques se sont révélées reproductibles dans deux cohortes indépendantes de patients, suggérant que ces motifs ne sont pas de simples artefacts.
Ce que cela signifie pour les patients
Pour un non‑spécialiste, le message essentiel est que la localisation des cellules dans une tumeur pulmonaire et leur façon de se nourrir peuvent aider à expliquer pourquoi certains patients répondent bien à l’immunothérapie tandis que d’autres n’y répondent pas. Cette étude montre que des informations spatiales et métaboliques riches issues d’une biopsie de routine, combinées à l’intelligence artificielle et à la modélisation statistique, peuvent révéler des signatures de bénéfice probable ou de résistance. Bien que ces travaux nécessitent une validation dans des cohortes plus larges et sur des sections tissulaires entières, ils tracent une voie vers des tests futurs capables d’indiquer aux cliniciens, avant le début du traitement, quels patients ont le plus de chances d’obtenir un contrôle durable par l’immunothérapie et lesquels pourraient nécessiter des stratégies alternatives ou des combinaisons thérapeutiques.
Citation: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Mots-clés: résistance à l’immunothérapie, cancer du poumon non à petites cellules, microenvironnement tumoral, biologie spatiale, métabolisme du cancer