Clear Sky Science · fr
Hydrogel portant des signaux d'adhésion cellule‑cellule améliore la régénération neuronale
Aider le cerveau blessé à se réparer
Les traumatismes crâniens peuvent laisser des troubles durables du mouvement, de la mémoire et du raisonnement parce que les neurones endommagés du cerveau repoussent rarement ou ne se reconnectent pas correctement. Les médecins peuvent retirer des caillots sanguins ou stabiliser le crâne, mais disposent de peu d’outils pour reconstruire le réseau délicat du cerveau. Cette étude décrit un matériau mou et riche en eau, appelé hydrogel, conçu pour imiter la façon dont les cellules cérébrales s’attachent naturellement les unes aux autres. En recréant ces minuscules « poignées de main » entre cellules, le matériau favorise la repousse des fibres nerveuses endommagées, la formation de nouvelles connexions et la restauration des fonctions dans des cerveaux de rats blessés.
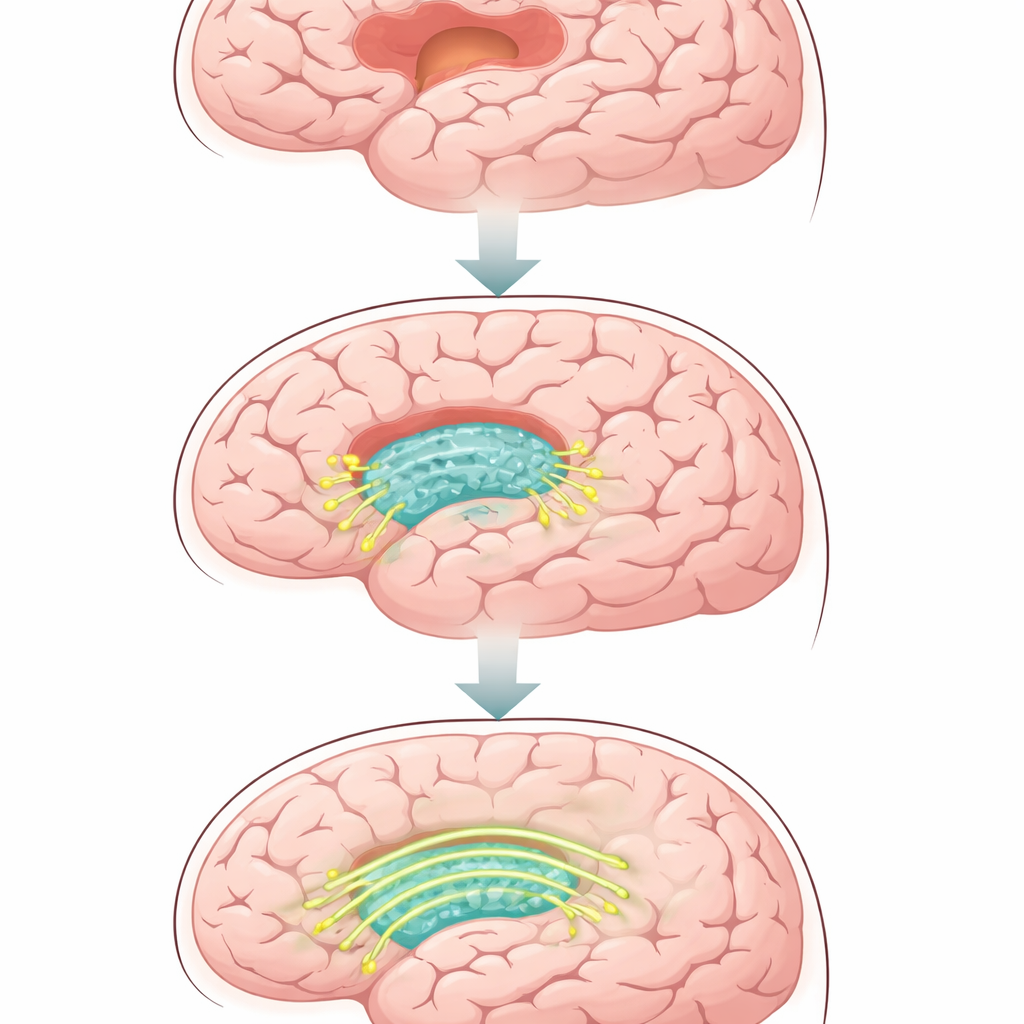
Un échafaudage souple pour le tissu cérébral abîmé
Les chercheurs ont commencé par un hydrogel à base de soie qui a une texture similaire au tissu cérébral — très souple et flexible, avec de minuscules pores où les cellules peuvent se déplacer et étendre leurs prolongements. Ils ont ensuite recouvert ce gel d’une fine couche fluide de molécules lipidiques qui se comporte comme une membrane cellulaire. Cette couche peut contenir des protéines particulières tout en leur permettant de dériver latéralement, exactement comme sur de vraies cellules. Le résultat est un matériau tridimensionnel injectable capable de remplir des plaies cérébrales irrégulières et de présenter des signaux mobiles aux neurones voisins, plutôt que d’être un simple remplissage passif.
Emprunter la poignée de main cellule‑à‑cellule de la nature
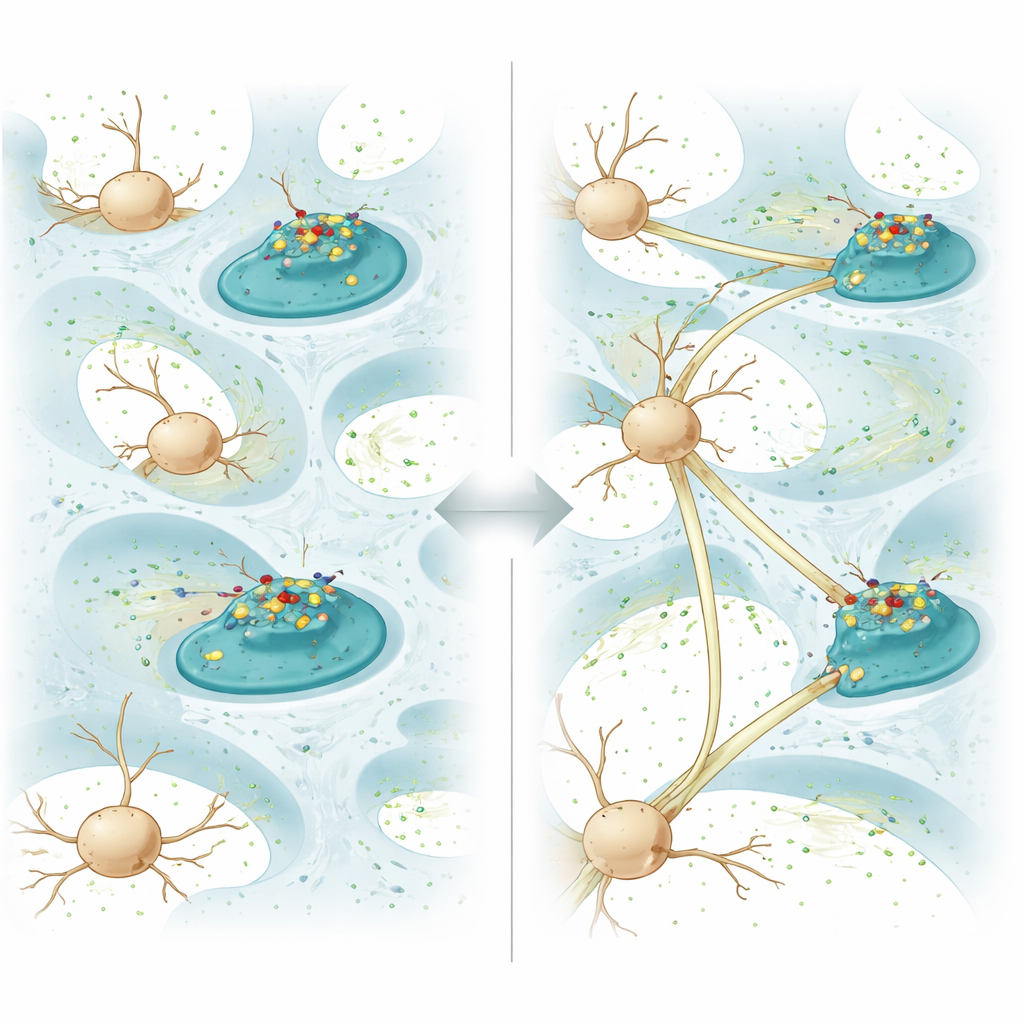
Pour faire de l’hydrogel un partenaire actif dans la réparation, l’équipe a fixé une protéine appelée N‑cadherine à la couche lipidique. Dans le cerveau, la N‑cadherine se trouve à la surface des neurones et aide les cellules voisines à se reconnaître et à se saisir, formant des contacts stables et, éventuellement, des synapses où les signaux passent d’une cellule à l’autre. Dans ce gel, la N‑cadherine n’est pas verrouillée en place ; elle peut diffuser librement à travers la couche. Lorsque les neurones poussent contre le gel, la protéine s’agrège aux points où leurs membranes touchent le matériau, remodelant les petits prolongements cellulaires et déclenchant la formation de jonctions cellule‑à‑cellule. En culture, les neurones cultivés sur ce gel à « N‑cadherine diffusive » ont étendu des fibres plus longues, formé davantage de connexions et montré une communication électrique plus forte que sur des gels similaires où la protéine était immobilisée.
Réveiller les programmes internes de réparation du cerveau
Au‑delà du simple contact, l’hydrogel incite aussi les neurones à activer des voies internes de réparation. Des analyses génétiques et protéiques ont montré que les cellules sur le gel à N‑cadherine diffusive réduisaient les signaux favorisant la mort cellulaire programmée et renforçaient les voies connues pour soutenir la croissance et la survie. En particulier, le matériau augmentait les niveaux d’une protéine appelée thrombospondine‑1, libérée par les cellules de soutien du cerveau et qui peut à la fois favoriser la formation de synapses et activer des voies pro‑croissance. Deux de ces voies, souvent désignées TGF‑β/Smad et AKT/mTOR, étaient fortement activées, conduisant à des mitochondries en meilleure santé, à une production d’énergie accrue et à une régénération renforcée des fibres nerveuses sectionnées dans un modèle microfluidique imitant des axones coupés.
De la boîte de Petri au cerveau vivant
Pour vérifier si ces effets avaient un impact dans un cerveau vivant, l’équipe a injecté l’hydrogel dans des rats soumis à une forme contrôlée de traumatisme crânien. Sur plusieurs semaines, les animaux traités avec le gel à N‑cadherine diffusive ont obtenu de meilleures performances aux tests moteurs et au labyrinthe aquatique évaluant l’apprentissage et la mémoire, comparativement aux animaux ayant reçu du gel neutre, du gel lipidique seul ou du sérum physiologique. Les imageries cérébrales et les coupes de tissu ont révélé des cavités plus petites sur le site de la lésion et davantage de fibres nerveuses et de synapses nouvellement formées dans la région réparée. Parallèlement, les cerveaux traités présentaient moins de cellules immunitaires hyperactives et un tissu cicatriciel moins dense, créant un environnement plus propice à la repousse. Les marqueurs de la mort cellulaire étaient réduits, tandis que les protéines associées à une communication saine entre neurones étaient augmentées.
Pourquoi cela compte pour la réparation cérébrale future
En termes simples, ce travail montre que fournir au tissu cérébral blessé le bon type de « signaux sociaux » peut faire une grande différence dans sa capacité à guérir. Plutôt que de soutenir les cellules uniquement sur le plan mécanique, l’hydrogel recrée les signaux de contact mobiles que les vraies cellules cérébrales utilisent pour se repérer et se maintenir ensemble. Chez le rat, cette stratégie n’a pas seulement comblé les cavités du cerveau, mais a également aidé à reconstruire des circuits neuronaux fonctionnels et amélioré le comportement après lésion. Bien que de nombreux tests restent à réaliser avant qu’un tel matériau puisse être utilisé chez l’humain, l’approche — intégrer des protéines d’adhésion cellulaire librement mobiles dans des gels mous et injectables — pourrait s’étendre au‑delà de la N‑cadherine et du cerveau, offrant une recette générale pour des matériaux guidant activement la régénération tissulaire.
Citation: Tang, X., Zhang, S., Liu, M. et al. Hydrogel with cell-cell adhesion cues enhances neural regeneration. Nat Commun 17, 2178 (2026). https://doi.org/10.1038/s41467-026-68632-9
Mots-clés: régénération neuronale, traumatisme crânien, échafaudage hydrogel, adhésion cellulaire, N‑cadherine