Clear Sky Science · fr
H3K9me2 médiée par G9a orchestre la régénération épithéliale intestinale via le silence épigénétique de gènes liés au cycle cellulaire
Pourquoi l’autoréparation de l’intestin est importante
Chaque jour, la muqueuse de votre intestin fait face à des conditions rudes : acide gastrique, particules alimentaires et des milliers de milliards de microbes. Pourtant, ce tissu non seulement survit, il se répare en permanence. Quand ce système de réparation échoue — après une radiothérapie, dans les maladies inflammatoires de l’intestin ou lors d’infections graves — les patients peuvent souffrir de douleur, d’hémorragie et de complications potentiellement mortelles. Cette étude met au jour un « interrupteur » caché à l’intérieur des cellules intestinales qui les aide à décider quand quitter l’état de repos pour se mettre à reconstruire, offrant des pistes pour de nouveaux traitements susceptibles de renforcer l’équipe naturelle de réparation de l’intestin.
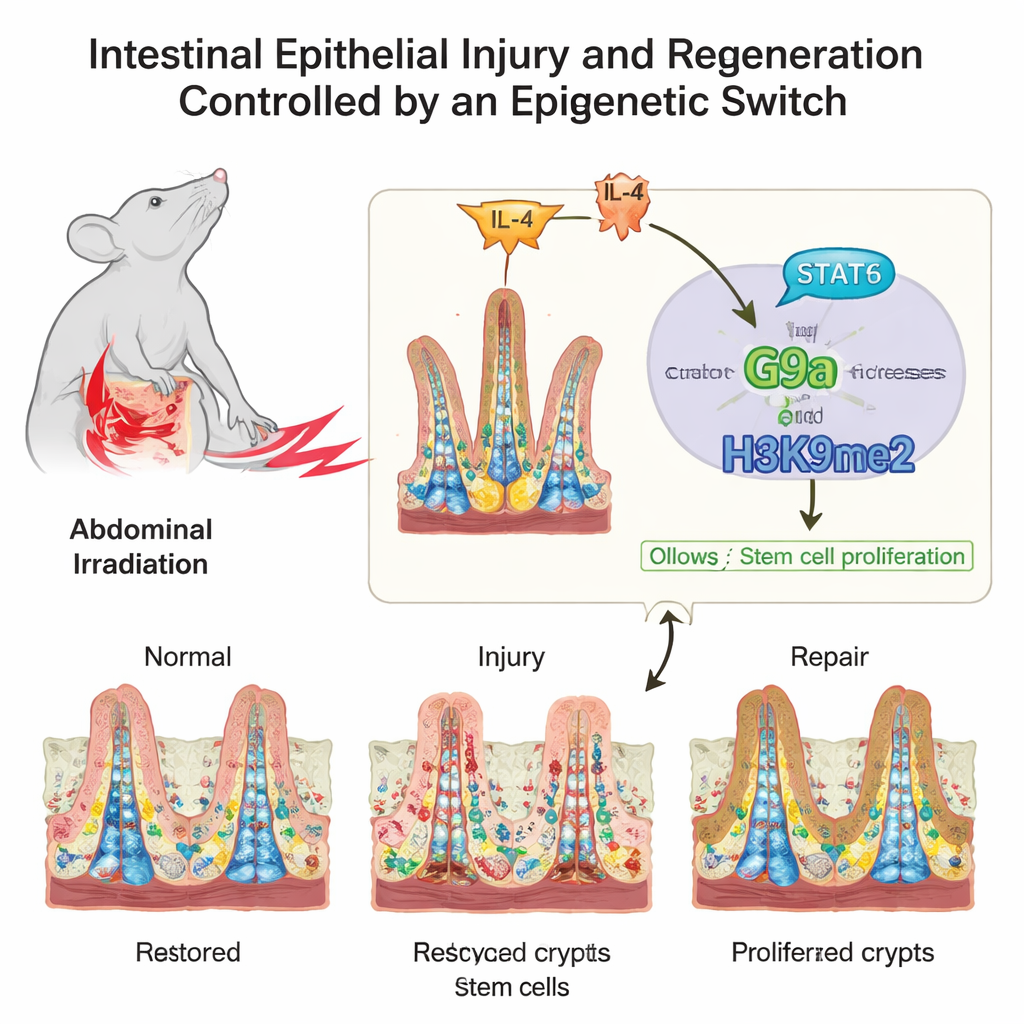
Une architecture délicate soumise à un stress constant
La surface interne de l’intestin ressemble, au microscope, à un tapis à poils, avec des villosités en forme de doigts qui absorbent les nutriments et des creux appelés cryptes où résident les cellules souches. Ces cellules souches, et leurs filles à division rapide, doivent trouver un équilibre entre renouvellement continu et réparation d’urgence. Les auteurs se sont intéressés à la façon dont des marques chimiques sur les protéines qui emballent l’ADN, appelées histones, influencent cet équilibre. Ces marques ne modifient pas les gènes eux‑mêmes, mais agissent davantage comme des variateurs d’intensité, augmentant ou diminuant l’expression de groupes de gènes lorsque l’intestin passe de la vie normale à la lésion, puis au rétablissement.
Une marque épigénétique qui suit la lésion et la guérison
En utilisant des souris exposées à la radiation — une cause fréquente de lésion intestinale pendant le traitement du cancer — les chercheurs ont analysé de nombreuses marques d’histones dans les cryptes riches en cellules souches. Une marque, connue sous le nom de H3K9me2, a fortement augmenté lorsque l’intestin passait de l’état de lésion à la phase de réparation. Son enzyme rédactrice, une protéine appelée G9a, a suivi le même schéma. L’équipe a ensuite examiné des échantillons humains provenant de patients ayant reçu une radiothérapie pelvienne, ainsi que de personnes atteintes de la maladie de Crohn. Dans les deux contextes, des niveaux plus élevés de H3K9me2 et de G9a dans les cellules intestinales s’associaient à de meilleurs signes de réparation tissulaire, suggérant que ce système est conservé entre souris et humains.
Quand l’interrupteur de réparation est cassé
Pour savoir si cette marque est simplement un témoin ou si elle pilote véritablement la guérison, les scientifiques ont supprimé G9a spécifiquement dans l’épithélium intestinal des souris, ou ont bloqué son activité avec un médicament. Dans les deux cas, les niveaux de H3K9me2 ont diminué. Après irradiation ou lésion chimique, ces souris ont perdu plus de poids, présenté des intestins plus courts et plus endommagés, et montré moins de cryptes et de cellules souches régénératrices que les animaux normaux. Même sans lésion délibérée, la muqueuse intestinale des souris déficientes en G9a paraissait atrophiée : les cryptes étaient moins profondes, les villosités plus courtes, et le nombre de cellules souches ainsi que de leurs descendants spécialisés était réduit. De minuscules « mini‑intestins » cultivés à partir de ces cellules en culture se développaient aussi mal, soulignant que ce système moléculaire est central au renouvellement quotidien de l’intestin.
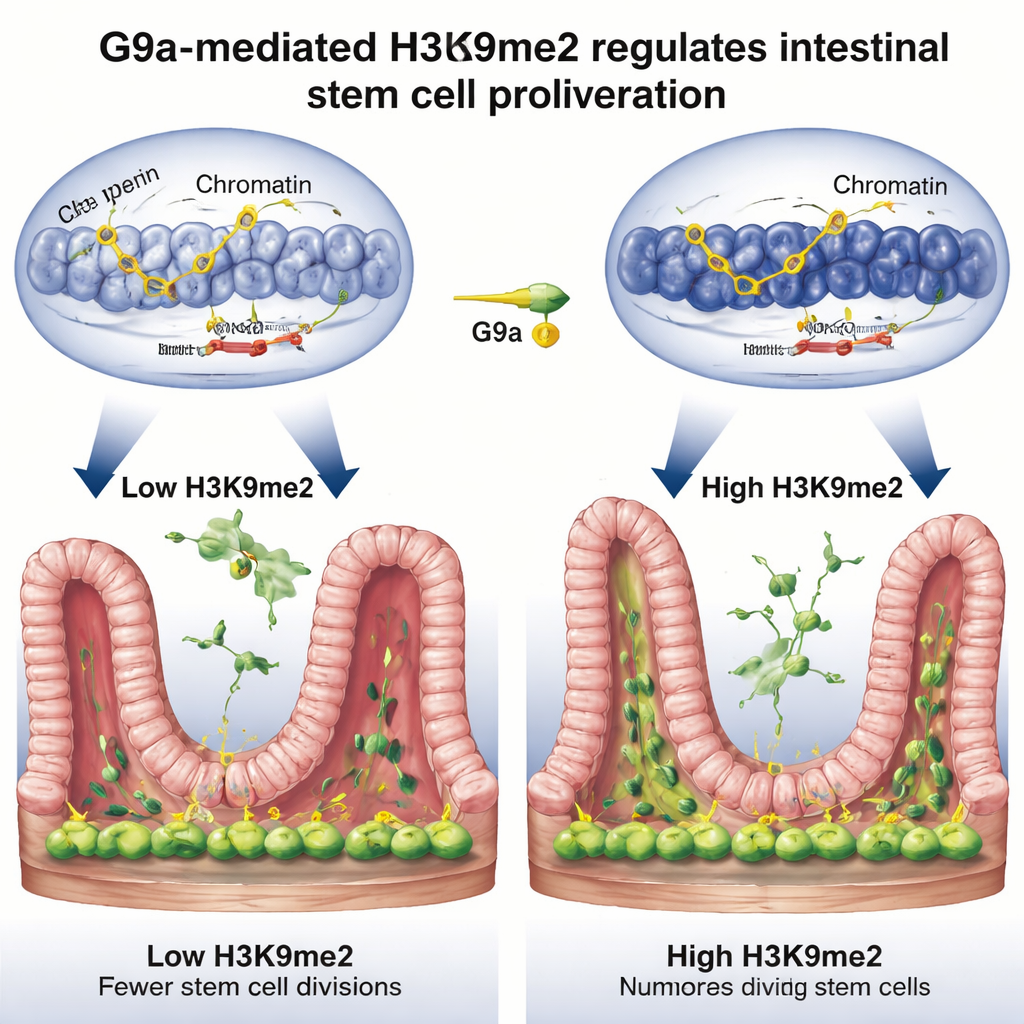
Relâcher les freins de la division cellulaire
Approfondissant leur investigation, l’équipe a cherché quels gènes sont contrôlés par cet interrupteur de réparation. En combinant trois méthodes génomiques puissantes, ils ont trouvé que H3K9me2, placée par G9a, se situe préférentiellement sur des régions d’ADN qui agissent normalement comme des freins du cycle cellulaire — des gènes tels que Rb1cc1, Rb1, Cdkn1a et Pten, qui ralentissent ou arrêtent la division cellulaire. Quand G9a faisait défaut, la marque chimique disparaissait de ces régions, l’ADN environnant s’ouvrait, et ces gènes freins s’exprimaient plus fortement, entraînant une prolifération ralentie des cellules souches. Pendant la réparation normale après lésion, les niveaux de H3K9me2 sur ces gènes augmentaient, leur activité diminuait, et les cellules souches pouvaient se diviser plus librement pour reconstruire la muqueuse. En substance, G9a et H3K9me2 étouffent temporairement les signaux d’arrêt pour permettre la régénération tissulaire.
Une chaîne de signalisation reliant les signaux immunitaires à la réparation
L’intestin n’agit pas seul ; il est constamment à l’écoute des signaux du système immunitaire. Les chercheurs ont retracé un de ces signaux en amont de G9a. Après lésion, les niveaux du messager immunitaire IL‑4 augmentent, déclenchant l’activation d’une protéine appelée STAT6 à l’intérieur des cellules intestinales. STAT6 activé se lie directement à la région de contrôle du gène G9a, augmentant sa production. Cela crée une chaîne de commandement : IL‑4 active STAT6, STAT6 stimule G9a, et G9a ajoute la marque H3K9me2 pour silencer les gènes freins du cycle cellulaire, permettant aux cellules souches de s’étendre et de restaurer la muqueuse endommagée.
Ce que cela signifie pour les traitements futurs
Pour un non‑spécialiste, ces résultats montrent que la réparation intestinale est guidée non seulement par les gènes, mais aussi par des marques chimiques réversibles qui règlent finement l’utilisation de ces gènes. La voie IL‑4–STAT6–G9a–H3K9me2 agit comme un panneau de contrôle interne qui desserre les freins de la division des cellules souches juste assez longtemps pour guérir, puis peut être réinitialisée. À l’avenir, des thérapies qui renforcent modérément cette voie — par exemple des médicaments ou des outils génétiques qui augmentent les niveaux de G9a au bon moment et au bon endroit — pourraient aider les patients à se remettre plus rapidement d’une lésion par radiation, des poussées de maladie inflammatoire de l’intestin ou d’autres affections endommageant la muqueuse intestinale, tout en minimisant les risques de prolifération cellulaire incontrôlée.
Citation: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Mots-clés: régénération intestinale, épigénétique, cellules souches, méthylation des histones, maladie inflammatoire de l’intestin