Clear Sky Science · fr
WDR5 remodèle les condensats de NANOG pour piloter des programmes transcriptionnels et maintenir l’identité des cellules souches
Pourquoi cela compte pour les cellules souches et le cancer
Les cellules souches ont la capacité remarquable de devenir de nombreux types cellulaires différents, une propriété qui sous-tend le développement précoce, la réparation tissulaire et, malheureusement, certains cancers. Cette étude révèle comment deux protéines clés, NANOG et WDR5, coopèrent pour maintenir les cellules souches dans cet état flexible. En montrant que WDR5 peut remodeler physiquement la façon dont NANOG se regroupe sur l’ADN, le travail relie la physique des gouttelettes protéiques à l’intérieur du noyau au contrôle des gènes, tant dans les cellules saines que dans la leucémie.
Des protéines qui décident du futur d’une cellule
Les cellules souches embryonnaires conservent la pluripotence — c’est‑à‑dire la capacité de devenir presque n’importe quelle cellule — grâce à des régulateurs maîtres tels que NANOG, OCT4 et SOX2. Ces protéines activent et répriment des réseaux entiers de gènes. NANOG occupe une place particulièrement centrale : il se lie à l’ADN mais recrute aussi de larges complexes enzymatiques qui ajoutent des marques chimiques activatrices aux histones, les protéines qui empaquettent l’ADN. WDR5 est un autre acteur crucial : il aide les machines qui modifient les histones à déposer des marques indiquant des gènes actifs. Bien que NANOG et WDR5 soient connus pour soutenir l’identité des cellules souches, on ignorait comment ils interagissaient au niveau moléculaire et si cela influait sur la façon dont ils forment de minuscules gouttelettes — ou « condensats » — dans le noyau.
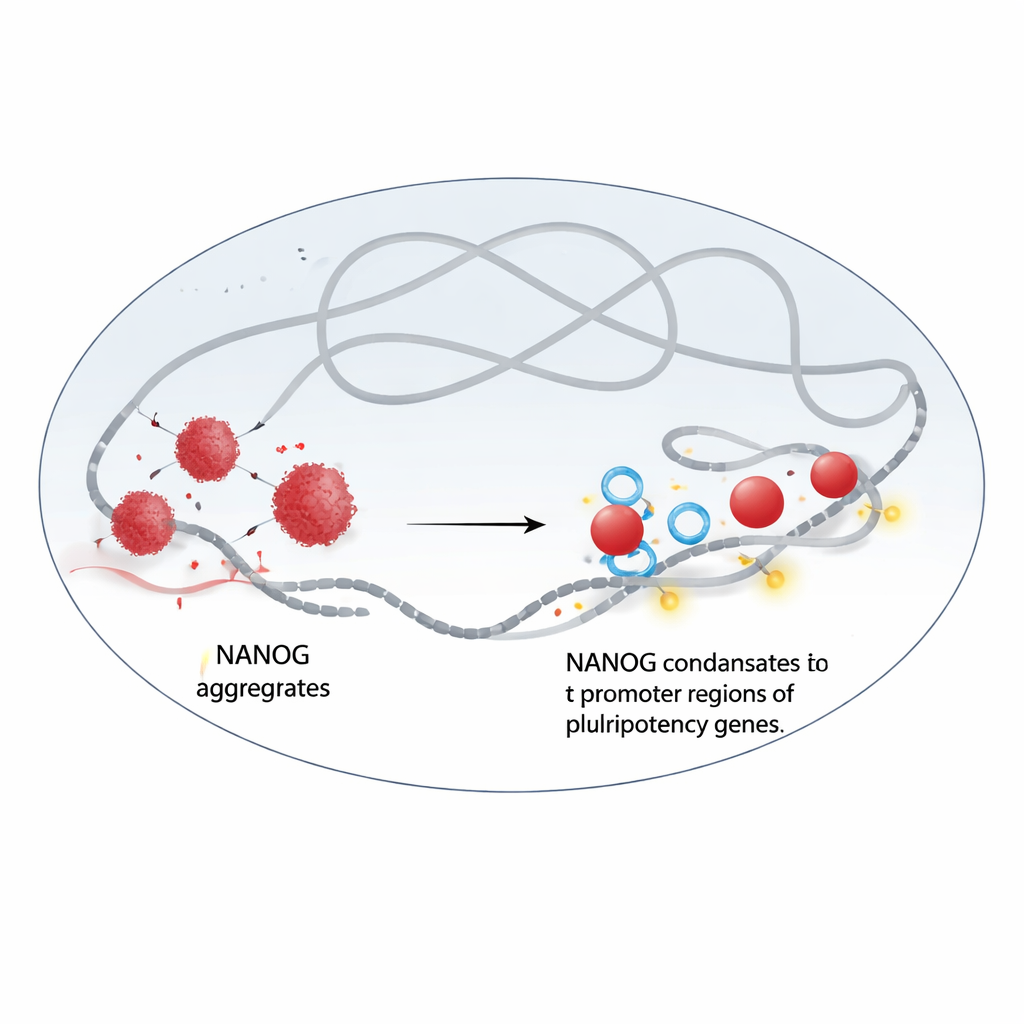
Des amas aux gouttelettes liquides
Les auteurs ont découvert que NANOG et WDR5 interagissent directement. Lorsqu’il est purifié seul, NANOG a tendance à former des amas irréguliers et de type solide. Grâce à la microscopie électronique et à des expériences de fluorescence, l’équipe a montré que l’ajout de WDR5 réorganise ces amas en gouttelettes rondes et de type liquide qui se comportent comme des condensats dynamiques. Dans des cellules vivantes, NANOG et WDR5 se rassemblent en points nucléaires brillants qui se dissolvent rapidement lorsqu’on les traite par une substance chimique connue pour perturber la séparation liquide‑liquide de phase. Quand cela se produit, les deux protéines perdent une grande partie de leur ancrage à la chromatine, le complexe ADN–protéines qui stocke l’information génétique, et leur présence aux gènes clés de la pluripotence chute nettement.
Une poignée moléculaire particulière
Pour comprendre ce partenariat à l’échelle atomique, les chercheurs ont résolu la structure cristalline de la région de NANOG qui lie l’ADN liée à WDR5. À la différence de nombreux autres partenaires de WDR5, qui utilisent de courts segments flexibles, NANOG engage WDR5 via une surface étendue comprenant à la fois un bras non structuré et des hélices voisines. Un seul acide aminé arginine dans NANOG, à la position 153, s’insère profondément dans un canal central de WDR5, constituant une partie essentielle de l’interaction « serrure‑clé ». Le remplacement de ce résidu par une alanine (la mutation R153A) élimine en grande partie la liaison. De manière importante, le NANOG mutant peut encore se lier à l’ADN, mais WDR5 ne parvient plus à remodeler efficacement ses agrégats en gouttelettes fluides, indiquant que ce contact spécifique est indispensable à la formation de condensats fonctionnels.
Conserver la jeunesse des cellules souches — et ce qui se passe quand cela échoue
Lorsque les auteurs ont modifié des cellules souches embryonnaires de souris pour qu’elles n’expriment que le mutant NANOG R153A, les conséquences furent spectaculaires. Les cellules mutantes perdirent les colonies serrées en forme de dôme typiques des cellules pluripotentes et s’aplatirent, signe visuel de différenciation. Elles formèrent moins de colonies positives pour la phosphatase alcaline, autre marqueur de la « stemness », et réduisirent l’expression de nombreux gènes centraux de la pluripotence tels que Nanog lui‑même, Sox2, Esrrb et Klf4. Parallèlement, des gènes associés à des lignées spécifiques, notamment des régulateurs du développement osseux, furent activés. Le profilage à l’échelle du génome révéla que NANOG et WDR5 n’occupèrent plus conjointement des milliers de promoteurs, et deux marques d’activation histone clés, H3K4me3 et H4K16ac, disparurent spécifiquement sur ces sites partagés. Au début de la différenciation, ces marques chimiques et les ARN nouvellement synthétisés déclinaient avant que les niveaux d’ARNm totaux ne chutent, suggérant une défaillance initiale dans le maintien d’une chromatine active.
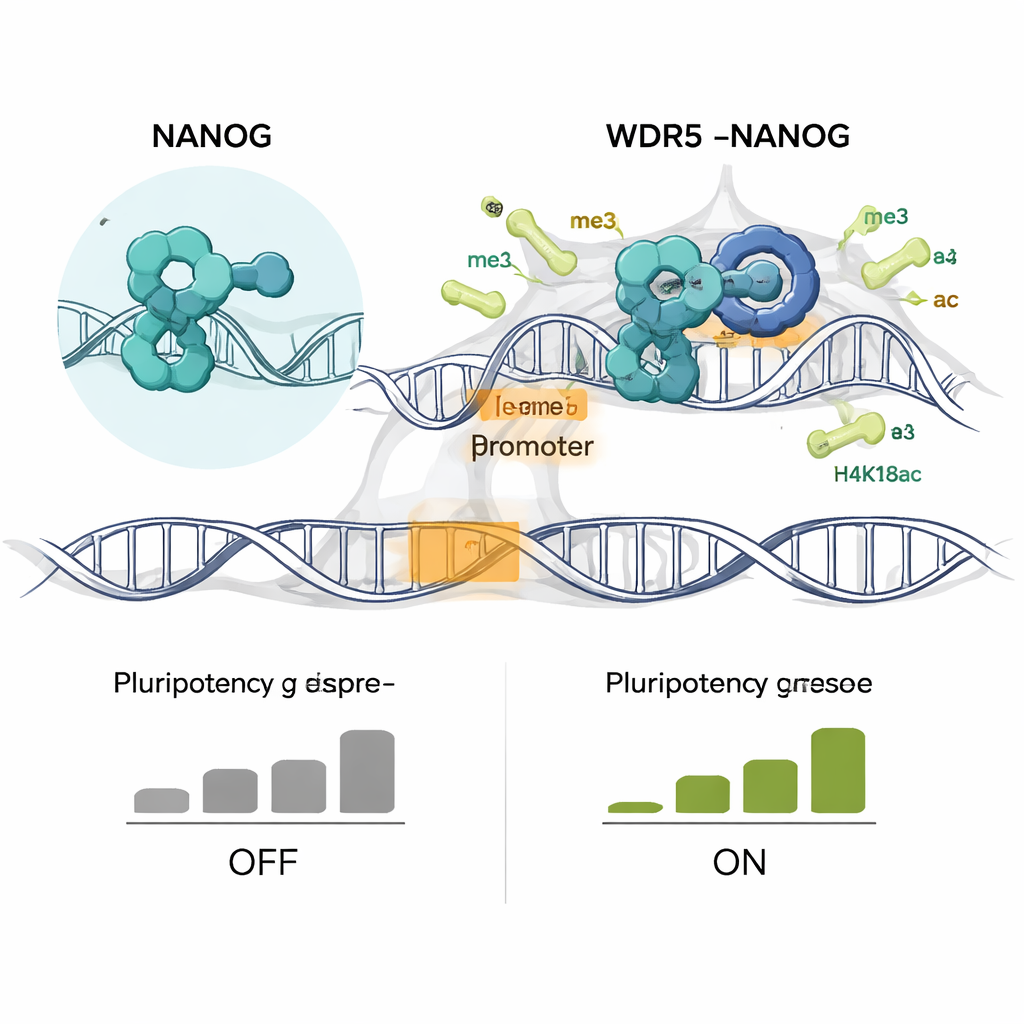
Transformer un mécanisme fondamental en stratégie anti‑cancer
Parce que des réseaux géniques similaires pilotent certaines cellules souches cancéreuses, l’équipe a testé si perturber l’axe NANOG–WDR5 pouvait freiner les cellules souches leucémiques dans un modèle murin de leucémie myéloïde aiguë. Une petite molécule, C16, qui se lie au même creux de WDR5 utilisé par NANOG, affaiblit sélectivement l’interaction WDR5–NANOG. Dans les cellules leucémiques, C16 réduisit fortement la formation de colonies, épuisa la population de cellules de type souche et poussa les cellules vers des destins myéloïdes matures, tout en épargnant beaucoup plus les cellules souches sanguines normales qu’un médicament leucémique existant ciblant un autre partenaire de WDR5. Le séquençage de l’ARN montra que C16 éteignait les programmes géniques de stemness et d’auto‑renouvellement et favorisait les voies de différenciation. Chez la souris, le traitement par C16 réduisit les populations de cellules souches et progénitrices leucémiques, soulignant le potentiel thérapeutique de cibler ce partenariat protéique.
Vue d’ensemble : comment les gouttelettes aident à décider l’identité cellulaire
Ce travail montre que WDR5 fait plus que se poser sur la chromatine et recruter des enzymes : il peut remodeler physiquement NANOG, le transformant d’agrégats inertes en condensats liquides flexibles qui siègent sur les promoteurs des gènes de pluripotence et attirent des marques d’histone activatrices. Lorsque ce remodelage est bloqué — soit par une mutation précise dans NANOG, soit par une petite molécule qui perturbe leur contact — les cellules souches perdent leur identité et les cellules souches cancéreuses perdent leur capacité d’auto‑renouvellement. Pour le lecteur non spécialiste, le message clé est que de petits changements dans la façon dont les protéines s’organisent en gouttelettes sur l’ADN peuvent avoir des conséquences majeures : qu’une cellule reste jeune et flexible, qu’elle mûrisse vers un destin spécifique, ou qu’elle alimente une maladie.
Citation: Wang, D., Shi, X., Xie, J. et al. WDR5 remodels NANOG condensates to drive transcriptional programs and sustain stem cell identity. Nat Commun 17, 1907 (2026). https://doi.org/10.1038/s41467-026-68623-w
Mots-clés: pluripotence des cellules souches, NANOG, WDR5, séparation de phase, cellules souches de leucémie